Filomena Fezza1,2,*, Monica Bari 1, Rita Florio3, Emanuela Talamonti4,5, Monica Feole1,2 και Mauro Maccarrone2,5,* “Endocannabinoids, Related Compounds and Their Metabolic Routes” Molecules. 2014 Nov; 19(11): 17078–17106, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6271436/
1 Department of Experimental Medicine & Surgery, Tor Vergata University of Rome, 00133 Rome, Italy; E-Mails: bari@med.uniroma2.it (M.B.); monica.feole@hotmail.it (M.F.)
2 European Center for Brain Research/IRCCS Santa Lucia Foundation, 00143 Rome, Italy
3 Department of Movement, Human and Health Sciences, Foro Italico University of Rome, 00128 Rome, Italy; E-Mail: rit.flo@libero.it
4 Endocannabinoid Research Group, Istituto di Chimica Biomolecolare, Consiglio Nazionale delle Ricerche, 80078 Pozzuoli (NA), Italy; E-Mail: emanuelatalamonti.86@libero.it
5 Center of Integrated Research, Campus Bio-Medico University of Rome, 00135 Rome, Italy
* Authors to whom correspondence should be addressed: E-Mails: filomena.fezza@uniroma2.it (F.F.); m.maccarrone@unicampus.it (M.M.).
Εξωτερικός επιμελητής: Derek J. McPhee
Παραλαβή: 1 Αυγούστου 2014, σε αναθεωρημένη μορφή: 16 Οκτωβρίου 2014 / Αποδοχή: 16 Οκτωβρίου 2014 / Δημοσίευση: 24 Οκτωβρίου 2014
Περίληψη
“Τα ενδοκανναβινοειδή είναι λιπιδικοί μεσολαβητές ικανοί να δεσμεύονται και να ενεργοποιούν τους κανναβινοειδείς υποδοχείς, τους πρωταρχικούς μοριακούς στόχους που είναι υπεύθυνοι για τις φαρμακολογικές επιδράσεις της Δ9-τετραϋδροκανναβινόλης. Αυτά τα βιοενεργά λιπίδια ανήκουν κυρίως σε δύο κατηγορίες ενώσεων: Ν-ακυλαιθανολαμίνες (N-acylethanolamines) και ακυλεστέρες (acylesters,), από τους οποίους η Ν-αραχιδονοϋλαιθανολαμίνη (N-arachidonoylethanolamine, AEA) και η 2-αραχιδονοϋλογλυκερόλη (2-arachidonoylglycerol, 2-AG), είναι αντίστοιχα οι κύριοι εκπρόσωποί τους. Κατά τη διάρκεια των τελευταίων είκοσι ετών, έχει ανακαλυφθεί ένας συνεχώς αυξανόμενος αριθμός παραγώγων λιπαρών οξέων (ενδοκανναβινοειδή και ενώσεις που μοιάζουν με ενδοκανναβινοειδή) και οι βιολογικές τους δραστηριότητες αποτελούν αντικείμενο έντονων ερευνών. Εδώ, θα ανασκοπηθούν οι πιο πρόσφατες εξελίξεις, από θεραπευτική άποψη, σχετικά με τα ενδοκανναβινοειδή, τις σχετικές ενώσεις και τις μεταβολικές οδούς τους”.
Λέξεις-κλειδιά: anandamide, 2-arachidonoylglycerol, endocannabinoid metabolic routes, fatty acids (ανανδαμίδιο, 2-αραχιδονοϋλογλυκερόλη, ενδοκανναβινοειδείς μεταβολικές οδοί, λιπαρά οξέα, αντίστοιχα).
1. Εισαγωγή
Οι βιολογικές επιδράσεις της κάνναβης (που λανθασμένα αναφέρεται ως marijuana / μαριχουάνα), της Δ9-τετραϋδροκανναβινόλης (Δ9-tetrahydrocannabinol, THC), του κύριου ψυχοδραστικού συστατικού της, διαμεσολαβούνται από δύο κανναβινοειδείς υποδοχείς συζευγμένους με πρωτεΐνη G (GPCR), τύπου-1 (CB1R) και τύπου-2 (CB2R) κανναβινοειδείς υποδοχείς[1].
Η εύρεση των γονιδίων που κωδικοποιούν τους CBRs οδήγησε στην αναζήτηση των ενδογενών συνδετών τους [που ονομάζονται “ενδοκανναβινοειδή (eCBs)” (endocannabinoids)] και των ενζύμων που είναι υπεύθυνα για τη σύνθεση και την αποικοδόμηση των eCBs, οδηγώντας με τη σειρά της στην ανακάλυψη μιας εντελώς νέας ενδογενούς σηματοδότησης σύστημα, τώρα γνωστό ως “ενδοκανναβινοειδές σύστημα (ΕΚΣ)” (endocannabinoid system (ECS))[2,3].
Σύμφωνα με την υψηλή λιποφιλικότητα της THC (Εικόνα 1), όλα τα eCBs προέρχονται από ακόρεστα λιπαρά οξέα[4]. Οι πιο σημαντικοί από αυτούς τους ενδογενείς συνδέτες είναι δύο παράγωγα αραχιδονικού οξέος (arachidonic acid, ΑΑ): Ν-αραχιδονοϋλαιθανολαμίνη (N-arachidonoylethanolamine) (ανανδαμίδιο / anandamide, ΑΕΑ) [5] και 2-αραχιδονοϋλογλυκερόλη (2-arachidonoylglycerol) (2-AG) (Εικόνα 1 και Πίνακας 1)[6,7], που ανήκουν στις μεγάλες οικογένειες των Ν-ακυλαιθανολαμινών (N-acylethanolamines, NAEs) και των 2-μονοακυλογλυκερολών (2-monoacylglycerols, MAGs), αντίστοιχα.
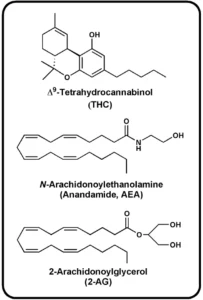
Εικόνα 1. Χημικές δομές της THC και από τα δύο εξέχοντα ενδοκανναβινοειδή
Πίνακας 1. eCBs και ενώσεις που μοιάζουν με eCBs, οι μοριακοί στόχοι τους, βιοσυνθετικά και καταβολικά ένζυμα
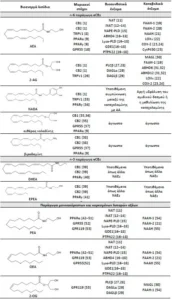
Σημειώσεις: ABHD4, α/β-υδρολάση 4 (α/β-hydrolase 4), ABHD6/12, περιοχή α/β-υδρολάσης 6/12 (α/β-hydrolase domain 6/12), CB1, κανναβινοειδείς υποδοχείς τύπου-1 (type-1 cannabinoid receptors), CB2, κανναβινοειδείς υποδοχείς τύπου 2 (type-2 cannabinoid receptors), COX-2, κυκλοοξυγενάση-2 (cyclooxygenase-2), Cyt P450, κυτόχρωμα P450 (cytochrome P450), DAGLα/β, λιπάση διακυλογλυκερόλης α/β (diacylglycerol lipase α/β), FAAH, υδρολάση αμιδίου λιπαρού οξέος (fatty acid amide hydrolase), GPR55, ορφανός συζευγμένος με πρωτεΐνη G υποδοχέας 55 (orphan G protein-coupled receptor 55), LOXs, λιποξυγενάσες (lipoxygenases), MAGL, μονοακυλογλυκερολική λιπάση (monoacylglycerol lipase), NAAA, αμιδάση οξέος υδρολυτικής Ν-ακυλαιθανολαμίνης (N-acylethanolamine-hydrolyzing acid amidase), NAPE-PLD, Ν-ακυλο-φωσφατιδυλαιθανολαμίνες-υδρολύουσα φωσφολιπάση D (N-acyl-phosphatidylethanolamines-hydrolyzing phospholipase D), NAT, Ν-ακυλοτρανσφεράση (N-acyltransferase), iNAT, Ca2+-ανεξάρτητη Ν-ακυλοτρανσφεράση (Ca2+-independent N-acyltransferase), PLCβ, φωσφολιπάση Cβ (phospholipase Cβ), PPARα/γ, ενεργοποιημένος από πολλαπλασιαστή υπεροξισώματος υποδοχέας α/γ (peroxisome proliferator-activated receptor α/γ), PTPN22, πρωτεϊνική φωσφατάση τυροσίνης μη υποδοχέας τύπου 22 (protein tyrosine phosphatase, non-receptor type 22), TRPV1, κανάλι βανιλλοειδούς δυναμικού παροδικού υποδοχέα τύπου 1 (transient receptor potential vanilloid type 1 channel)
Επιπλέον, άλλες ενώσεις ω-6 (n-6) λιπαρών οξέων, συμπεριλαμβανομένων της Ν-διομο-γ-λινολενολαιθανολαμίνης (N-dihomo-γ-linolenoylethanolamine), Ν-αραχιδονοϋλδοπαμίνης (N-arachidonoyldopamine, NADA), του 2-αραχιδονοϋλογλυκεραιθέρας (2-arachidonoylglycerylether) (νολαδινικός αιθέρας / noladin ether) και της Ο-αραχιδονοϋλ-αιθανολαμίνης (O-arachidonoylethanolamine) (βιροδαμίνη / virodhamine) (Πίνακας 1), έχουν επίσης βρεθεί ότι αλληλεπιδρούν με τους CBRs, αν και με διαφορετική ισχύ και αποτελεσματικότητα όπως αναφέρεται σε μια ολοκληρωμένη ανασκόπηση[1] και συνοψίζεται στον Πίνακα 1. Έχουν επίσης ανακαλυφθεί δύο μεταβολικά σημαντικές αιθανολαμίνες ω-3 (n-3) λιπαρών οξέων (ω-3 (n-3) fatty acid ethanolamines): Ν-εικοσαπενταενολαιθανολαμίνη (N-eicosapentaenoylethanolamine, EPEA) και Ν-εικοσιδυοεξαενοϋλαιθανολαμίνη (N-docosahexaenoylethanolamine, DHEA) (Πίνακας 1)[56,57]. Αυτά τα n-3 eCBs έχουν προταθεί ως πρόσθετοι αγωνιστές των CBRs[58], αλλά η φαρμακολογία και η βιολογική τους συνάφεια μένει να διευκρινιστεί.
Το ΕΚΣ περιπλέκεται περαιτέρω από σημαντικές ενώσεις που σχετίζονται δομικά με τα eCBs και ονομάζονται ουσίες που “μοιάζουν με eCBs” (eCBs-like). Τα τελευταία βρίσκονται συχνά σε πολύ υψηλότερες ποσότητες από το ΑΕΑ και στερούνται συγγένειας με CBRs. Ωστόσο, μεταβολίζονται από τα ίδια ένζυμα σύνθεσης και αποδόμησης με τα αυθεντικά eCBs[11]. Μεταξύ αυτών των ενώσεων, το Ν-ακυλο παράγωγο του παλμιτικού οξέος (palmitic acid) και τα Ν- και Ο-ακυλο παράγωγα του ελαϊκού οξέος (oleic acid) (Πίνακας 1) είναι ιδιαίτερα σχετικά.
Οι βιολογικές δράσεις των eCBs και των ομοειδών ουσιών ελέγχονται μέσω μη πλήρως χαρακτηρισμένων κυτταρικών μηχανισμών, που περιλαμβάνουν βασικούς παράγοντες που είναι υπεύθυνοι για: (i) σύνθεση AEA και 2-AG, όπως οι Ν-ακυλο-φωσφατιδυλαιθανολαμίνες (NAPE) που υδρολύουν φωσφολιπάση D (N-acyl-phosphatidylethanolamines (NAPE)-hydrolyzing phospholipase D, NAPE-PLD) και η ειδική για sn-1 λιπάση διακυλογλυκερόλης (sn-1-specific diacylglycerol lipase, DAGL), αντίστοιχα και (ii) την αποικοδόμησή τους, όπως η υδρολάση αμιδίου λιπαρού οξέος (fatty acid amide hydrolase, FAAH) και η μονοακυλογλυκερολική λιπάση (monoacylglycerol lipase, MAGL), αντίστοιχα. Είναι αξιοσημείωτο ότι τα τελευταία χρόνια έχουν περιγραφεί πολλαπλές οδοί για το μεταβολισμό των eCBs (ειδικά για τις NAEs) και θα περιγραφούν αργότερα σε αυτήν την ανασκόπηση.
Ισχυρά φαρμακολογικά και βιοχημικά στοιχεία έχουν δείξει ότι τα eCBs και τα σχετικά μόρια είναι επίσης ικανά να αλληλεπιδρούν με στόχους που δεν είναι CBRs, αυξάνοντας την πολυπλοκότητα του ΕΚΣ και των μοριακών οδών που ενεργοποιούνται από αυτό. Συγκεκριμένα, ο πιο γνωστός μη-CBR στόχος των eCBs είναι ο παροδικός δυναμικός υποδοχέας βανιλλοειδούς τύπου 1 (transient receptor potential vanilloid type 1, TRPV1), ο οποίος ενεργοποιείται τόσο από το AEA[8] όσο και από την 2-AG[26].
Άλλοι πιθανοί υποδοχείς που ενεργοποιούνται από τα eCBs είναι οι υποδοχείς που ενεργοποιoύνται από πολλαπλασιαστή υπεροξισώματος α και γ (peroxisome proliferator-activated receptor α and γ, PPARα / PPARγ)[9] και ο ορφανός συζευγμένος με πρωτεΐνη G υποδοχέας (orphan G protein-coupled receptor, GPR55)[10,37,52]. Στον Πίνακα 1 τα παλιά και τα νέα μέλη του ΕΚΣ παρατίθενται μαζί. Το ΕΚΣ έχει αποδειχθεί ότι ρυθμίζει διαφορετικές φυσιολογικές διεργασίες στο κεντρικό νευρικό σύστημα (ΚΝΣ) και στην περιφέρεια[59-63], υποδηλώνοντας έτσι ότι ο σηματοδότης του μπορεί να ενθαρρύνει την ανάπτυξη φαρμάκων επιλεκτικών οδών για θεραπευτικό όφελος[39,63- 68].
Σε αυτήν την ανασκόπηση, παρουσιάζουμε την τελευταία γνώση αιχμής σχετικά με τα eCBs, τις σχετικές ενώσεις και τις μεταβολικές οδούς τους με αναφορά στον πιθανό θεραπευτικό τους ρόλο.
2. Σύστημα Ενδοκανναβινοειδών (Endocannabinoids System)
Αν και πολλοί GPCRs (υποδοχείς συζευγμένοι με πρωτεΐνη G / G protein-coupled receptors) έχουν ενδογενείς συνδέτες που είναι υδρόφιλα κατιόντα, οι CBRs έχουν ουδέτερους, εξαιρετικά λιπόφιλους συνδέτες που προέρχονται από λιπαρά οξέα. Οι διαφορές στην αμοιβαία ενδογενή συγκέντρωση των eCBs, τη συγγένεια των υποδοχέων και τον ασύμμετρο εντοπισμό (ενδοκυτταρικό και ιστό) των μεταβολικών τους ενζύμων υποστηρίζουν διακριτούς ρόλους για αυτά τα μόρια κάτω από διάφορες φυσιολογικές συνθήκες (πχ. σε διαφορετικές μορφές συναπτικής πλαστικότητας)[2,69-75].
2.1. Ενδογενείς συνδέτες κανναβινοειδών υποδοχέων (Endogenous Ligands of Cannabinoid Receptors)
2.1.1. Κύρια ενδοκανναβινοειδή
Η αναζήτηση για ενδογενείς συνδέτες των θέσεων δέσμευσης της THC αποδείχθηκε δύσκολη στην αρχή, επειδή οι υδατοδιαλυτές ουσίες αναζητήθηκαν κατ’ αναλογία με τις ενδορφίνες. Αργότερα, η λιπιδική φύση της THC οδήγησε στην ανακάλυψη δύο εικοσανοειδών: της Ν-αραχιδονοϋλεθανολαμίνης, που ονομάζεται “ανανδαμίδιο” από τη σανσκριτική λέξη “ananda” για την εσωτερική ευδαιμονία[5], και τη 2-αραχιδονοϋλογλυκερόλη (Εικόνα 1)[6,7].
Έχουν διεξαχθεί πολυάριθμες μελέτες για το ΑΕΑ από το 1992. Αυτό το eCB βρέθηκε αρχικά στον εγκέφαλο και στη συνέχεια σε πολλά άλλα όργανα και υγρά[76]. Το AEA μοιράζεται πολλές ιδιότητες με την THC και δρα ως μερικός αγωνιστής του CB1 και ως ασθενής μερικός αγωνιστής/ανταγωνιστής του CB2[1].
Ωστόσο, θα πρέπει να επισημανθεί ότι το ΑΕΑ είναι παρών, συχνά σε χαμηλές ποσότητες[72], σε περιοχές με υψηλή ή χαμηλή πυκνότητα CBRs, γεγονός που υποδηλώνει την πιθανότητα να ενεργοποιεί άλλους υποδοχείς[1].
Οι σχετικά χαμηλές ποσότητες ΑΕΑ μπορούν να εξηγηθούν λαμβάνοντας υπόψη τη βιοδιαθεσιμότητα του προδρόμου του και επιπλέον μπορεί να υπάρχει θέμα από την αδυναμία μέτρησης της ακριβούς τοπικής συγκέντρωσης[72].
Αντίθετα, τα επίπεδα του δεύτερου eCB, της 2-AG, είναι συνήθως σημαντικά υψηλότερα από εκείνα του AEA στους ίδιους ιστούς[76]. Η 2-AG δρα ως πλήρης αγωνιστής στους CBRs και έχει προταθεί ως ο κύριος ενδογενής αγωνιστής και για τους υποδοχείς CB1 και CB2[1]. Τα δύο κύρια eCBs έχουν διαφορετική συγγένεια με τους CBRs, στην πραγματικότητα η 2-AG εμπλέκεται σε ανάδρομη σηματοδότηση που εξαρτάται από τον CB1, ενώ το AEA είναι μόνο υπό ορισμένες προϋποθέσεις, προκαλώντας την αναστολή της προσυναπτικής απελευθέρωσης του διεγερτικού νευροδιαβιβαστή γλουταμικού ή/και του ανασταλτικού νευροδιαβιβαστή GABA (γάμμα-αμινοβουτυρικό οξύ / gamma-aminobutyric acid)[77-79].
Συγκεκριμένα, η 2-AG, εκτός από το ότι δρα ως eCB, είναι επίσης ένας σημαντικός ενδιάμεσος στον μεταβολισμό των λιπιδίων και, ως εκ τούτου, οι φυσιολογικές συγκεντρώσεις της μπορεί να μην αντικατοπτρίζουν μόνο την ποσότητα που απαιτείται για την ενεργοποίηση των CBRs[69]. Πράγματι, η 2-AG θεωρείται από καιρό ως προϊόν αποικοδόμησης φωσφολιπιδίων ινοσιτόλης και ως πιθανή πηγή αραχιδονικού οξέος σε διεγερμένα κύτταρα. Επιπλέον, κατά την αξιολόγηση των επιπέδων της 2-AG, είναι απαραίτητο να ληφθεί υπόψη ότι αυτή η ένωση (όπως και όλες οι 2-ακυλογλυκερίνες) υφίσταται μετανάστευση ακυλίου σε θερμοκρασία δωματίου σε υδατικά μέσα, με αποτέλεσμα την ισορροπία του κυρίαρχου 1(3)-AG (90%) με την ίδια την 2-AG (10%)[80].
Επιπλέον, αν και διαφορετικές μελέτες υποστηρίζουν την υπόθεση ότι η σύνθεση των διαιτητικών λιπαρών οξέων μπορεί να επηρεάσει τα επίπεδα των eCBs (και των ενώσεων που μοιάζουν με eCBs) με συγκεκριμένο χρόνο και ιστό[56,81,82], ωστόσο δεν υπάρχουν αλλαγές στο αίμα, τα eCBs βρέθηκαν με δίαιτες χαμηλής και υψηλής περιεκτικότητας σε λιπαρά σε παχύσαρκα και φυσιολογικού βάρους άτομα, αλλά, στον ίδιο διαγωνισμό, αναφέρθηκε μια τροποποίηση στους σκελετικούς μυς των υποδοχέων CB1 και MAGL[83]. Άλλες μελέτες έχουν δείξει ότι μια δίαιτα χαμηλή σε n-3 πολυακόρεστα λιπαρά οξέα σε ποντίκια προκαλεί επιδείνωση των λειτουργιών του υποδοχέα CB1 στους απογόνους[84]. Συγκεκριμένα, το επίπεδο των eCBs (και των ενώσεων που μοιάζουν με eCBs) ποικίλλει ανάλογα με τις φυσιολογικές και παθολογικές συνθήκες, και συχνά η περιεκτικότητα σε ξεχωριστά παράγωγα λιπαρών οξέων ρυθμίζεται ανεξάρτητα[38,85] και αυτή η διαφορετική ρύθμιση προσφέρει τη δυνατότητα να ενεργούν επιλεκτικά στη συγκέντρωση του παραγώγου ενδιαφέροντος με πιθανή ευεργετική επίδραση.
2.1.2. Πρόσθετα n-6-Ενδοκανναβινοειδή
Τα τελευταία χρόνια, έχουν ανιχνευθεί διαφορετικά παράγωγα ΑΑ με κανναβιμιμητικές ιδιότητες, υποδηλώνοντας την ύπαρξη νέων μελών της οικογένειας των ενδοκανναβινοειδών. Ειδικότερα, ένα eCB τύπου αιθέρα, 2-αραχιδονυλ-γλυκερυλαιθέρας (2-arachidonoyl-glyceryl ether) ή νολαδινικός αιθέρας (noladin ether) (Πίνακας 1)[84] και ένα παράγωγο ΑΑ και αιθανολαμίνης (ethanolamine) με έναν εστερικό δεσμό (ένα “ανεστραμμένο” ΑΕΑ), που ονομάζεται βιροδαμίνη (virodhamine) (Πίνακας 1)[36], έχουν απομονωθεί στον εγκέφαλο. Επιπλέον, η Ν-αραχιδονοϋλδοπαμίνη (N-arachidonoyldopamine, NADA), η οποία είναι πρωτίστως ένας αγωνιστής του TRPV1, έχει κάποια δράση και στον CB1 (Πίνακας 1)[86]. Αυτές οι ενώσεις έχουν λάβει λιγότερη προσοχή από τα δύο κύρια eCBs (AEA και 2-AG), ίσως λόγω της δυσκολίας για πολλούς ερευνητές να τις απομονώσουν από βιολογικούς ιστούς[72,87].
Εν πάση περιπτώσει, έχει αναφερθεί ότι ο νολαδινικός αιθέρας δεσμεύεται στους υποδοχείς CB1 και πολύ ασθενώς στους υποδοχείς CB2[35], εκτός του ότι επηρεάζει την πρόσληψη ΑΕΑ[88]. Επιπλέον, η βιροδαμίνη έχει αποδειχθεί ότι συμπεριφέρεται in vitro ως πλήρης αγωνιστής του υποδοχέα CB2 και ως μερικός αγωνιστής του CB1. Αντίθετα, in vivo είναι ανταγωνιστής στον CB1, και επίσης ένας ασθενής αναστολέας της πρόσληψης του AEA[36].
Όπως το AEA, ο νολαδινικός αιθέρας και η βιροδαμίνη αλληλεπιδρούν, αν και με διαφορετική συγγένεια, με τον PPARa και τον ορφανό υποδοχέα GPR55[9,37,87-91], υποδηλώνοντας και πάλι ότι οι μη CBRs μπορούν να είναι κοινοί στόχοι για πολλά παράγωγα λιπαρών οξέων.
Το τελευταίο παράγωγο του AA που έχει προστεθεί στην οικογένεια των eCBs είναι μέχρι στιγμής η NADA[86], η οποία μοιράζεται με το AEA, και με την ανάλογή της N-oleoyldopamine (N-oleoyldopamine)[33], την ικανότητα να ενεργοποιεί τον TRPV1. Πράγματι, η NADA έχει βρεθεί σε περιοχές του εγκεφάλου βοοειδών με αυξημένη πυκνότητα διαύλων TRPV1 και θεωρείται πραγματικό “ενδοβανιλλοειδές” (endovanilloid)[92]. Επιπλέον, το AEA και η NADA φαίνεται να μοιράζονται επίσης τον PPARγ ως στόχο[34]. Η NADA έχει βρεθεί σε περιοχές του εγκεφάλου με τις υψηλότερες ποσότητες ντοπαμίνης, επομένως προτάθηκε ότι είναι το προϊόν συμπύκνωσης αυτής της κατεχολαμίνης με ΑΑ[86,93]. Αντίθετα, η αδρανοποίηση της πιθανότατα περνάει μέσω μιας πολύ αργής υδρόλυσης του αμιδικού δεσμού ή μέσω της μεθυλίωσης του τμήματος κατεχολαμίνης από την κατεχολ-Ο-μεθυλοτρανσφεράση, με το σχηματισμό ενός λιγότερο ισχυρού παραγώγου 3-Ο-μεθυλίου[86].
Εκτός από το AEA, σχηματίζονται και άλλα λιγότερο γνωστά ω-6 (n-6) ακόρεστα NAEs, ικανά να αλληλεπιδρούν με CBRs και προικισμένα με τρεις ή τέσσερις διπλούς δεσμούς, προφανώς ακόμη και σε υψηλότερες ποσότητες από το AEA. Μεταξύ αυτών, η Ν-διομο-γ-λινολενολαιθανολαμίνη (N-dihomo-γ-linolenoylethanolamine) έχει απομονωθεί από διαφορετικούς ιστούς[94,95], καθώς και από βιολογικά υγρά[40], όπου δρα ως ασθενής αγωνιστής των CBRs, αλλά με ελάχιστα κατανοητό (αν υπάρχει) φυσιολογική σημασία.
2.1.3. n-3-Ενδοκανναβινοειδή
Από τη δεκαετία του ‘30 ανατέθηκαν ουσιαστικοί ρόλοι στα n-3 πολυακόρεστα λιπαρά οξέα (n-3 polyunsaturated fatty acids, PUFAs), επειδή η έλλειψή τους στη δίαιτα οδήγησε σε άγνωστες ακόμη μορφές ασθενειών ανεπάρκειας εκείνη την εποχή[96]. Υπάρχει πολλή βιβλιογραφία που κάνει λόγο για τις διάφορες ευεργετικές επιδράσεις των PUFAs, όπως προστατευτικές επιδράσεις έναντι καρδιαγγειακών παθήσεων, φλεγμονών και καρκίνου[97,98], αν και υπάρχουν τώρα αρκετά άρθρα που αμφισβητούν τις ευεργετικές επιδράσεις αυτών των λιπαρών οξέων[99].
Είναι ενδιαφέρον ότι μεταξύ των μορίων που είναι ικανά να ενεργοποιούν τους CBRs, ανιχνεύθηκαν μεταβολίτες που προέρχονται από PUFAs. Συγκεκριμένα, βρέθηκαν δύο παράγωγα εικοσιδυαεξανοϊκού οξέος (docosahexaenoic acid, DHA, C22:6) και εικοσαπεντανοϊκού οξέος (eicosapentaenoic acid, EPA, C20:5) και ονομάστηκαν DHEA και EPEA αντίστοιχα (Πίνακας 1)[39]. Ακόμη και αυτά τα n-3 NAEs έδειξαν την ίδια ασυδοσία των αντίστοιχων αναλόγων n-6 και πράγματι εκτός από τη σύνδεση με τους υποδοχείς CB είναι επίσης σε θέση να ενεργοποιήσουν τον PPARγ[41].
Επιπλέον, τα n-3 PUFAs και τα φυσικά τους παράγωγα, οι ρεσολβίνες (resolvins), μπορούν να ρυθμίσουν τη δραστηριότητα του TRPV1[100-102]. Σύμφωνα με αυτό, το βιοδραστικό παράγωγο του DHA, η ρεσολβίνη D2, αναστέλλει τα ρεύματα TRPV1 στους νευρώνες των γαγγλίων της ραχιαίας ρίζας, αν και ο υποκείμενος μηχανισμός δεν φαίνεται να είναι άμεσος, αλλά μάλλον μεσολαβείται από έναν άγνωστο GPCR (G protein-coupled receptor / υποδοχέας συζευγμένος με πρωτεΐνη G)[101]. Η ικανότητα των ρεσολβινών να μειώνουν τη φλεγμονή υπό φυσιολογικές συνθήκες[103] καθιστά αυτά τα μόρια πολύ ελκυστικά ως πιθανά αντιφλεγμονώδη/αναλγητικά φάρμακα.
Συνολικά, η σηματοδότηση ενδοκανναβινοειδών φαίνεται μάλλον περίπλοκη και φαίνεται να επηρεάζεται σαφώς από τη διατροφή (με ιδιαίτερη αναφορά στην αναλογία n-3/n-6). Για παράδειγμα, το DHEA μπορεί να βρεθεί σε βασικές συνθήκες, ενώ το EPEA ανιχνεύεται στα ίδια κύτταρα μόνο όταν παρέχεται με κατάλληλη δίαιτα[42,57]. Αυτά τα n-3 eCBs έχουν δείξει αντιφλεγμονώδεις ιδιότητες σε μακροφάγα[43] και λιποκύτταρα[3] και μπορούν να αναστείλουν την κυτταρική ανάπτυξη στον καρκίνο του μαστού πυροδοτώντας την αυτοφαγία μέσω του PPARγ[41].
Είναι αξιοσημείωτο ότι η από του στόματος χορήγηση DHEA έχει αποδειχθεί ότι έχει ευεργετικά αποτελέσματα σε ασθενείς που ανταποκρίθηκαν ανεπαρκώς στις θεραπείες εξωσωματικής γονιμοποίησης[45].
2.1.4. Ενώσεις που μοιάζουν με ενδοκανναβινοειδή
Το AEA ανήκει σε μια κατηγορία φυσικών μορίων (NAEs) γνωστών εδώ και πολύ καιρό. Ένα από τα μέλη της, η Ν-παλμιτοϋλαιθανολαμίνη (N-palmitoylethanolamine, PEA), αναφέρθηκε για πρώτη φορά πριν από σχεδόν 50 χρόνια σε ανθρώπους, ωστόσο η φυσιολογική της σχέση παραμένει υπό συζήτηση όταν ο μηχανισμός δεν είναι μέσω CBRs[46].
Η PEA και άλλα NAEs μοιράζονται με τα αληθινά eCBs πολλούς αποικοδομητικούς μηχανισμούς και ενισχύουν την επίδραση των eCBs στους στόχους των υποδοχέων τους αναστέλλοντας ανταγωνιστικά την υδρόλυση τους ή ρυθμίζοντας αλλοστερικά τη δέσμευσή τους στον υποδοχέα: την λεγόμενη “entourage effect” (συνδυαστική επίδραση)[47,48]. Σε αυτή τη βάση, αυτές οι ουσίες είναι επίσης γνωστές ως ενώσεις που μοιάζουν με eCBs (Πίνακας 1).
Μεταξύ των πιο μελετημένων ενώσεων που μοιάζουν με eCBs, ο αντιφλεγμονώδης παράγοντας PEA και η κατασταλτική της όρεξης Ν-ελαιολαιθανολαμίνη (N-oleoylethanolamine, OEA) μπορούν να καταγραφούν (Πίνακας 1)[46]. Η βιολογική τους δραστηριότητα συχνά εμπλέκει την ενεργοποίηση των PPARα και TRPV1[47-51], αν και ορισμένες από τις δράσεις τους αποτρέπονται από ανταγωνιστές CB1[104,105]. Μεταξύ των ενώσεων που μοιάζουν με eCBs, η OEA δείχνει την υψηλότερη συγγένεια για τον PPARa[106] και σταθερά ορισμένες από τις βιολογικές του επιδράσεις απουσιάζουν σε ποντίκια με έλλειψη PPARa[107]. Ωστόσο, οι αντιερεθιστικές ιδιότητες της ΟΕΑ ασκούνται επίσης μέσω ενός μηχανισμού ανεξάρτητου από PPARα[108].
Η OEA, καθώς και η PEA και η 2-ελαιοϋλογλυκερόλη (2-oleoylglycerol, 2-OG) (Πίνακας 1), μπορούν επίσης να ενεργοποιήσουν την GPR119, μια GPCR που εκφράζεται κυρίως στο πάγκρεας ανθρώπου και αρουραίου[53], υποδηλώνοντας ότι οι επιδράσεις της ΟΕΑ στην πρόσληψη τροφής μπορεί να προκληθούν, τουλάχιστον εν μέρει, μέσω GPR119[53,109,110]. Αντίθετα, οι Lan et al. ανέφεραν ότι η υποφαγική επίδραση της ΟΕΑ διατηρήθηκε σε ποντίκια Gpr119(-/-)[111]. Δεν αποτελεί έκπληξη το γεγονός ότι υπάρχουν επίσης ενδείξεις ότι η OEA (όπως και η PEA) μπορεί να εμπλέξει, αν και σε υψηλές συγκεντρώσεις, πρόσθετους υποδοχείς όπως ο GPR55[52].
Ένα άλλο κορεσμένο ΝΑΕ, η Ν-στεαροϋλαιθανολαμίνη (N-stearoylethanolamine, SEA), αναφέρθηκε ότι δρα ως ελεγκτής κυτταρικής ανάπτυξης και αντιφλεγμονώδης / ανοσοτροποποιητικός παράγοντας, μέσω ακόμη άγνωστων στόχων[46,112,113]. Η SEA παρουσιάζει επίσης ανορεξικές επιδράσεις που είναι ανεξάρτητες από τον PPAR[114] και, μαζί με την PEA, διαδραματίζει έναν αντιλοχιστικό ρόλο στους ανθρώπους[114].
Όπως αναφέρθηκε παραπάνω, επίσης τα ενδογενή επίπεδα αυτών των ενώσεων που μοιάζουν με eCBs (PEA, OEA και SEA) επηρεάζονται από διαφορετικά διατροφικά σχήματα, με διαφορετικά αποτελέσματα στον εγκέφαλο σε σύγκριση με τους περιφερικούς ιστούς[56,82].
Η πρόσφατη πρόοδος των αναλυτικών τεχνικών επέτρεψε την ανίχνευση μιας μεγάλης ποικιλίας ενώσεων που περιέχουν αλυσίδες λιπαρών οξέων συζευγμένες με διαφορετικές πολικές κεφαλές[87,115,116]. Μέσα σε αυτά τα νέα λιπίδια, η Ν-αραχιδονοϋλγλυκίνη (N-arachidonoylglycine, NArGly) και η Ν-αραχιδονοϋλσερίνη (N-arachidonoylserine, NArS) (Σχήμα 2) ως αραχιδονοϋλ-αμινοξέα (arachidonoyl-amino acids) μπορούν να καταγραφούν[53,109-120].
Η NAGly, που διαφέρει από το AEA μόνο για την οξείδωση του άνθρακα β, δρα ως πρόσδεμα υψηλής συγγένειας για τον GPR18[121-123] και ως μερικός αγωνιστής των υποδοχέων Gq/11.coupled GPR92[124]. Η NAGly αποδείχθηκε αρχικά ότι είναι ένας ισχυρός in vitro αναστολέας FAAH[125] και αργότερα αποδείχθηκε ότι εμφανίζεται φυσικά in vivo, ότι μιμείται το φαρμακολογικό προφίλ της μη φυσιολογικής κανναβιδιόλης[119] και ότι ασκεί έμμεση νευροπροστατευτική δράση μέσω των CB2 και TRPV1, αλλά όχι στους υποδοχείς CB1 ή GPR55 [126].
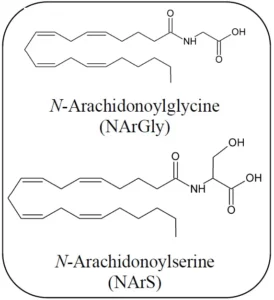
Εικόνα 2. Χημικές δομές ορισμένων μορίων που μοιάζουν με ενδοκανναβινοειδή
Αν και απαιτούνται περαιτέρω έρευνες για να αποσαφηνιστεί η πραγματική φυσιολογική συνάφεια των ενώσεων που μοιάζουν με eCBs και των αραχιδονοϋλ-αμινοξέων, είναι σημαντικό να επισημανθεί ότι η PEA, λόγω της έλλειψης δυσμενών παρενεργειών στους κεντρικούς υποδοχείς CB1, έχει δυνατότητα για την ανάπτυξη καινοτόμων φαρμάκων, και κυκλοφορεί επί του παρόντος για τη θεραπεία του νευροπαθητικού και του πυελικού πόνου[127].
2.2. Μεταβολισμός Ενδοκανναβινοειδών και Συναφών Ενώσεων
Όπως και πολλά άλλα βιοενεργά μόρια, η δραστηριότητα των eCBs ελέγχεται από τα ενδογενή τους επίπεδα και επομένως από την ισορροπία μεταξύ βιοσυνθετικών και αποικοδομητικών μηχανισμών. Με βάση τις αρχικές παρατηρήσεις που πραγματοποιήθηκαν στο AEA[128], υποτέθηκε ότι τα eCBs δεν αποθηκεύονται σε προσχηματισμένα κυστίδια, αλλά μάλλον συντίθενται και απελευθερώνονται “κατ’ απαίτηση”, δηλαδή όταν και όπου χρειάζεται. Ωστόσο, πιο πρόσφατες απόψεις επέβαλαν μια επανεξέταση αυτού του “δόγματος”, επειδή το ΑΕΑ μπορεί να αποθηκευτεί σε σταγονίδια λιπιδίων (λιποσώματα) και δεσμεύεται σε ενδοκυτταρικούς μεταφορείς[2,129]. Μια σύγχρονη άποψη των μεταβολικών οδών των AEA και 2-AG (και σχετικών ουσιών) παρουσιάζεται στις επόμενες ενότητες.
2.2.1. Βιοσύνθεση ΑΕΑ και ομοειδών
Ο συνεχώς αυξανόμενος αριθμός ενζύμων που εμπλέκονται στη βιοσύνθεση του AEA (και των σχετικών NAEs) υποδηλώνει ότι ο ενδογενής τόνος αυτού του eCB υπόκειται σε ένα εξαιρετικά περίπλοκο και εξαιρετικά ρυθμιζόμενο δίκτυο αντιδράσεων (Σχήμα 1).
Η κύρια οδός για τη βιοσύνθεση των NAEs αποτελείται από δύο ενζυματικές αντιδράσεις. Η πρώτη είναι μια μεταφορά λιπαρής ακυλικής αλυσίδας από φωσφολιπίδια μεμβράνης σε φωσφατιδυλαιθανολαμίνη (phosphatidylethanolamine), με αποτέλεσμα τον σχηματισμό Ν-ακυλοφωσφατιδυλαιθανολαμίνης (N-acylphosphatidylethanolamine, NAPE), από μια ακόμη μη αναγνωρισμένη εξαρτώμενη από Ca2+ Ν-ακυλοτρανσφεράση (N-acyltransferase, NAT)[11], ή αντίστοιχη ανεξάρτητη από Ca2+ (iNAT)[12-14]. Όντας τα παλμιτοϋλ και ελαιολικά οξέα που ενσωματώνονται κατά προτίμηση στη θέση sn-1, η ΝΑΤ παράγει κατά προτίμηση PEA και OEA παρά ΑΕΑ[11]. Αντίθετα, η iNAT αφαιρεί μια ομάδα λιπαρού ακυλίου τόσο από τη θέση sn-1 όσο και από τη θέση sn-2 (όπου το ΑΑ είναι πιο άφθονο) της φωσφατιδυλοχολίνης (phosphatidylcholine, PC), δηλαδή του δότη ακυλίου[13,14].
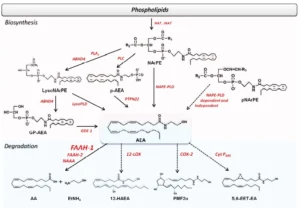
Σχήμα1. Οι εναλλακτικές διαδρομές βιοσύνθεσης και αποκομιδής του AEA και των ομοειδών του
Σημειώσεις: NAAA, αμιδάση οξέος υδρολυτικής Ν-ακυλαιθανολαμίνης (N-acylethanolamine-hydrolyzing acid amidase), NArPE, Ν-αραχιδονοϋλφωσφατιδυλαιθανολαμίνη (N-arachidonoylphosphatidylethanolamine), pNArPE, πλασμαγόνο Ν-αραχιδονοϋλεθανολαμίνης (N-arachidonoylethanolamine plasmalogen), ABHD4, α/β-υδρολάση 4 (α/β-hydrolase 4), NAPE-PLD, Ν-ακυλο-φωσφατιδυλαιθανολαμίνες-υδρολύουσα φωσφολιπάση D (N-acyl-phosphatidylethanolamines-hydrolyzing phospholipase D), ΑΑ, αραχιδονικό οξύ (arachidonic acid), COX-2, κυκλοοξυγενάση-2 (cyclooxygenase-2), Cyt P450, κυτόχρωμα P450 (cytochrome P450), EET-EA, εποξυεικοσατριενοϋλ αιθανολαμίδια (epoxyeicosatrienoyl ethanolamides), EtNH2, αιθανολαμίνη (ethanolamine), FAAH, υδρολάση αμιδίου λιπαρού οξέος (fatty acid amide hydrolase), GP-AEA, γλυκεροφωσφο-ΑΕΑ (glycerophospho-AEA), GDE1, γλυκεροφωσφοδιεστερική φωσφοδιεστεράση 1 (glycerophosphodiester phosphodiesterase 1), 12-HAEA, 12-υδροξυανανταμίδιο (12-hydroxyanandamide), lyso-NArPE, λυσο-Ν-αραχιδονοϋλφωσφατιδυλαιθανολαμίνη (lyso-N-arachidonoylphosphatidylethanolamine), 12-LOX, 12-λιποξυγενάση (12-lipoxygenase), pAEA, φωσφο-ΑΕΑ (phospho-AEA), NAT, Ν-ακυλο-τρανσφεράση (N-acyl-transferase), iNAT, Ca2+-ανεξάρτητη Ν-ακυλοτρανσφεράση (Ca2+-independent N-acyltransferase), PMF2α, προσταμίδια F2α (prostamides F2α), PLA2, φωσφολιπάση Α2 (phospholipase A2), PLC, φωσφολιπάση C (phospholipase C), lyso-PLD, λυσο-φωσφολιπάση D (lyso-phospholipase D), PTPN22, πρωτεϊνική φωσφατάση τυροσίνης, μη υποδοχέα τύπου 22 (protein tyrosine phosphatase, non-receptor type 22)
Επιπλέον, η NAT και η iNAT έχουν διαφορετικούς κυτταρικούς και ιστικούς εντοπισμούς, για παράδειγμα η τελευταία εκφράζεται ελάχιστα στον εγκέφαλο[11] υποδηλώνοντας έναν ξεχωριστό ρόλο στον έλεγχο των επιπέδων NAEs.
Στο δεύτερο στάδιο καταλύεται από μια φωσφολιπάση τύπου D (NAPE-PLD) (Σχήμα 1), η οποία διαφέρει από τα κλασικά PLD. Πράγματι, η NAPE-PLD, η οποία διατηρείται σε μεγάλο βαθμό από τα τρωκτικά στον άνθρωπο, ανήκει στην οικογένεια των ενζύμων μεταλλολακταμάσης και in vitro καταλύει τον σχηματισμό AEA από την πρόδρομη C20:4-NAPE του, καθώς και από άλλα NAPEs[15].
Τα συσσωρευμένα στοιχεία υποδεικνύουν, ωστόσο, την ύπαρξη πρόσθετων οδών για το σχηματισμό ΑΕΑ από την NArPE[11,130]. Πράγματι, μέσω της χρήσης νοκ-άουτ ποντικών έχουν εντοπιστεί και χαρακτηριστεί αρκετά ένζυμα και μεταβολίτες που εμπλέκονται στην ανεξάρτητη από την NAPE-PLD βιοσύνθεση του AEA[16-18]. Αυτές οι εναλλακτικές οδοί του ΑΕΑ φαίνονται στο Σχήμα 1. Πιο πρόσφατα, μια ενδιαφέρουσα εργασία ανέφερε μια νέα οδό για το σχηματισμό NAE από το πλασμαγόνο Ν-ακυλαιθανολαμίνης /N-acylethanolamine plasmalogen (1-αλκενυλ-2-ακυλ-γλυκερο-3-φωσφο(Ν-ακυλ)αιθανολαμίνη / 1-alkenyl-2-acyl-glycero-3-phospho(N-acyl)ethanolamine, pNAPE), μια από τις κύριες κατηγορίες γλυκεροφωσφολιπιδίων (glycerophospholipids) στον εγκέφαλο ποντικού[131]. Επίσης αυτή η διαδρομή απεικονίζεται στο Σχήμα 1.
2.2.2. Βιοσύνθεση 2-AG και ομοειδών
Η πιο γνωστή βιοσυνθετική οδός για την 2-AG απαιτεί τη συνδυασμένη δράση δύο μεμβρανικών ενζύμων: της φωσφολιπάσης C (phospholipase C, PLC) και της διακυλογλυκερολικής λιπάσης (diacylglycerol lipase, DAGL), όπως φαίνεται στο Σχήμα 2. Συγκεκριμένα, μεταξύ διαφόρων ισομορφών PLC[132], β1 και β4, έχουν συνδεθεί με το σχηματισμό 2-AG που προκαλείται από GPCRs στους νευρώνες του ιππόκαμπου και στα κύτταρα Purkinje της παρεγκεφαλίδας, αντίστοιχα[27,28]. Επιπλέον, δεδομένου ότι η PLC αναγνωρίζει διαφορετικά φωσφολιπίδια, η κατανομή της οποίας ποικίλλει μεταξύ των ιστών, ο σχηματισμός της DAG και στη συνέχεια της 2-AG, από μια τέτοια λιπάση είναι ειδικός για τον ιστό[133,134]. Εναλλακτικές οδοί βιοσύνθεσης 2-AG φαίνονται στο Σχήμα 2.
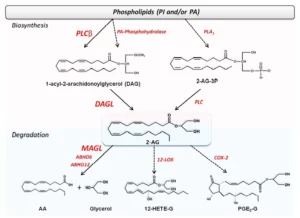
Σχήμα 2. Οι εναλλακτικές βιοσυνθετικές και αποικοδομητικές οδοί της 2-AG και των ομοειδών
Σημειώσεις: AA, αραχιδονικό οξύ (arachidonic acid), 2-AG-3P, 3-φωσφορική 2-αραχιδονοϋλογλυκερόλη (2-arachidonoylglycerol-3-phosphate), COX-2, κυκλοοξυγενάση-2 (cyclooxygenase-2), DAG, διακυλογλυκερόλη (diacylglycerol), DAGL, λιπάση διακυλογλυκερόλης (diacylglycerol lipase), 12-HETE-G, 12-υδροξυαραχιδονοϋλ-γλυκερόλη (12-hydroxyarachidonoyl-glycerol), ABHD6/12, περιοχή α/β-υδρολάσης 6/12 (α/β-hydrolase domain 6/12), 12-LOX, 12-λιποξυγενάση (12-lipoxygenase), MAGL, μονοακυλογλυκερολική λιπάση (monoacylglycerol lipase), PLC, φωσφολιπάση C (phospholipase C), PLCβ, φωσφολιπάση Cβ (phospholipase Cβ), PGE2-G, προσταγλανδική γλυκερόλη E2-G (prostaglandinglycerol E2-G)
Η DAGL, το δεύτερο ένζυμο που εμπλέκεται στο σχηματισμό της 2-AG, υπάρχει σε δύο μορφές, α και β[29]. Έτσι, η υψηλή περιεκτικότητα σε AA στην τελευταία θέση μπορεί να εξηγήσει την κυρίαρχη παραγωγή 2-AG έναντι άλλων MAGs[29]. Αξιοσημείωτα, δύο ανεξάρτητες μελέτες έχουν προτείνει ότι μόνο η 2-AG που παράγεται από την DAGLα είναι υπεύθυνη για την ανάδρομη καταστολή μέσω του CB1 στις κεντρικές συνάψεις στον εγκέφαλο[135,136]. Επιπλέον, έχουν αναφερθεί μειωμένα επίπεδα ΑΕΑ στην παρεγκεφαλίδα και τον ιππόκαμπο των daglα-/- ποντικών[136], υποστηρίζοντας μια αμοιβαία αλληλεπίδραση μεταξύ AEA και 2-AG, πιθανώς εμπλέκοντας και τα κανάλια TRPV1 όπως τεκμηριώνεται στο ραβδωτό σώμα[137]. Επιπρόσθετα, αναφέρθηκε μια ρύθμιση της DAGLα από την εξαρτώμενη από ασβέστιο / καλμοδουλίνη πρωτεϊνική κινάση II[138], και μια τέτοια πρωτεϊνική κινάση είχε προηγουμένως αποδειχθεί ότι ρυθμίζει επίσης τον υποδοχέα TRPV1[139]. Οι εναλλακτικές οδοί της βιοσύνθεσης 2-AG φαίνονται στο Σχήμα 2.
2.2.3. Αποικοδόμηση ενδοκανναβινοειδών και συγγενών
Πρόσληψη ενδοκανναβινοειδών και ομοειδών
Στην αρχή, ο μηχανισμός που εμπλέκεται στη διαμεμβρανική μεταφορά eCBs που έλαβε τη μεγαλύτερη προσοχή ήταν η διευκολυνόμενη μεταφορά[140-142], ωστόσο δεν έχει κλωνοποιηθεί ακόμη καμία πρωτεΐνη μεταφορέας. Στη συνέχεια, έχουν προταθεί πρόσθετοι μηχανισμοί, οι οποίοι αναθεωρήθηκαν πρόσφατα[143]: (i) παθητική διάχυση που περιορίζεται από FAAH[144,145], με ενδοκυτταρική δέσμευση[146] ή με σχηματισμό συμπλόκων ΑΕΑ-χοληστερόλης[147], (ii) ενδοκυττάρωση εξαρτώμενη από τα κοιλώματα[143].
Ένα άλλο καυτό θέμα είναι η κατανόηση του τρόπου με τον οποίο τα eCBs μπορούν να φτάσουν στις ξεχωριστές θέσεις δράσης τους μέσα στο κύτταρο (πχ. μεμβρανικοί ή πυρηνικοί υποδοχείς ή μεταβολικά ένζυμα) τη σωστή στιγμή, προκειμένου να πυροδοτήσουν την κατάλληλη απόκριση σε ένα ερέθισμα. Σε αυτό το πλαίσιο, η ύπαρξη ενδοκυτταρικών οργανιδίων αποθήκευσης (σταγονίδια λιπιδίων ή λιποσώματα)[146] και συστατικών ενδοκυτταρικών μεταφορέων (ΑΕΑ ενδοκυτταρικοί μεταφορείς, ΑΙΤ) έχουν αναφερθεί για ΑΕΑ. Μεταξύ των συστατικών ΑΙΤ είναι η πρωτεΐνη θερμικού σοκ 70 (Hsp70) και η λευκωματίνη[148], στις οποίες έχουν προστεθεί οι πρωτεΐνες 5 και 7 που δεσμεύουν τα λιπαρά οξέα (FABP5 και FABP7) ως εξωγενείς οντότητες[149]. Είναι ενδιαφέρον ότι ένας λειτουργικός ρόλος για τα FABPs στη σηματοδότηση ενδοκανναβινοειδών έχει τεκμηριωθεί πρόσφατα[150], παρέχοντας μια απόδειξη της ιδέας ότι πράγματι οι AITs μπορούν να οδηγήσουν τη σηματοδότηση ενδοκανναβινοειδών μέσω μιας ξεχωριστής οδού (πχ. αυτής που διενεργείται μέσω PPARα από OEA[150]).
Επιπλέον, έχει προταθεί ότι ορισμένες NAEs συσσωρεύονται σε κύτταρα μέσω ενός γενικού μηχανισμού που μοιράζεται με το AEA[151], ο οποίος μπορεί να λειτουργεί σε αμφίδρομη λειτουργία[141,151,152]. Είναι ενδιαφέρον ότι η PEA έχει αποδειχθεί ότι παρεμβαίνει στη διαμεμβρανική μεταφορά του AEA με τρόπο που εξαρτάται από τον κυτταρικό τύπο[153] και αρκετά ανάλογα της OEA αποδείχθηκαν πιο ισχυρά από τις NAEs που περιέχουν AA στην παρεμπόδιση της πρόσληψης AEA[128]. Λιγότερες πληροφορίες είναι διαθέσιμες για την κυτταρική συσσώρευση άλλων αναλόγων eCBs, ωστόσο τουλάχιστον ένας διπλός δεσμός στην ακυλική αλυσίδα φαίνεται απαραίτητος για να πραγματοποιηθεί η διαμεμβρανική μεταφορά[143,154].
Μέχρι στιγμής, μόνο λίγες μελέτες έχουν ασχοληθεί με τη μεταφορά της 2-AG, αλλά προφανώς αυτό το eCB χρησιμοποιεί τον ίδιο μηχανισμό που χρησιμοποιεί το AEA[151,155,156]. Επιπλέον, η 2-AG μπορεί να εστεροποιηθεί απευθείας σε (φωσφο)γλυκερίδια, μέσω φωσφορυλίωσης ή/και ακυλίωσης των ελεύθερων υδροξυλομάδων του[156].
Συμπερασματικά, η ακόλουθη παραπομπή φαίνεται αρκετά διδακτική: “Η μετατόπιση κατά μήκος της πλασματικής μεμβράνης επιτυγχάνεται με μια συναυλία συνυπάρχουσων μηχανισμών. Αυτά τα λιπίδια μπορούν να διαχέονται παθητικά, αλλά η μεταφορά μπορεί επίσης να επιταχυνθεί από ορισμένες μεμβρανικές πρωτεΐνες καθώς και από λιπιδικές σχεδίες”[157].
Υδρόλυση ΑΕΑ και ομοειδών
Πιθανώς το κύριο καταβολικό ένζυμο που είναι υπεύθυνο για τον τερματισμό του σήματος του ΑΕΑ είναι η υδρολάση αμιδίου λιπαρών οξέων (FAAH)[19]. Αυτό το ένζυμο κλωνοποιήθηκε από τους Cravatt et. al το 1996[35,54] και αποδείχθηκε ότι διασπά το AEA, καθώς και άλλες NAEs και επίσης την 2-AG (Πίνακας 1 και Σχήμα 1).
Η FAAH είναι μια ενδοκυτταρική μεμβράνη υδρολάση σερίνης με S241-S217-K142 ως καταλυτική τριάδα[158,159]. Αυτή η υδρολάση είναι ευρέως παρούσα στον εγκέφαλο, όπου δείχνει μια υποκυτταρική κατανομή που επικαλύπτει αυτή των υποδοχέων CB1 και ουσιαστικά σε όλα τα περιφερειακά όργανα, αλλά με διαφορετική κατανομή μεταξύ τρωκτικών και ανθρώπων[158].
Λίγα χρόνια μετά τον χαρακτηρισμό της FAAH (τώρα ονομάζεται FAAH-1), αναφέρθηκαν δύο άλλες υδρολάσεις ικανές να υδρολύσουν ΑΕΑ και πρόσφατα έχουν ανασκοπηθεί[55]: μια ισομορφή της FAAH που είναι γνωστή ως FAAH-2[20], και μια λυσοσωμική κυστεϊνική υδρολάση που ονομάζεται αμιδάση οξέος υδρολυτικής Ν-ακυλαιθανολαμίνης (N-acylethanolamine-hydrolyzing acid amidase, NAAA) (Σχήμα 1)[21]. Συγκεκριμένα, η FAAH-2 έχει περιορισμένη κατανομή ειδών στα θηλαστικά και φαίνεται να συνδέεται μόνιμα με λιποσώματα[160], όπου μπορεί να αποθηκευτεί το AEA και εντοπίστηκε επίσης σε σταγονίδια λιπιδίων[146]. Οι FAAH-1 και FAAH-2 μοιράζονται περιορισμένη ταυτότητα αλληλουχίας (~20%), ενώ δεν υπάρχει ομολογία μεταξύ τους και της NAAA[21], ενός ενζύμου που δείχνει προτίμηση υποστρώματος έναντι άλλων κορεσμένων ή μονοακόρεστων NAEs[55]. Είναι ενδιαφέρον ότι αρκετοί ισχυροί αναστολείς NAAA έχουν αποδειχθεί ότι ενισχύουν την επίδραση της PEA στο PPARa[161,162]. Αντίθετα, ο πρωταρχικός ρόλος της FAAH-1 φαίνεται να ελέγχει τα in vivo επίπεδα της ΑΕΑ και άλλων πολυακόρεστων ΝΑΕs, όπως επιβεβαιώνεται από ποντίκια FAAH1-/-[163].
Υδρόλυση 2-AG και ομοειδών
Στερεά στοιχεία δείχνουν ότι η μονοακυλογλυκερολική λιπάση (MAGL) είναι η κύρια υπεύθυνη για την αποικοδόμηση της 2-AG in vivo (Πίνακας 1 και Σχήμα 2). Πράγματι, η υδρόλυση και η περιεκτικότητα σε 2-AG παραμένουν αμετάβλητα στα ποντίκια FAAH1-/-, ενώ αυξήθηκαν σημαντικά στα ποντίκια MAGL-/-[30] και συσχετίστηκαν με βαθιές αλλαγές στη σηματοδότηση 2-AG[164]. Επιπλέον, ο διαφορετικός εντοπισμός των MAGL και FAAH-1 στον εγκέφαλο[30,70] υποστηρίζει την υπόθεση των διακριτών ρόλων για αυτά τα δύο eCBs[165].
Είναι ενδιαφέρον ότι η MAGL εμφανίζει υψηλότερη ειδικότητα από την FAAH-1, επειδή η θεραπεία με τον ισχυρό και εκλεκτικό αναστολέα JZL-184 αυξάνει μόνο τα επίπεδα της 2-AG, χωρίς να επηρεάζει εκείνα οποιαδήποτε άλλης MAG (πχ. μονοπαλμιτοϋλογλυκερόλη / monopalmitoylglycerol και μονοελαιοϋλογλυκερόλη / monooleoylglycerol)[166]. Η MAGL είναι μια υδρολάση σερίνης με μια καταλυτική τριάδα (S122-D239-H269) που διατηρείται σε μεγάλο βαθμό μεταξύ διαφορετικών ειδών[166-170]. Είναι ενδιαφέρον ότι διαφορετικές παρατηρήσεις υποστηρίζουν έναν ρόλο για την MAGL ως πάροχο ελεύθερων λιπαρών οξέων, που υποστηρίζει τον καρκίνο[171-173].
Δύο επιπλέον υδρολάσες σερίνης, ο τομέας 6 α/β-υδρολάσης (ABHD6, με υποτιθέμενη καταλυτική τριάδα S148-D278-H306) και 12 (ABHD12, με υποτιθέμενη καταλυτική τριάδα S246-D333-H372), εμπλέκονται στην υδρόλυση 2-AG (Πίνακας 1 και Σχήμα 2)[31,32]. Αξίζει να σημειωθεί ότι οι MAGLs, ABHD6 και ABHD12 δείχνουν μια ξεχωριστή κατανομή εντός του ΚΝΣ[32,174], που υποδηλώνει διαφορετική φυσιολογική λειτουργία αυτών των τριών ενζύμων στη ρύθμιση της σηματοδότησης 2-AG[32,175]. Προς υποστήριξη αυτής της άποψης, έχουν αναφερθεί πρόσφατα αντιφλεγμονώδη αποτελέσματα της αναστολής της ABHD6 χωρίς τις παρενέργειες που συνήθως συνδέονται με την αναστολή MAGL[176].
Επιπλέον, οι μεταλλάξεις στο γονίδιο abhd12 σχετίζονται με τη νευροεκφυλιστική νόσο που ονομάζεται PHARC (πολυνευροπάθεια, απώλεια ακοής, αταξία, μελαγχρωστική αμφιβληστροειδίτιδα και καταρράκτης)[177]. Θα μπορούσε να υποθέσει ότι αυτή η κληρονομική ασθένεια μπορεί να συνδεθεί με μια δυσλειτουργία του μεταβολισμού 2-AG, αν και μια πρόσφατη μελέτη για την ABHD12-/- ποντίκια φαίνεται να εμπλέκουν το ΕΚΣ σε αυτή την ασθένεια[178].
Οξειδωτικός μεταβολισμός eCBs και ενώσεων που μοιάζουν με eCBs
Εναλλακτικά αντί των υδρολυτικών οδών, τα eCBs είναι επίσης υποστρώματα των ενζύμων που οξυγονώνουν το ΑΑ. Αυτά τα καταβολικά μονοπάτια αντιπροσωπεύουν ένα ενδιαφέρον σημείο τομής μεταξύ ενδοκανναβινοειδών και κλασικών εικοσανοειδών συστημάτων, οδηγώντας στην παραγωγή νέων βιολογικά ενεργών μεταβολιτών[23].
Συγκεκριμένα, το AEA και η 2-AG μεταβολίζονται από τις λιποξυγενάσες (LOXs)[22] και από την κυκλοοξυγενάση-2 (COX-2)[23,24], και επιπλέον το AEA μπορεί να οξυγονωθεί και από το κυτόχρωμα P450 (Πίνακας 1)[25]. Τα κύρια προϊόντα του οξειδωτικού μεταβολισμού των AEA και 2-AG αναφέρονται στα Σχήματα 1, 2 και στο Σχήμα 3.
Αρκετά φαρμακολογικά δεδομένα υποδεικνύουν παράγωγα LOX του AEA (υδροξυανανταμίδια, HAEAs) ως συνδέτες για υποδοχείς CB1, CB2, PPARs και TRPV1[179-181], και μπορούν επίσης να αλληλεπιδράσουν με ορισμένα ένζυμα του συστήματος ΕΚΣ[22,182], όπως καθώς και με τις ιδιότητες των κυτταρικών μεμβρανών[183,184].
Εκτός από το AEA, άλλα παράγωγα λιπαρών οξέων όπως η DHEA, η NArGly και η Ν-αραχιδονοϋλταυρίνη υφίστανται οξυγόνωση καταλυόμενη από LOX[185-187]. Συγκεκριμένα, η 17-υδροξυ-DHEA (Εικόνα 3) εμφανίζεται φυσικά στον εγκέφαλο του ποντικού, όπου φαίνεται να ασκεί προστατευτική λειτουργία[185].
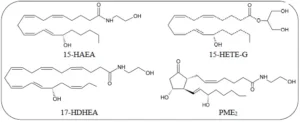
Εικόνα 3. Χημικές δομές των κύριων προϊόντων οξειδωτικού μεταβολισμού των ΑΕΑ και 2-AG
Η COX-2, αλλά όχι η COX-1, μπορεί να οξυγονώσει τα κύρια eCBs παράγοντας έναν αριθμό οξυγονωμένων μορίων[23]. Κατ’ αναλογία με τα προστανοειδή, τα προϊόντα της οξυγόνωσης ΑΑ από COX-2, AEA και 2-AG μπορούν να οξυγονωθούν σε αιθανολαμίδια προσταγλανδίνης (προσταμίδια, PMs) και εστέρες γλυκερίνης προσταγλανδίνης (PGs-G), αντίστοιχα (Σχήματα 1, 2 και Εικόνα 3)[188]. Σε αντίθεση με τα παράγωγα των eCBs που δημιουργούνται από την LOX, οι βιολογικές δραστηριότητες των μεταβολιτών που προέρχονται από COX-2 πιθανώς μεσολαβούνται από διαφορετικούς υποδοχείς σε σύγκριση με αυτούς που δεσμεύουν τα eCBs[23,183,189]. Είναι ενδιαφέρον ότι ορισμένοι ασθενείς αναστολείς της οξυγόνωσης ΑΑ από την COX-2, όπως τα μη στεροειδή αντιφλεγμονώδη φάρμακα (ΜΣΑΦ), είναι ισχυροί αναστολείς της οξυγόνωσης των ενδοκανναβινοειδών από το ίδιο ένζυμο[190,191], υποδηλώνοντας ότι τα ΜΣΑΦ μπορεί να είναι χρήσιμα για την καλύτερη κατανόηση των μακρολογικών ιδιοτήτων των PM in vivo του φαρμάκου. Είναι ενδιαφέρον ότι μια αύξηση της προσταμίδης F2α (PMF2α) βρέθηκε στο νωτιαίο μυελό σε ποντίκια, μετά από πρόκληση φλεγμονής, και βρέθηκε ότι ασκεί προαλγητική δράση, υποστηρίζοντας τη συνάφεια της οξείδωσης ενδοκανναβινοειδών in vivo[192]. Επιπλέον, το ανάλογο PMF2α βιματοπρόστη χρησιμοποιείται επί του παρόντος για τη θεραπεία του γλαυκώματος[193]. Πιο πρόσφατα, ο εστέρας της προσταγλανδίνης D2-γλυκερόλης βρέθηκε να μειώνει την ενεργοποίηση των μακροφάγων και αυτό το αποτέλεσμα εξαρτιόταν από τη δραστηριότητα του ABDH6[176].
Τέλος, το ΑΕΑ μπορεί να μεταβολιστεί από πολλά διαφορετικά ανθρώπινα κυτοχρώματα P450, για να σχηματίσει έναν αριθμό δομικά σχετιζόμενων εποξυεικοσατριενοϊκών αιθανολαμιδίων (EETs-EA)[185]. Συγκεκριμένα, το εποξείδιο AEA στις θέσεις C5-C6 (5,6-EET-EA) (Σχήμα 1) παράγεται από το ανθρώπινο CYP3A4, μια ισομορφή του κυτοχρώματος P450, και δρα ως ισχυρός και εκλεκτικός αγωνιστής των υποδοχέων CB2[194]. Αντίθετα, το ορφανό κυτόχρωμα P450 4X1 βρέθηκε να παράγει 14,15-EET-EA, του οποίου η (παθο)φυσιολογική συνάφεια μένει να διευκρινιστεί[195].
3. Συμπεράσματα
Η απανταχού παρουσία των eCBs και οι πολλαπλές (παθο)φυσιολογικές επιπτώσεις τους επέτρεψαν τον εντοπισμό νέων στόχων για θεραπευτικές μεθόδους επόμενης γενιάς. Ωστόσο, οι πολυάριθμες παρενέργειες σε κεντρικό και περιφερειακό επίπεδο μπορεί να μειώσουν τον ενθουσιασμό προς αυτούς τους νέους στόχους. Πράγματι, πρόσφατα οδήγησαν στην απόσυρση του Acomplia® (rimonabant), ενός ανταγωνιστή / αντίστροφου αγωνιστή των υποδοχέων CB1 που αδειοδοτήθηκε και διατέθηκε στην αγορά ως παράγοντας κατά της παχυσαρκίας[67].
Ωστόσο, τα τελευταία 20 χρόνια φάρμακα που σχετίζονται με τα eCBs έχουν πράγματι κυκλοφορήσει στο εμπόριο, όπως το Cesamet® (nabilone, ένα συνθετικό κανναβινοειδές) και το Marinol® (dronabinol, μια συνθετική εκδοχή της THC), που είναι παρασκευάσματα που χρησιμοποιούνται για τη θεραπεία της ναυτίας και του εμέτου που σχετίζονται με χημειοθεραπεία καρκίνου. Το τελευταίο από αυτά τα φάρμακα συνταγογραφείται επίσης για τη διαχείριση της απώλειας της όρεξης σε άτομα με σύνδρομο επίκτητης ανοσοανεπάρκειας (AIDS). Επιπλέον, το Sativex®, ένα φάρμακο που περιέχει απομονωμένη THC και απομονωμένη κανναβιδιόλη σε αναλογία 1:1, έχει λάβει άδεια για τη συμπτωματική θεραπεία (πόνος, σπαστικότητα και ακράτεια) ασθενών με σκλήρυνση κατά πλάκας σε έναν (διαρκώς αυξανόμενο) αριθμό χωρών (πχ. Ηνωμένο Βασίλειο, Καναδάς, Νέα Ζηλανδία και ΗΠΑ). Επιπλέον, η PEA κυκλοφορεί επί του παρόντος για τη θεραπεία του νευροπαθητικού (Normast®) και του πυελικού (Pelvilen®) πόνου και είναι ένα από τα κύρια συστατικά μιας κρέμας (Physiogel®) που χρησιμοποιείται για φλεγμονώδες ή ερεθισμένο δέρμα ατόμων με ατοπική δερματίτιδα.
Για το σκοπό αυτό, έχουν δοκιμαστεί ρυθμιστές των ενδοκανναβινοειδών μεταβολικών οδών, με την υπόσχεση ότι θα είναι απαλλαγμένοι από ανεπιθύμητες παρενέργειες τυπικές ενώσεων που ενεργοποιούν τους υποδοχείς δέσμευσης eCBs. Αυτές οι μελέτες οδήγησαν σε αντίθετα αποτελέσματα, ο αποκλεισμός FAAH δεν οδήγησε σε απευαισθητοποίηση των υποδοχέων CB1[196], ενώ η χρόνια φαρμακολογική απενεργοποίηση της MAGL προκαλεί αλλοιώσεις στη λειτουργία του υποδοχέα CB1[197]. Συμπερασματικά, η ανάπτυξη φαρμάκων που βασίζονται σε eCBs με περιορισμένη περιοχή στόχο φαίνεται πολλά υποσχόμενη να θεραπεύσει ή να επιβραδύνει διαφορετικές ανθρώπινες παθολογίες.
Ευχαριστίες
Οι συγγραφείς επιθυμούν να ευχαριστήσουν όλους τους συναδέλφους στο Tor Vergata University της Ρώμης, το IRCCS Santa Lucia Foundation της Ρώμης και το Campus Bio-Medico University της Ρώμης. Αυτή η έρευνα υποστηρίχθηκε με χρηματοδότηση από το Italian Ministero dell’Istruzione, dell’Universita e della Ricerca στο MM (grant PRIN 2010-2011) και στο FF (grant PRIN 2012).
Συνεισφορές Συγγραφέων
Οι FF και MB έγραψαν το χειρόγραφο. Οι RF, ET και MF συνέλεξαν δεδομένα από τη βιβλιογραφία και ετοίμασαν πίνακα, σχήματα και σχήματα. Ο ΜΜ σχεδίασε και αναθεώρησε το χειρόγραφο. Όλοι οι συγγραφείς έχουν διαβάσει και εγκρίνει το χειρόγραφο.
Συγκρούσεις συμφερόντων
Οι συγγραφείς δηλώνουν ότι δεν υπάρχει σύγκρουση συμφερόντων.
Βιβλιογραφικές αναφορές
- 1. Pertwee, R.G.; Howlett, A.C.; Abood, M.E.; Alexander, S.P.; Di Marzo, V.; Elphick, M.R.; Greasley, P.J.; Hansen, H.S.; Kunos, G.; Mackie, K.; et al. International Union of Basic and Clinical Pharmacology. LXXIX. Cannabinoid receptors and their ligands: beyond CB1 and CB2. Pharmacol. Rev. 2010, 62, 588–631.
- 2. Maccarrone, M.; Dainese, E.; Oddi, S. Intracellular trafficking of anandamide: new concepts for signaling. Trends Biochem. Sci. 2010, 35, 601–608.
- 3. Piomelli, D. More surprises lying ahead. The endocannabinoids keep us guessing. Neuropharmacology 2014, 76, 228–234.
- 4. Di Marzo, V.; Fontana, A. Anandamide, an endogenous cannabinomimetic eicosanoid: ‘Killing two birds with one stone’. Prostaglandins Leukot. Essent. Fat. Acids 1995, 53, 1–11.
- 5. Devane, W. A.; Hannus, L.; Breuer, A.; Pertwee, R.G.; Stevenson, L.A.; Griffin, G.; Gibson, D.; Mandelbaum, A.; Etinger, A.; Mechoulam, R. Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science 1992, 258, 1946–1949.
- 6. Mechoulam, R.; Ben-Shabat, S.; Hanus, L.; Ligumsky, M.; Kaminski, N.E.; Schatz, A.R.; Gopher, A.; Almog, S.; Martin, B.R.; Compton, D.R.; et al. Identification of an endogenous 2-monoglyceride, present in canine gut, that binds to cannabinoid receptors. Biochem. Pharmacol. 1995, 50, 83–90.
- 7. Sugiura, T.; Kondo, S.; Sukagawa, A.; Nakane, S.; Shinoda, A.; Itoh, K.; Yamashita, A.; Waku, K. Arachidonoylglycerol: A possible endogenous cannabinoid receptor ligand in brain. Biochem. Biophys. Res. Commun. 1995, 215, 89–95.
- 8. Di Marzo, V.; de petrocellis, l. Endocannabinoids as regulators of transient receptor potential (TRP) channels: A further opportunity to develop new endocannabinoid-based therapeutic drugs. Curr. Med. Chem. 2010, 17, 1430–1449.
- 9. Pistis, M.; Melis, M. From surface to nuclear receptors: The endocannabinoid family extends its assets. Curr. Med. Chem. 2010, 17, 1450–1467.
- 10. Gasperi, V.; Dainese, E.; Oddi, S.; Sabatucci, A.; Maccarrone, M. GPR55 and its interaction with membrane lipids: Comparison with other endocannabinoid-binding receptors. Curr. Med. Chem. 2013, 20, 64–78.
- 11. Ueda, N.; Tsuboi, K.; Uyama, T. Metabolism of endocannabinoids and related N-acylethanolamines: Canonical and alternative pathways. FEBS J. 2013, 280, 1874–1894.
- 12. Golczak, M.; Kiser, P.D.; Sears, A.E.; Lodowski, D.T.; Blaner, W.S.; Palczewski, K. Structural basis for the acyltransferase activity of lecithin:retinol acyltransferase-like proteins. Biol. Chem. 2012, 287, 23790–23807.
- 13. Jin, X.H.; Okamoto, Y.; Morishita, J.; Tsuboi, K.; Tonai, T.; Ueda, N. Discovery and characterization of a Ca2+-independent phosphatidylethanolamine N-acyltransferase generating the anandamide precursor and its congeners. J. Biol. Chem. 2007, 282, 3614–3623.
- 14. Jin, X.H.; Uyama, T.; Wang, J.; Okamoto, Y.; Tonai, T.; Ueda, N. cDNA cloning and characterization of human and mouse Ca(2+)-independent phosphatidylethanolamine N-acyltransferases. Biochim. Biophys. Acta 2009, 1791, 32–38.
- 15. Okamoto, Y.; Morishita, J.; Tsuboi, K.; Tonai, T.; Ueda, N. Molecular characterization of a phospholipase D generating anandamide and its congeners. J. Biol. Chem. 2004, 279, 5298– 5305.
- 16. Simon, G.M.; Cravatt, B.F. Characterization of mice lacking candidate N-acyl ethanolamine biosynthetic enzymes provides evidence for multiple pathways that contribute to endocannabinoid production in vivo. Mol. Biosyst. 2010, 6, 1411–1418.
- 17. Liu, J.; Wang, L.; Harvey-White, J.; Osei-Hyiaman, D.; Razdan, R.; Gong, Q.; Chan, A.C.; Zhou, Z.; Huang, B.X.; Kim, H.Y.; et al. A biosynthetic pathway for anandamide. Proc. Natl. Acad. Sci. USA 2006, 103, 13345–13350.
- 18. Sun, Y.X.; Tsuboi, K.; Okamoto, Y.; Tonai, T.; Murakami, M.; Kudo, I.; Ueda, N. Biosynthesis of anandamide and N-palmitoylethanolamine by sequential actions of phospholipase A2 and lysophospholipase D. Biochem. J. 2004, 380, 749–756.
- 19. McKinney, M.K.; Cravatt, B.F. Structure and function of fatty acid amide hydrolase. Annu. Rev. Biochem. 2005, 74, 411–432.
- 20. Wei, B.Q.; Mikkelsen, T. S.; McKinney, M.K.; Lander, E.S.; Cravatt, B.F. A second fatty acid amide hydrolase with variable distribution among placental mammals. J. Biol. Chem. 2006, 281, 36569–36578.
- 21. Tsuboi, K.; Takezaki, N.; Ueda, N. The N-acylethanolamine-hydrolyzing acid amidase (NAAA). Chem. Biodivers. 2007, 4, 1914–1925.
- 22. Van der Stelt, M.; van Kuik, J.A.; Bari, M.; van Zadelhoff, G.; Leeflang, B.R.; Veldink, G.A.; Finazzi-Agro, A.; Vliegenthart, J.F.; Maccarrone, M. Oxygenated metabolites of anandamide and 2-arachidonoylglycerol: Conformational analysis and interaction with cannabinoid receptors, membrane transporter, and fatty acid amide hydrolase. J. Med. Chem. 2002, 45, 3709–3720.
- 23. Rouzer, C.A.; Marnett, L.J. Endocannabinoid oxygenation by cyclooxygenases, lipoxygenases, and cytochromes P450: Cross-talk between the eicosanoid and endocannabinoid signaling pathways. Chem. Rev. 2011, 111, 5899–5921.
- 24. Funk, C.D. Prostaglandins and leukotrienes: Advances in eicosanoid biology. Science 2001, 294, 1871–1875.
- 25. Snider, N.T.; Walker, V.J.; Hollenberg, P.F. Oxidation of the endogenous cannabinoid arachidonoyl ethanolamide by the cytochrome P450 monooxygenases: Physiological and pharmacological implications. Pharmacol. Rev. 2010, 62, 136–154.
- 26. Zygmunt, P.M.; Ermund, A.; Movahed, P.; Andersson, D.A.; Simonsen, C.; Jonsson, B.A.; Blomgren, A.; Birnir, B.; Bevan, S.; Eschalier, A.; et al. Monoacylglycerols activate TRPV1-a link between phospholipase C and TRPV1. PLoS One 2013, 8, e81618.
- 27. Hashimotodani, Y.; Ohno-Shosaku, T.; Tsubokawa, H.; Ogata, H.; Emoto, K.; Maejima, T.; Araishi, K.; Shin, H.S.; Kano, M. Phospholipase Cbeta serves as a coincidence detector through its Ca2+ dependency for triggering retrograde endocannabinoid signal. Neuron 2005, 45, 257–268.
- 28. Maejima, T.; Oka, S.; Hashimotodani, Y.; Ohno-Shosaku, T.; Aiba, A.; Wu, D.; Waku, K.; Sugiura, T.; Kano, M. Synaptically driven endocannabinoid release requires Ca2+-assisted metabotropic glutamate receptor subtype 1 to phospholipase Cbeta4 signaling cascade in the cerebellum. J. Neurosci. 2005, 25, 6826–6835.
- 29. Bisogno, T.; Howell, F.; Williams, G.; Minassi, A.; Cascio, M.G.; Ligresti, A.; Matias, I.; Schiano-Moriello, A.; Paul, P.; Williams, E.J.; et al. Cloning of the first sn1-DAG lipases points to the spatial and temporal regulation of endocannabinoid signaling in the brain. J. Cell Biol. 2003, 163, 463–468.
- 30. Chanda, P.K.; Gao, Y.; Mark, L.; Btesh, J.; Strassle, B.W.; Lu, P.; Piesla, M.J.; Zhang, M.Y.; Bingham, B.; Uveges, A.; et al. Monoacylglycerol lipase activity is a critical modulator of the tone and integrity of the endocannabinoid system. Mol. Pharmacol. 2010, 78, 996–1003.
- 31. Blankman, J.L.; Simon, G.M.; Cravatt, B.F. A comprehensive profile of brain enzymes that hydrolyze the endocannabinoid 2-arachidonoylglycerol. Chem. Biol. 2007, 14, 1347–1356.
- 32. Marrs, W.R.; Blankman, J.L.; Horne, E.A.; Thomazeau, A.; Lin, Y.H.; Coy, J.; Bodor, A.L.; Muccioli, G.G.; Hu, S.S.; Woodruff, G.; et al. The serine hydrolase ABHD6 controls the accumulation and efficacy of 2-AG at cannabinoid receptors. Nat. Neurosci. 2010, 13, 951–957.
- 33. Chu, C.J.; Huang, S.M.; de Petrocellis, L.; Bisogno, T.; Ewing, S.A.; Miller, J.D.; Zipkin, R.E.; Daddario, N.; Appendino, G.; Di Marzo, V.; et al. Noleoyldopamine, a novel endogenous capsaicin-like lipid that produces hyperalgesia. J. Biol. Chem. 2003, 278, 13633–13639.
- 34. O’Sullivan, S.E. Cannabinoids go nuclear: Evidence for activation of peroxisome proliferator-activated receptors. Br. J. Pharmacol. 2007, 152, 576–582.
- 35. Hanus, L.; Abu-Lafi, S.; Fride, E.; Breuer, A.; Vogel, Z.; Shalev, D.E.; Kustanovich, I.; Mechoulam, R. 2-Arachidonyl glyceryl ether, an endogenous agonist of the cannabinoid CB1 receptor. Proc. Natl. Acad. Sci. USA 2001, 98, 3662–3665.
- 36. Porter, A.C.; Sauer, J.M.; Knierman, M.D.; Becker, G.W.; Berna, M.J.; Bao, J.; Nomikos, G.G.; Carter, P.; Bymaster, F.P.; Leese, A.B.; et al. Characterization of a novel endocannabinoid, virodhamine, with antagonist activity at the CB1 receptor. J. Pharmacol. Exp. Ther. 2002, 301, 1020–1024.
- 37. Ross, R.A. The enigmatic pharmacology of GPR55. Trends Pharmacol. Sci. 2009, 30, 156–163.
- 38. Ligresti, A.; Petrosino, S.; Di Marzo, V. From endocannabinoid profiling to “endocannabinoid therapeutics”. Curr. Opin. Chem. Biol. 2009, 13, 321–331.
- 39. Brown, I.; Cascio, M.G.; Rotondo, D.; Pertwee, R.G.; Heys, S.D.; Wahle, K.W. Cannabinoids and omega-3/6 endocannabinoids as cell death and anticancer modulators. Prog. Lipid Res. 2013, 52, 80–109.
- 40. Balvers, M.G.; Wortelboer, H.M.; Witkamp, R.F.; Verhoeckx, K.C. Liquid chromatography-tandem mass spectrometry analysis of free and esterified fatty acid N-acyl ethanolamines in plasma and blood cells. Anal. Biochem. 2013, 434, 275–283.
- 41. Rovito, D.; Giordano, C.; Vizza, D.; Plastina, P.; Barone, I.; Casaburi, I.; Lanzino, M.; de Amicis, F.; Sisci, D.; Mauro, L.; et al. Omega-3 PUFA ethanolamides DHEA and EPEA induce autophagy through PPARγ activation in MCF-7 breast cancer cells. J. Cell. Physiol. 2013, 228, 1314–1322.
- 42. Brown, I.; Wahle, K.W.; Cascio, M.G.; Smoum-Jaouni. R.; Mechoulam, R.; Pertwee, R.G.; Heys, S.D. Omega-3 N-acylethanolamines are endogenously synthesised from omega-3 fatty acidsin different human prostate and breast cancer cell lines. Prostaglandins Leukot. Essent. Fat. Acids 2011, 85, 305–310.
- 43. Meijerink, J.; Plastina, P.; Vincken, J.P.; Poland, M.; Attya, M.; Balvers, M.; Gruppen, H.; Gabriele, B.; Witkamp, R.F. The ethanolamide metabolite of DHA, docosahexaenoylethanolamine, shows immunomodulating effects in mouse peritoneal and RAW264.7 macrophages: Evidence for a new link between fish oil and inflammation. Br. J. Nutr. 2011, 4, 1–10.
- 44. Balvers, M.G.; Verhoeckx, K.C.; Plastina, P.; Wortelboer, H.M.; Meijerink, J.; Witkamp, R.F. Docosahexaenoic acid and eicosapentaenoic acid are converted by 3T3-L1 adipocytes to N-acyl ethanolamines with anti-inflammatory properties. Biochim. Biophys. Acta 2010, 1801, 1107–1114.
- 45. Poli, E.; Manfe, S.; Capuzzo, D.; Gava, S.; Vigano, F.; Coronella, M.L.; Gangemi, M. DHEA pre-treated patients, poor responders to a first IVF (ICSI) cycle: Clinical results. Clin. Exp. Obstet. Gynecol. 2014, 41, 5–9.
- 46. Hansen, H.S. Palmitoylethanolamide and other anandamide congeners. Proposed role in the diseased brain. Exp. Neurol. 2010, 224, 48–55.
- 47. Ho, W.S.; Barrett, D.A.; Randall, M.D. “Entourage” effects of N-palmitoylethanolamide and N-oleoylethanolamide on vasorelaxation to anandamide occur through TRPV1 receptors. Br. J. Pharmacol. 2008, 155, 837–846.
- 48. Costa, B.; Comelli, F.; Bettoni, I.; Colleoni, M.; Giagnoni, G. The endogenous fatty acid amide, palmitoylethanolamide, has anti-allodynic and anti-hyperalgesic effects in a murine model of neuropathic pain: Involvement of CB(1), TRPV1 and PPARgamma receptors and neurotrophic factors. Pain 2008, 139, 541–550.
- 49. Almasi, R.; Szoke, E.; Bolcskei, K.; Varga, A.; Riedl, Z.; Sandor, Z.; Szolcsanyi, J.; Petho, G. Actions of 3-methyl-N-oleoyldopamine, 4-methyl-N-oleoyldopamine and N-oleoylethanolamide on the rat TRPV1 receptor in vitro and in vivo. Life Sci. 2008, 82, 644–651.
- 50. Di Cesare Mannelli, L.; D’Agostino, G.; Pacini, A.; Russo, R.; Zanardelli, M.; Ghelardini, C.; Calignano, A. Palmitoylethanolamide is a disease-modifying agent in peripheral neuropathy: Pain relief and neuroprotection share a PPAR-alpha-mediated mechanism. Mediat. Inflamm. 2013, 2013, 328797, doi:10.1155/2013/328797.
- 51. Esposito, G.; Capoccia, E.; Turco, F.; Palumbo, I.; Lu, J.; Steardo, A.; Cuomo, R.; Sarnelli, G.; Steardo, L. Palmitoylethanolamide improves colon inflammation through an enteric glia/toll like receptor 4-dependent PPAR-α activation. Gut 2014, 63, 1300–1312.
- 52. Moriconi, A.; Cerbara, I.; Maccarrone, M.; Topai, A. GPR55: Current knowledge and future perspectives of a purported “Type-3” cannabinoid receptor. Curr. Med. Chem. 2010, 17, 1411–1429.
- 53. Overton, H.A.; Fyfe, M.C.; Reynet, C. GPR119, a novel G protein-coupled receptor target for the treatment of type 2 diabetes and obesity. Br. J. Pharmacol. 2008, 153, S76–S81.
- 54. Cravatt, B.F.; Giang, D.K.; Mayfield, S.P.; Boger, D.L.; Lerner, R.A.; Gilula, N.B. Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature 1996, 384, 83–87.
- 55. Ueda, N.; Tsuboi, K.; Uyama, T. N-acylethanolamine metabolism with special reference to N-acylethanolamine-hydrolyzing acid amidase (NAAA). Prog. Lipid Res. 2010, 49, 299–315.
- 56. Artmann, A.; Petersen, G.; Hellgren, L.I.; Boberg, J.; Skonberg C.; Nellemann, C.; Hansen, S.H.; Hansen, H.S. Influence of dietary fatty acids on endocannabinoid and N-acylethanolamine levels in rat brain, liver and small intestine. Biochim. Biophys. Acta 2008, 1781, 200–212.
- 57. Lucanic, M.; Held, J.M.; Vantipalli, M.C.; Klang, I.M.; Graham, J.B.; Gibson, B.W.; Lithgow, G.J.; Gill, M.S. N-acylethanolamine signalling mediates the effect of diet on lifespan in Caenorhabditis elegans. Nature 2011, 473, 226–229.
- 58. Brown, I.; Cascio, M.G.; Wahle, K.W.; Smoum, R.; Mechoulam, R.; Ross, R.A.; Pertwee, R.G.; Heys, S.D. Cannabinoid receptor-dependent and -independent anti-proliferative effects of omega-3 ethanolamides in androgen receptor-positive and -negative prostate cancer cell lines. Carcinogenesis 2010, 31, 1584–1591.
- 59. Di Patrizio, N.V.; Piomelli, D. The thrifty lipids: Endocannabinoids and the neural control of energy conservation. Trends Neurosci. 2012, 35, 403–411.
- 60. Maccarrone, M. Endocannabinoids: Friends and foes of reproduction. Prog. Lipid Res. 2009, 48, 344–354.
- 61. Maione, S.; Costa, B.; di Marzo, V. Endocannabinoids: A unique opportunity to develop multitarget analgesics. Pain 2013, 154, S87–S93.
- 62. Galve-Roperh, I.; Chiurchiu, V.; Diaz-Alonso, J.; Bari, M.; Guzman, M.; Maccarrone, M. Cannabinoid receptor signaling in progenitor/stem cell proliferation and differentiation. Prog. Lipid Res. 2013, 52, 633–650.
- 63. Pacher, P.; Kunos, G. Modulating the endocannabinoid system in human health and disease—Successes and failures. FEBS J. 2013, 280, 1918–1943.
- 64. Bisogno, T.; Maccarrone, M. Latest advances in the discovery of fatty acid amide hydrolase inhibitors. Expert Opin. Drug Discov. 2013, 8, 509–522.
- 65. Gaetani, S.; Kaye, W.H.; Cuomo, V.; Piomelli, D. Role of endocannabinoids and their analogues in obesity and eating disorders. Eat. Weight Disord. 2008, 13, e42–e46.
- 66. Maccarrone, M.; Bernardi, G.; Agro, A.F.; Centonze, D. Cannabinoid receptor signalling in neurodegenerative diseases: A potential role for membrane fluidity disturbance. Br. J. Pharmacol. 2011, 163, 1379–1390.
- 67. Pertwee, R.G. Targeting the endocannabinoid system with cannabinoid receptor agonists: Pharmacological strategies and therapeutic possibilities. Philos. Trans. R. Soc. Lond. B Biol. Sci. 2012, 367, 3353–3363.
- 68. McPartland, J.M.; Guy, G.; Di Marzo, V. Care and feeding of the endocannabinoid system: A systematic review of potential clinical interventions that upregulate the endocannabinoid system. PLoS One 2014, 9, e89566.
- 69. Di Marzo, V.; Petrosino, S. Endocannabinoids and the regulation of their levels in health and disease. Curr. Opin. Lipidol. 2007, 18, 129–140.
- 70. Katona, I.; Freund, T.F. Endocannabinoid signaling as a synaptic circuit breaker in neurological disease. Nat. Med. 2008, 14, 923–930.
- 71. Schlosburg, J.E.; Blankman, J.L.; Long, J.Z.; Nomura, D.K.; Pan, B.; Kinsey, S.G.; Nguyen, P.T.; Ramesh, D.; Booker, L.; Burston, J.J.; et al. Chronic monoacylglycerol lipase blockade causes functional antagonism of the endocannabinoid system. Nat. Neurosci. 2010, 13, 1113–1119.
- 72. Zoerner, A.A.; Gutzki, F.M.; Batkai, S.; May, M.; Rakers, C.; Engeli, S.; Jordan, J.; Tsikas, D. Quantification of endocannabinoids in biological systems by chromatography and mass spectrometry: A comprehensive review from an analytical and biological perspective. Biochim. Biophys. Acta 2011, 1811, 706–723.
- 73. Alger, B.E.; Kim, J. Supply and demand for endocannabinoids. Trends Neurosci. 2011, 34, 304–315.
- 74. Di Marzo, V.; de Petrocellis, L. Why do cannabinoid receptors have more than one endogenous ligand? Philos. Trans. R. Soc. Lond. B Biol. Sci. 2012, 367, 3216–3228.
- 75. Jung, K.M.; Clapper, J.R.; Fu, J.; D’Agostino, G.; Guijarro, A.; Thongkham, D.; Avanesian, A.; Astarita, G.; Di Patrizio, N.V.; Frontini, A.; et al. 2-arachidonoylglycerol signaling in forebrain regulates systemic energy metabolism. Cell Metab. 2012, 15, 299–310.
- 76. Sugiura, T.; Kobayashi, Y.; Oka, S.; Waku, K. Biosynthesis and degradation of anandamide and 2-arachidonoylglycerol and their possible physiological significance. Prostaglandins Leukot. Essent. Fat. Acids 2002, 66, 173–192.
- 77. Elphick, M.R. The evolution and comparative neurobiology of endocannabinoid signalling. Philos. Trans. R. Soc. Lond. B Biol. Sci. 2012, 367, 3201–3215.
- 78. Wilson, R.I.; Nicoll, R.A. Endogenous cannabinoids mediate retrograde signalling at hippocampal synapses. Nature 2001, 410, 588–592.
- 79. Vaughan, C.W.; Christie, M.J. Retrograde signalling by endocannabinoids. Handb. Exp. Pharmacol. 2005, 168, 367–383.
- 80. Buczynski, M.W.; Parsons, L.H.B. Quantification of brain endocannabinoid levels: Methods, interpretations and pitfalls. J. Pharmacol. 2010, 160, 423–442.
- 81. Maccarrone, M.; Gasperi, V.; Catani, M.V.; Diep, T.A.; Dainese, E.; Hansen, H.S.; Avigliano, L. The endocannabinoid system and its relevance for nutrition. Annu. Rev. Nutr. 2010, 30, 423–440.
- 82. Kleberg, K.; Hassing, H.A.; Hansen, H.S. Classical endocannabinoid-like compounds and their regulation by nutrients. Biofactors 2014, doi:10.1002/biof.1158.
- 83. Engeli, S.; Lehmann, A.C.; Kaminski, J.; Haas, V.; Janke, J.; Zoerner, A.A.; Luft, F.C.; Tsikas, D.; Jordan, J. Influence of dietary fat intake on the endocannabinoid system in lean and obese subjects. Obesity 2014, 22, E70–E76.
- 84. Lafourcade, M.; Larrieu, T.; Mato, S.; Duffaud, A.; Sepers, M.; Matias, I.; de Smedt-Peyrusse, V.; Labrousse, V.F.; Bretillon, L.; Matute, C.; et al. Nutritional omega-3 deficiency abolishes endocannabinoid-mediated neuronal functions. Nat. Neurosci. 2011, 14, 345–350.
- 85. Blankman, J.L.; Cravatt B.F. Chemical probes of endocannabinoid metabolism. Pharmacol. Rev. 2013, 65, 849–871.
- 86. Huang, S.M.; Bisogno, T.; Trevisani, M.; Al-Hayani, A.; de Petrocellis, L.; Fezza, F.; Tognetto, M.; Petros, T.J.; Krey, J.F.; Chu, C.J.; et al. An endogenous capsaicin-like substance with high potency at recombinant and native vanilloid VR1 receptors. Proc. Natl. Acad. Sci. USA 2002, 99, 8400–8405.
- 87. Balvers, M.G.; Verhoeckx, K.C.; Witkamp, R.F. Development and validation of a quantitative method for the determination of 12 endocannabinoids and related compounds in human plasma using liquid chromatography-tandem mass spectrometry. J. Chromatogr. B Anal. Technol. Biomed. Life Sci. 2009, 877, 14–15.
- 88. Fezza, F.; Bisogno, T.; Minassi, A.; Appendino, G.; Mechoulam, R.; Di Marzo, V. Noladin ether, a putative novel endocannabinoid: Inactivation mechanisms and a sensitive method for its quantification in rat tissues. FEBS Lett. 2002, 513, 294–298.
- 89. Sun, Y.; Alexander, S.P.; Kendall, D.A.; Bennett, A.J. Cannabinoids and PPARalpha signalling. Biochem. Soc. Trans. 2006, 34, 1095–1097.
- 90. Sun, Y.; Alexander, S.P.; Garle, M.J. Cannabinoid activation of PPAR alpha; a novel neuroprotective mechanism. Br. J. Pharmacol. 2007, 152, 734–743.
- 91. Sharir, H.; Console-Bram, L.; Mundy, C.; Popoff, S.N.; Kapur, A.; Abood, M.E. The endocannabinoids anandamide and virodhamine modulate the activity of the candidate cannabinoid receptor GPR55. J. Neuroimmune Pharmacol. 2012, 7, 856–865.
- 92. De Petrocellis, L.; Di Marzo, V. Role of endocannabinoids and endovanilloids in Ca2+ signalling. Cell Calcium 2009, 45, 611–624.
- 93. Hu, S.S.; Bradshaw, H.B.; Benton, V.M.; Chen, J.S.; Huang, S.M.; Minassi, A.; Bisogno, T.; Masuda, K.; Tan, B.; Roskoski, R., Jr.; et al. The biosynthesis of N-arachidonoyl dopamine (NADA), a putative endocannabinoid and endovanilloid, via conjugation of arachidonic acid with dopamine. Prostaglandins Leukot. Essent. Fat. Acids 2009, 81, 291–301.
- 94. Lehtonen, M.; Storvik, M.; Malinen, H.; Hyytia, P.; Lakso, M.; Auriola, S.; Wong, G.; Callaway, J.C. Determination of endocannabinoids in nematodes and human brain tissue by liquid chromatography electrospray ionization tandem mass spectrometry. J. Chromatogr. B Anal. Technol. Biomed. Life Sci. 2011, 879, 677–694.
- 95. Bystrowska, B.; Smaga, I.; Tyszka-Czochara, M.; Filip, M. Troubleshooting in LC-MS/MS method for determining endocannabinoid and endocannabinoid-like molecules in rat brain structures applied to assessing the brain endocannabinoid / endovanilloid system significance. Toxicol. Mech. Methods 2014, 24, 315–322.
- 96. Burr, G.O.; Burr, M.M. Nutrition classics from The Journal of Biological Chemistry 82:345-67, 1929. A new deficiency disease produced by the rigid exclusion of fat from the diet. Nutr. Rev. 1973, 31, 248–249.
- 97. Barrett, S.J. The role of omega-3 polyunsaturated fatty acids in cardiovascular health. Altern. Ther. Health Med. 2013, 1, 26–30.
- 98. Maskrey, B.H.; Megson, I.L.; Rossi, A.G.; Whitfield, P.D. Emerging importance of omega-3 fatty acids in the innate immune response: Molecular mechanisms and lipidomic strategies for their analysis. Mol. Nutr. Food Res. 2013, 57, 1390–1400.
- 99. Peskin, B.S. Why fish oil fails: A comprehensive 21st century lipids-based physiologic analysis. J. Lipids 2014, 2014, 495761.
- 100. Morales-Lazaro, S.L.; Simon, S.A.; Rosenbaum, T. The role of endogenous molecules in modulating pain through transient receptor potential vanilloid 1 (TRPV1). J. Physiol. 2013, 591, 3109–3121.
- 101. Park, C.K.; Xu, Z.Z.; Liu, T.; Serhan, C.N.; Ji, R.R. Resolvin D2 is a potent endogenous inhibitor for transient receptor potential subtype V1/A1, inflammatory pain, and spinal cord synaptic plasticity in mice: Distinct roles of resolvin D1, D2, and E1. J. Neurosci. 2011, 31, 18433–18438.
- 102. Weylandt, K.H.; Chiu, C.Y.; Gomolka, B.; Waechter, S.F.; Wiedenmann, B. Omega-3 fatty acids and their lipid mediators: Towards an understanding of resolvin and protectin formation. Prostaglandins Other Lipid Mediat. 2012, 97, 73–82.
- 103. Russell, C.D.; Schwarze, J. The role of pro-resolution lipid mediators in infectious disease. Immunology 2014, 141, 166–173.
- 104. Citraro, R.; Russo, E.; Scicchitano, F.; van Rijn, C.M.; Cosco, D.; Avagliano, C.; Russo, R.; D’Agostino, G.; Petrosino, S.; Guida, F.; et al. Antiepileptic action of N-palmitoylethanolamine through CB1 and PPAR-α receptor activation in a genetic model of absence epilepsy. Neuropharmacology 2013, 69, 115–126.
- 105. Esposito, E.; Impellizzeri, D.; Mazzon, E.; Paterniti, I.; Cuzzocrea, S. Neuroprotective activities of palmitoylethanolamide in an animal model of Parkinson’s disease. PLoS One 2012, 7, e41880.
- 106. Fu, J.; Bottegoni, G.; Sasso, O.; Bertorelli, R.; Rocchia, W.; Masetti, M.; Guijarro, A.; Lodola, A.; Armirotti, A.; Garau, G.; et al. A catalytically silent FAAH-1 variant drives anandamide transport in neurons. Nat. Neurosci. 2011, 15, 64–69.
- 107. Guzman, M.; Lo Verme, J.; Fu, J.; Oveisi, F.; Blazquez, C.; Piomelli, D. Oleoylethanolamide stimulates lipolysis by activating the nuclear receptor peroxisome proliferator-activated receptor alpha (PPAR-alpha). J. Biol. Chem. 2004, 279, 27849–27854.
- 108. Suardiaz, M.; Estivill-Torrus, G.; Goicoechea, C.; Bilbao, A.; Rodriguez de Fonseca, F. Analgesic properties of oleoylethanolamide (OEA) in visceral and inflammatory pain. Pain 2007, 133, 99–110.
- 109. Moran, B.M.; Abdel-Wahab, Y.H.; Flatt, P.R.; McKillop, A.M. Activation of GPR119 by fatty acid agonists augments insulin release from clonal β-cells and isolated pancreatic islets and improves glucose tolerance in mice. Biol. Chem. 2014, 395, 453–464.
- 110. Hansen, H.S.; Rosenkilde, M.M.; Holst, J.J.; Schwartz, T.W. GPR119 as a fat sensor. Trends Pharmacol. Sci. 2012, 33, 374–381.
- 111. Lan, H.; Vassileva, G.; Corona, A.; Liu, L.; Baker, H.; Golovko, A.; Abbondanzo, S.J.; Hu, W.; Yang, S.; Ning, Y.; et al. GPR119 is required for physiological regulation of glucagon-like peptide-1 secretion but not for metabolic homeostasis. J. Endocrinol. 2009, 201, 219–230.
- 112. Maccarrone, M.; Cartoni, A.; Parolaro, D.; Margonelli, A.; Massi, P.; Bari, M.; Battista, N.; Finazzi-Agro, A. Cannabimimetic activity, binding, and degradation of stearoylethanolamide within the mouse central nervous system. Mol. Cell. Neurosci. 2002, 21, 126–140.
- 113. Dalle Carbonare, M.; Del Giudice, E.; Stecca, A.; Colavito, D.; Fabris, M.; D’Arrigo, A.; Bernardini, D.; Dam, M.; Leon, A. A saturated N-acylethanolamine other than N-palmitoyl ethanolamine with anti-inflammatory properties: A neglected story. J. Neuroendocrinol. 2008, 1, 26–34.
- 114. Ghafouri, N.; Ghafouri, B.; Larsson, B.; Stensson, N.; Fowler, C.J.; Gerdle, B. Palmitoylethanolamide and stearoylethanolamide levels in the interstitium of the trapezius muscle of women with chronic widespread pain and chronic neck-shoulder pain correlate with pain intensity and sensitivity. Pain 2013, 154, 1649–1658.
- 115. Han, B.; Wright, R.; Kirchhoff, A.M.; Chester, J.A.; Cooper, B.R.; Davisson, V.J.; Barker, E. Quantitative LC-MS/MS analysis of arachidonoyl amino acids in mouse brain with treatment of FAAH inhibitor. Anal. Biochem. 2013, 432, 74–81.
- 116. Ottria, R.; Ravelli, A.; Gigli, F.; Ciuffreda, P. Simultaneous ultra-high performance liquid chromathograpy-electrospray ionization-quadrupole-time of flight mass spectrometry quantification of endogenous anandamide and related N-acylethanolamides in bio-matrices. J. Chromatogr. B Anal. Technol. Biomed. Life Sci. 2014, 958, 83–89.
- 117. Terrazzino, S.; Berto, F.; Dalle Carbonare, M.; Fabris, M.; Guiotto, A.; Bernardini, D.; Leon, A. Stearoylethanolamide exerts anorexic effects in mice via down-regulation of liver stearoyl-coenzyme A desaturase-1 mRNA expression. FASEB J. 2004, 18, 1580–1582.
- 118. Huang, S.M.; Bisogno, T.; Petros, T.J.; Chang, S.Y.; Zavitsanos, P.A.; Zipkin, R.E.; Sivakumar, R.; Coop, A.; Maeda, D.Y.; De Petrocellis, L.; et al. Identification of a new class of molecules, the arachidonyl amino acids, and characterization of one member that inhibits pain. J. Biol. Chem. 2001, 276, 42639–42644.
- 119. Milman, G.; Maor, Y.; Abu-Lafi, S.; Horowitz, M.; Gallily, R.; Batkai, S.; Mo, F.M.; Offertaler, L.; Pacher, P.; Kunos, G.; et al. N-arachidonoyl L-serine, an endocannabinoid-like brain constituent with vasodilatory properties. Proc. Natl. Acad. Sci. USA 2006, 103, 2428–2433.
- 120. Hanus, L.; Shohami, E.; Bab, I.; Mechoulam, R. N-Acyl amino acids and their impact on biological processes. Biofactors 2014, doi:10.1002/biof.1166.
- 121. Kohno, M.; Hasegawa, H.; Inoue, A.; Muraoka, M.; Miyazaki, T.; Oka, K.; Yasukawa, M. Identification of N-arachidonylglycine as the endogenous ligand for orphan G-protein-coupled receptor GPR18. Biochem. Biophys. Res. Commun. 2006, 347, 827–832.
- 122. McHugh, D.; Roskowski, D.; Xie, S.; Bradshaw, H.B. Δ(9)-THC and N-arachidonoyl glycine regulate BV-2 microglial morphology and cytokine release plasticity: Implications for signaling at GPR18. Front. Pharmacol. 2014, 4, 162, doi:10.3389/fphar.2013.00162.
- 123. Penumarti, A.; Abdel-Rahman, A.A. The novel endocannabinoid receptor GPR18 is expressed in the rostral ventrolateral medulla and exerts tonic restraining influence on blood pressure. J. Pharmacol. Exp. Ther. 2014, 349, 29–38.
- 124. Oh, D.Y.; Yoon, J.M.; Moon, M.J.; Hwang, J.I.; Choe, H.; Lee, J.Y.; Kim, J.I.; Kim, S.; Rhim, H.; O’Dell, D.K.; et al. Identification of farnesyl pyrophosphate and N-arachidonylglycine as endogenous ligands for GPR92. J. Biol. Chem. 2008, 283, 21054–21064.
- 125. Cascio, M.G.; Minassi, A.; Ligresti, A.; Appendino, G.; Burstein, S.; Di Marzo, V. A structure-activity relationship study on N-arachidonoyl-amino acids as possible endogenous inhibitors of fatty acid amide hydrolase. Biochem. Biophys. Res. Commun. 2004, 314, 192–196.
- 126. Cohen-Yeshurun, A.; Willner, D.; Trembovler, V.; Alexandrovich, A.; Mechoulam, R.; Shohami, E.; Leker, R.R. N-arachidonoyl-L-serine (AraS) possesses proneurogenic properties in vitro and in vivo after traumatic brain injury. J. Cereb. Blood Flow Metab. 2013, 33, 1242–1250.
- 127. Hesselink, J.M.; Hekker, T.A. Therapeutic utility of palmitoylethanolamide in the treatment of neuropathic pain associated with various pathological conditions: A case series. J. Pain Res. 2012, 5, 437–442.
- 128. Di Marzo, V.; Ligresti, A.; Morera, E.; Nalli, M.; Ortar, G. The anandamide membrane transporter. Structure-activity relationships of anandamide and oleoylethanolamine analogs with phenyl rings in the polar head group region. Bioorg. Med. Chem. 2004, 12, 5161–5169.
- 129. Min, R.; di Marzo, V.; Mansvelder, H.D. DAG lipase involvement in depolarization-induced suppression of inhibition: Does endocannabinoid biosynthesis always meet the demand? Neuroscientist 2010, 16, 608–613.
- 130. Di Marzo, V. Endocannabinoid signaling in the brain: Biosynthetic mechanisms in the limelight. Nat. Neurosci. 2011, 14, 9–15.
- 131. Tsuboi, K.; Okamoto, Y.; Ikematsu, N.; Inoue, M.; Shimizu, Y.; Uyama, T.; Wang, J.; Deutsch, D.G.; Burns, M.P.; Ulloa, N.M.; et al. Enzymatic formation of N-acylethanolamines from N-acylethanolamine plasmalogen through N-acylphosphatidylethanolamine-hydrolyzing phospholipase D-dependent and -independent pathways. Biochim. Biophys. Acta 2011, 1811, 565–577.
- 132. Fukami, K.; Inanobe, S.; Kanemaru, K.; Nakamura, Y. Phospholipase C is a key enzyme regulating intracellular calcium and modulating the phosphoinositide balance. Prog. Lipid Res. 2010, 49, 429–437.
- 133. Berdyshev, E.V.; Schmid, P.C.; Krebsbach, R.J.; Schmid, H.H. Activation of PAF receptors results in enhanced synthesis of 2-arachidonoylglycerol (2-AG) in immune cells. FASEB J. 2001, 15, 2171–2178.
- 134. Oka, S.; Yanagimoto, S.; Ikeda, S.; Gokoh, M.; Kishimoto, S.; Waku, K.; Ishima, Y.; Sugiura, T. Evidence for the involvement of the cannabinoid CB2 receptor and its endogenous ligand 2-arachidonoylglycerol in 12-O-tetradecanoylphorbol-13-acetate-induced acute inflammation in mouse ear. J. Biol. Chem. 2005, 280, 18488–18497.
- 135. Gao, Y.; Vasilyev, D.V.; Goncalves, M.B.; Howell, F.V.; Hobbs, C.; Reisenberg, M.; Shen, R.; Zhang, M.Y.; Strassle, B.W.; Lu, P.; et al. Loss of retrograde endocannabinoid signaling and reduced adult neurogenesis in diacylglycerol lipase knock-out mice. J. Neurosci. 2010, 30, 2017–2024.
- 136. Tanimura, A.; Yamazaki, M.; Hashimotodani, Y.; Uchigashima, M.; Kawata, S.; Abe, M.; Kita, Y.; Hashimoto, K.; Shimizu, T.; Watanabe, M.; et al. The endocannabinoid 2-arachidonoylglycerol produced by diacylglycerol lipase alpha mediates retrograde suppression of synaptic transmission. Neuron 2010, 65, 320–327.
- 137. Maccarrone, M.; Rossi, S.; Bari, M.; de Chiara, V.; Fezza, F.; Musella, A.; Gasperi, V.; Prosperetti, C.; Bernardi, G.; Finazzi-Agro, A.; et al. Anandamide inhibits metabolism and physiological actions of 2-arachidonoylglycerol in the striatum. Nat. Neurosci. 2008, 11, 152–159.
- 138. Shonesy, B.C.; Wang, X.; Rose, K.L.; Ramikie, T.S.; Cavener, V.S.; Rentz, T.; Baucum, A.J.; Jalan-Sakrikar, N.; Mackie, K.; Winder, D.G.; et al. CaMKII regulates diacylglycerol lipase-α and striatal endocannabinoid signaling. Nat. Neurosci. 2013, 16, 456–463.
- 139. Price, T.J.; Jeske, N.A.; Flores, C.M.; Hargreaves, K.M. Pharmacological interactions between calcium/calmodulin-dependent kinase II alpha and TRPV1 receptors in rat trigeminal sensory neurons. Neurosci. Lett. 2005, 389, 94–98.
- 140. Di Marzo, V.; Fontana, A.; Cadas, H.; Schinelli, S.; Cimino, G.; Schwartz, J.C.; Piomelli, D. Formation and inactivation of endogenous cannabinoid anandamide in central neurons. Nature 1994, 372, 686–691.
- 141. Fezza, F.; Oddi, S.; Di Tommaso, M.; de Simone, C.; Rapino, C.; Pasquariello, N.; Dainese, E.; Finazzi-Agro, A.; Maccarrone, M. Characterization of biotin-anandamide, a novel tool for the visualization of anandamide accumulation. J. Lipid Res. 2008, 49, 1216–1223.
- 142. Hillard, C.; Jarrahian, A. The movement of N-arachidonoylethanolamine (anandamide) across cellular membranes. Chem. Phys. Lipids 2000, 108, 123–134.
- 143. Fowler, C.J. Transport of endocannabinoids across the plasma membrane and within the cell. FEBS J. 2013, 3280, 1895–1904.
- 144. Deutsch, D.G.; Glaser, S.T.; Howell, J.M.; Kunz, J.S.; Puffenbarger, R.A.; Hillard, C.J.; Abumrad, N. The cellular uptake of anandamide is coupled to its breakdown by fatty-acid amide hydrolase. J. Biol. Chem. 2001, 276, 6967–6973.
- 145. Kaczocha, M.; Hermann, A.; Glaser, S.T.; Bojesen, I.N.; Deutsch, D.G. Anandamide uptake is consistent with rate-limited diffusion and is regulated by the degree of its hydrolysis by fatty acid amide hydrolase. J. Biol. Chem. 2006, 281, 9066–9075.
- 146. Oddi, S.; Fezza, F.; Pasquariello, N.; de Simone, C.; Rapino, C.; Dainese, E.; Finazzi-Agro, A.; Maccarrone, M. Evidence for the intracellular accumulation of anandamide in adiposomes. Cell. Mol. Life Sci. 2008, 65, 840–850.
- 147. Di Pasquale, E.; Chahinian, H.; Sanchez, P.; Fantini, J. The insertion and transport of anandamide in synthetic lipid membranes are both cholesterol-dependent. PLoS One 2009, 4, e4989, doi:10.1371/journal.pone.0004989.
- 148. Oddi, S.; Fezza, F.; Pasquariello, N.; D’Agostino, A.; Catanzaro, G.; De Simone, C.; Rapino, C.; Finazzi-Agro, A.; Maccarrone, M. Molecular identification of albumin and Hsp70 as cytosolic 12 anandamide-binding proteins. Chem. Biol. 2009, 16, 624–632.
- 149. Kaczocha, M.; Glaser, S.T.; Deutsch, D.G. Identification of intracellular carriers for the endocannabinoid anandamide. Proc. Natl. Acad. Sci. USA 2009, 106, 6375–6380.
- 150. Kaczocha, M.; Vivieca, S.; Sun, J.; Glaser, S.T.; Deutsch, D.G. Fatty acid-binding proteins transport N-acylethanolamines to nuclear receptors and are targets of endocannabinoid transport inhibitors. J. Biol. Chem. 2012, 287, 3415–3424.
- 151. Chicca, A.; Marazzi, J.; Nicolussi, S.; Gertsch, J. Evidence for bidirectional endocannabinoid transport across cell membranes. J. Biol. Chem. 2012, 287, 34660–34682.
- 152. Maccarrone, M.; Bari, M.; Battista, N.; Finazzi-Agro, A. Estrogen stimulates arachidonoylethanolamide release from human endothelial cells and platelet activation. Blood 2002 100, 4040–4048.
- 153. Hillard, C.J.; Jarrahian, A. Accumulation of anandamide: Evidence for cellular diversity. Neuropharmacology 2005, 48, 1072–1078.
- 154. Piomelli, D.; Beltramo, M.; Glasnapp, S.; Lin, S.Y.; Goutopoulos, A.; Xie, X.Q.; Makriyannis, A. Structural determinants for recognition and translocation by the anandamide transporter. Proc. Natl. Acad. Sci. USA 1999, 96, 5802–5807.
- 155. Bisogno, T.; Maccarrone, M.; de Petrocellis, L.; Jarrahian, A.; Finazzi-Agro, A.; Hillard, C.; di Marzo, V. The uptake by cells of 2-arachidonoylglycerol, an endogenous agonist of cannabinoid receptors. Eur. J. Biochem. 2001, 268, 1982–1989.
- 156. Hermann, A.; Kaczocha, M.; Deutsch, D.G. 2-Arachidonoylglycerol (2-AG) membrane transport: History and outlook. AAPS J. 2006, 8, 409–412.
- 157. Ehehalt, R.; Fullekrug, J.; Pohl, J.; Ring, A.; Herrmann, T.; Stremmel, W. Translocation of long chain fatty acids across the plasma membrane—Lipid rafts and fatty acid transport proteins. Mol. Cell. Biochem. 2006, 284, 135–140.
- 158. Fezza, F.; de Simone, C.; Amadio, D.; Maccarrone, M. Fatty acid amide hydrolase: A gate-keeper of the endocannabinoid system. Subcell. Biochem. 2008, 49, 101–132.
- 159. McKinney, M.K.; Cravatt, B.F. Evidence for distinct roles in catalysis for residues of the serine-serine-lysine catalytic triad of fatty acid amide hydrolase. J. Biol. Chem. 2003, 278, 37393–37399.
- 160. Kaczocha, M.; Glaser, S.T.; Chae, J.; Brown, D.A.; Deutsch, D.G. Lipid droplets are novel sites of N-acylethanolamine inactivation by fatty acid amide hydrolase-2. J. Biol. Chem. 2010, 285, 2796–2806.
- 161. Ponzano, S.; Bertozzi, F.; Mengatto, L.; Dionisi, M.; Armirotti, A.; Romeo, E.; Berteotti, A.; Fiorelli, C.; Tarozzo, G.; Reggiani, A.; et al. Synthesis and structure-activity relationship (SAR) of 2-methyl-4-oxo-3-oxetanylcarbamic acid esters, a class of potent N-acylethanolamine acid amidase (NAAA) inhibitors. J. Med. Chem. 2013, 56, 6917–6934.
- 162. Vitale, R.; Ottonello, G.; Petracca, R.; Bertozzi, S.M.; Ponzano, S.; Armirotti, A.; Berteotti, A.; Dionisi, M.; Cavalli, A.; Piomelli, D.; et al. Synthesis, structure-activity, and structure-stability relationships of 2-substituted-N-(4-oxo-3-oxetanyl) N-acylethanolamine acid amidase (NAAA) inhibitors. Chem. Med. Chem. 2014, 9, 323–336.
- 163. Cravatt, B.F.; Demarest, K.; Patricelli, M.P.; Bracey, M.H.; Giang, D.K.; Martin, B.R.; Lichtman, A.H. Supersensitivity to anandamide and enhanced endogenous cannabinoid signaling in mice lacking fatty acid amide hydrolase. Proc. Natl. Acad. Sci. USA 2001, 98, 9371–9376.
- 164. Pan, B.; Wang, W.; Zhong, P.; Blankman, J.L.; Cravatt, B.F.; Liu Q.S. Alterations of endocannabinoid signaling, synaptic plasticity, learning, and memory in monoacylglycerol lipase knock-out mice. J. Neurosci. 2011, 31, 13420–13430.
- 165. Di Marzo, V.; Maccarrone, M. FAAH and anandamide: Is 2-AG really the odd one out? Trends Pharmacol. Sci. 2008, 29, 229–233.
- 166. Long, J.Z.; Li, W.; Booker, L.; Burston, J.J.; Kinsey, S.G.; Schlosburg, J.E.; Pavon, F.J.; Serrano, A.M.; Selley, D.E.; Parsons, L.H.; et al. Selective blockade of 2-arachidonoylglycerol hydrolysis produces cannabinoid behavioral effects. Nat. Chem. Biol. 2009, 5, 37–44.
- 167. Dinh, T.P.; Carpenter, D.; Leslie, F.M.; Freund, T.F.; Katona, I.; Sensi, S.L.; Kathuria, S.; Piomelli, D. Brain monoglyceride lipase participating in endocannabinoid inactivation. Proc. Natl. Acad. Sci. USA 2002, 99, 10819–10824.
- 168. Ho, S.Y.; Delgado, L.; Storch, J. Monoacylglycerol metabolism in human intestinal Caco-2 cells: Evidence for metabolic compartmentation and hydrolysis. J. Biol. Chem. 2002, 277, 1816–1823.
- 169. Karlsson, M.; Contreras, J.A.; Hellman, U.; Tornqvist, H.; Holm, C. cDNA cloning, tissue distribution, and identification of the catalytic triad of monoglyceride lipase. Evolutionary relationship to esterases, lysophospholipases, and haloperoxidases. Biol. Chem. 1997, 272, 27218–27223.
- 170. Karlsson, M.; Reue, K.; Xia, Y.R.; Lusis, A.J.; Langin, D.; Tornqvist, H.; Holm, C. Exon-intron organization and chromosomal localization of the mouse monoglyceride lipase gene. Gene 2001, 272, 11–18.
- 171. Nomura, D.K.; Long, J.Z.; Niessen, S.; Hoover, H.S.; Ng, S.W.; Cravatt, B.F. Monoacylglycerol lipase regulates a fatty acid network that promotes cancer pathogenesis. Cell 2010, 140, 49–61.
- 172. Galli, G.G.; Multhaupt, H.A.; Carrara, M.; de Lichtenberg, K.H.; Christensen, I.B.; Linnemann, D.; Santoni-Rugiu, E.; Calogero, R.A.; Lund, A.H. Prdm5 suppresses Apc(Min)-driven intestinal adenomas and regulates monoacylglycerol lipase expression. Oncogene 2014, 33, 3342–3350.
- 173. Qin, H.; Ruan, Z.H. The Role of Monoacylglycerol Lipase (MAGL) in the Cancer Progress. Cell Biochem. Biophys. 2014, 70, 33–36.
- 174. Savinainen, J.R.; Saario, S.M.; Laitinen, J.T. The serine hydrolases MAGL, ABHD6 and ABHD12 as guardians of 2-arachidonoylglycerol signalling through cannabinoid receptors. Acta Physiol. 2012, 204, 267–276.
- 175. Tchantchou, F.; Zhang, Y. Selective inhibition of alpha/beta-hydrolase domain 6 attenuates neurodegeneration, alleviates blood brain barrier breakdown, and improves functional recovery in a mouse model of traumatic brain injury. J. Neurotrauma 2013, 30, 565–79.
- 176. Alhouayek, M.; Masquelier, J.; Cani, P.D.; Lambert, D.M.; Muccioli, G.G. Implication of the anti-inflammatory bioactive lipid prostaglandin D2-glycerol ester in the control of macrophage activation and inflammation by ABHD6. Proc. Natl. Acad. Sci. USA 2013, 110, 17558–17563.
- 177. Fiskerstrand, T.; H’mida-Ben Brahim, D.; Johansson, S.; M’zahem, A.; Haukanes, B.I.; Drouot, N.; Zimmermann, J.; Cole, A.J.; Vedeler, C.; Bredrup, C.; et al. Mutations in ABHD12 cause the neurodegenerative disease PHARC: An inborn error of endocannabinoid metabolism. Am. J. Hum. Genet. 2010, 87, 410–417.
- 178. Blankman, J.L.; Long, J.Z.; Trauger, S.A.; Siuzdak, G.; Cravatt, B.F. ABHD12 controls brain lysophosphatidylserine pathways that are deregulated in a murine model of the neurodegenerative disease PHARC. Proc. Natl. Acad. Sci. USA 2013, 110, 1500–1505.
- 179. Kozak, K.R.; Marnett, L.J. Oxidative metabolism of endocannabinoids. Prostaglandins Leukot. Essent. Fat. Acids 2002, 66, 211–220.
- 180. McHugh, D.; McMaster, R.S.; Pertwee, R.G.; Roy, S.; Mahadevan, A.; Razdan, R.K.; Ross, R.A. Novel compounds that interact with both leukotriene B4 receptors and vanilloid TRPV1 receptors. J. Pharmacol. Exp. Ther. 2006, 316, 955–965.
- 181. Starowicz, K.; Przewlocka, B. Modulation of neuropathic-pain-related behaviour by the spinal endocannabinoid/endovanilloid system. Philos. Trans. R. Soc. Lond. B Biol. Sci. 2012, 367, 3286–3299.
- 182. Amadio, D.; Fezza, F.; Catanzaro, G.; Incani, O.; van Zadelhoff, G.; Finazzi Agro, A.; Maccarrone, M. Methylation and acetylation of 15-hydroxyanandamide modulate its interaction with the endocannabinoid system. Biochimie 2010, 92, 378–387.
- 183. Dainese, E.; Sabatucci, A.; Angelucci, C.B.; Barsacchi, D.; Chiarini, M.; Maccarrone, M. Impact of embedded endocannabinoids and their oxygenation by lipoxygenase on membraneproperties. ACS Chem. Neurosci. 2012, 3, 386–392.
- 184. Wong-Ekkabut, J.; Xu, Z.; Triampo, W.; Tang, I.M.; Tieleman, D.P.; Monticelli, L. Effect of lipid peroxidation on the properties of lipid bilayers: A molecular dynamics study. Biophys. J. 2007, 93, 4225–4236.
- 185. Yang, R.; Fredman, G.; Krishnamoorthy, S.; Agrawal, N.; Irimia, D.; Piomelli, D.; Serhan, C.N. Decoding functional metabolomics with docosahexaenoyl ethanolamide (DHEA) identifies novel bioactive signals. J. Biol. Chem. 2011, 286, 31532–31541.
- 186. Prusakiewicz, J.J.; Turman, M.V.; Vila, A.; Ball, H.L.; Al-Mestarihi, A.H.; Di Marzo, V.; Marnett, L.J. Oxidative metabolism of lipoamino acids and vanilloids by lipoxygenases and cyclooxygenases. Arch. Biochem. Biophys. 2007, 464, 260–268.
- 187. Turman, M.V.; Kingsley, P.J.; Rouzer, C.A.; Cravatt, B.F.; Marnett, L.J. Oxidative metabolism of a fatty acid amide hydrolase-regulated lipid, arachidonoyltaurine. Biochemistry 2008, 47, 3917–3925.
- 188. Alhouayek, M.; Muccioli, G.G. COX-2-derived endocannabinoid metabolites as novel inflammatory mediators. Trends Pharmacol. Sci. 2014, 35, 284–292.
- 189. Woodward, D.F.; Carling, R.W.; Cornell, C.L.; Fliri, H.G.; Martos, J.L.; Pettit, S.N.; Liang, Y.; Wang, J.W. The pharmacology and therapeutic relevance of endocannabinoid derived cyclo-oxygenase (COX)-2 products. Pharmacol. Ther. 2008, 120, 71–80.
- 190. Duggan, K.C.; Hermanson, D.J.; Musee, J.; Prusakiewicz, J.J.; Scheib, J.L.; Carter, B.D.; Banerjee, S.; Oates, J.A.; Marnett, L.J. (R)-Profens are substrate-selective inhibitors of endocannabinoid oxygenation by COX-2. Nat. Chem. Biol. 2011, 7, 803–809.
- 191. Prusakiewicz, J.J.; Duggan, K.C.; Rouzer, C.A.; Marnett, L.J. Differential sensitivity and mechanism of inhibition of COX-2 oxygenation of arachidonic acid and 2-arachidonoylglycerol by ibuprofen and mefenamic acid. Biochemistry 2009, 48, 7353–7355.
- 192. Gatta, L.; Piscitelli, F.; Giordano, C.; Boccella, S.; Lichtman, A.; Maione, S.; Di Marzo, V. Discovery of prostamide F2α and its role in inflammatory pain and dorsal horn nociceptive neuron hyperexcitability. PLoS One 2012, 7, e31111.
- 193. Woodward, D.F.; Wang, J.W.; Poloso, N.J. Recent progress in prostaglandin F2α ethanolamide (prostamide F2α) research and therapeutics. Pharmacol. Rev. 2013, 65, 1135–1147.
- 194. Snider, N.T.; Nast, J.A.; Tesmer, L.A.; Hollenberg, P.F. A cytochrome P450-derived epoxygenated metabolite of anandamide is a potent cannabinoid receptor 2-selective agonist. Mol. Pharmacol. 2009, 75, 965–972.
- 195. Stark, K.; Dostalek, M.; Guengerich, F.P. Expression and purification of orphan cytochrome P450 4X1 and oxidation of anandamide. FEBS J. 2008, 275, 3706–3717.
- 196. Pan, B.; Wang, W.; Long, J.Z.; Sun, D.; Hillard, C.J.; Cravatt, B.F.; Liu, Q.S. Blockade of 2-arachidonoylglycerol hydrolysis by selective monoacylglycerol lipase inhibitor 4-nitrophenyl 4-(dibenzo[d][1,3]dioxol-5-yl(hydroxy)methyl)piperidine-1-carboxylate (JZL184) Enhances retrograde endocannabinoid signaling. J. Pharmacol. Exp. Ther. 2009, 331, 591–597.
- 197. Schlosburg, J.E.; Blankman, J.L.; Long, J.Z.; Nomura, D.K.; Pan, B.; Kinsey, S.G.; Nguyen, P.T.; Ramesh, D.; Booker, L.; Burston, J.J.; et al. Chronic monoacylglycerol lipase blockade causes functional antagonism of the endocannabinoidsystem. Nat. Neurosci. 2010, 13, 1113–1119.



