(Ethan B Russo1,*, “Beyond Cannabis: Plants and the Endocannabinoid System”, Trends Pharmacol Sci. 2016 Jul;37(7):594-605.
https://pubmed.ncbi.nlm.nih.gov/27179600/)
1PHYTECS, 204028 1st Avenue SW, Vashon, WA98070, USA
*Αλληλογραφία: ethanrusso@comcast.net (E.B. Russo)
Περίληψη
“Τα φυτά υπήρξαν η κυρίαρχη πηγή φαρμάκων σε όλη τη συντριπτική πλειονότητα της ανθρώπινης ιστορίας, και έτσι παραμένουν σήμερα εκτός των βιομηχανικών κοινωνιών. Ένα από τα πιο ευέλικτα όσον αφορά τη φυτοχημεία της είναι η κάνναβη, η έρευνα της οποίας οδήγησε άμεσα στην ανακάλυψη ενός μοναδικού και ευρέως διαδεδομένου ομοιοστατικού φυσιολογικού ρυθμιστή, του ενδοκανναβινοειδούς συστήματος. Ενώ ήταν η συμβατική σοφία μέχρι πρόσφατα ότι μόνο η κάνναβη περιείχε ενεργούς παράγοντες που επηρεάζουν το ενδοκανναβινοειδές σύστημα, τις τελευταίες δεκαετίες η έρευνα έχει διευρυνθεί και έχει εντοπίσει πολλά επιπλέον φυτά των οποίων τα συστατικά διεγείρουν, ανταγωνίζονται ή ρυθμίζουν διαφορετικές πτυχές αυτού του συστήματος. Αυτά περιλαμβάνουν κοινά τρόφιμα, βότανα, μπαχαρικά και πιο εξωτικά συστατικά, όπως: κάβα, σοκολάτα, μαύρο πιπέρι και πολλά άλλα που εξετάζονται σε αυτήν την ανασκόπηση”.
Σχετικά
Το ενδοκανναβινοειδές σύστημα (ΕΚΣ) (endocannabinoid system, ECS) είναι ένας ομοιοστατικός ρυθμιστής της δραστηριότητας των νευροδιαβιβαστών και σχεδόν κάθε άλλου φυσιολογικού συστήματος στο σώμα.
Το όνομά του προέρχεται από την κάνναβη, το φυτό που παράγει κανναβινοειδή (τετραϋδροκανναβινόλη, κανναβιδιόλη, καρυοφυλλένιο και άλλα) και του οποίου η έρευνα διευκρίνισε τις μυριάδες λειτουργίες του ΕΚΣ.
Τις τελευταίες δύο δεκαετίες, πρόσθετη έρευνα ανακάλυψε ότι πολλές άλλες φυτικές τροφές και βότανα ρυθμίζουν το ΕΚΣ άμεσα και έμμεσα. Η προώθηση αυτής της γνώσης μπορεί να έχει σημαντικές επιπτώσεις για την ανθρώπινη υγεία και τη διατροφή.
Επισκόπηση του ενδοκανναβινοειδούς συστήματος
Η κάνναβη (Cannabis sativa) ήταν ένα σημαντικό εργαλείο στο οπλοστάσιο των βοτανολόγων και στην ιατρική φαρμακοποιία για χιλιετίες, αλλά μόνο τα τελευταία 25 χρόνια η επιστήμη έχει παράσχει καλύτερη κατανόηση των μυριάδων οφελών της. Αυτό ξεκίνησε με την ανακάλυψη των υποδοχέων κανναβινοειδών (βλ. Γλωσσάρι) [CB1, CB2, και του ιοντοτροπικού υποδοχέα κανναβινοειδών, του παροδικού δυναμικού βανιλλοειδούς υποδοχέα 1 (TRPV1)], ακολουθούμενο από ενδογενή κανναβινοειδή [ή ενδοκανναβινοειδή, ανανδαμίδιο (AEA) και 2-αραχιδονοϋλογλυκερόλη (2-AG)] και τα ρυθμιστικά μεταβολικά και καταβολικά τους ένζυμα [υδρολάση αμιδίου λιπαρού οξέος (FAAH), μονοακυλογλυκερολική λιπάση (MAGL) και άλλα], η τριάδα που είναι τώρα συλλογικά γνωστή ως το ενδοκανναβινοειδές σύστημα (ΕΚΣ)[1,2]. Το ΕΚΣ εκτελεί σημαντικές ρυθμιστικές ομοιοστατικές λειτουργίες στον εγκέφαλο, το δέρμα, το πεπτικό σύστημα, το συκώτι, το καρδιαγγειακό σύστημα, την ουρογεννητική λειτουργία, ακόμη και τα οστά[1,3]. Διάφοροι παράγοντες του τρόπου ζωής, συμπεριλαμβανομένων της διατροφής και της αερόβιας δραστηριότητας, επηρεάζουν τη συνολική λειτουργία του ΕΚΣ ή τον “ενδοκανναβινοειδή τόνο” (endocannabinoid tone), που είναι μια συνάρτηση της πυκνότητας των υποδοχέων κανναβινοειδών, της λειτουργικής τους κατάστασης (προς τα πάνω ή προς τα κάτω ρύθμιση / upregulated ή downregulated) και της σχετικής αφθονίας ή έλλειψης ενδοκανναβινοειδών[4]. Μερικοί ήταν αρκετά τολμηροί ώστε να υποδείξουν ότι μια κλινική ανεπάρκεια ενδοκανναβινοειδών βρίσκεται κάτω από πολλές ανθρώπινες ασθένειες που προκαλούν πόνο και ψυχιατρικές διαταραχές[4,5]. Πρόσφατα, πολυάριθμοι φυτικοί παράγοντες και φυτά τροφίμων πέρα από την κάνναβη έχουν εξεταστεί για τις πιθανές ρυθμιστικές τους επιδράσεις στο ΕΚΣ. Ίσως είναι σκόπιμο να αλλάξουμε ελαφρώς το κοινό ρητό για να σκεφτούμε, “Είσαι αυτό που καταναλώνεις”, καθώς ίσως υπάρχουν πολλά περισσότερα μαθήματα που πρέπει να μάθουμε στα δάση και στους αγρούς που μπορεί να βοηθήσουν στην περίθαλψη της ανθρώπινης υγείας.
Φυτά που επηρεάζουν τον CB1, τον ψυχοδραστικό κανναβινοειδή υποδοχέα
Ο CB1, ο νευροτροποποιητικός κανναβινοειδής υποδοχέας, ανακαλύφθηκε το 1988 ως αποτέλεσμα δεκαετιών έρευνας για την τετραϋδροκανναβινόλη (THC), το κύριο ψυχοδραστικό συστατικό της κάνναβης[6], και έχει αποδειχθεί ότι έχει σημαντική ομοιοστατική επιρροή στο κεντρικό νευρικό σύστημα (ΚΝΣ), όπου είναι ο πιο άφθονος υποδοχέας συζευγμένος με πρωτεΐνη G (GPCR)[7], που υπερβαίνει κατά πολύ εκείνους τους νευροδιαβιβαστές που ρυθμίζει. Ένας παρόμοιος αναπόσπαστος ρόλος διαδραματίζεται σε διάφορα άλλα φυσιολογικά συστήματα σε όλο το σώμα. Οι λειτουργίες του ΕΚΣ έχουν χαρακτηριστεί ως “χαλαρώστε, φάτε, κοιμηθείτε, ξεχάστε και προστατέψτε”[8], αλλά η λίστα των συστημάτων που διαμορφώνει αυξάνεται κάθε χρόνο με πρόσθετες ερευνητικές ανακαλύψεις. Ήταν μια μακροχρόνια πεποίθηση ότι οι φυσικές ουσίες που επηρέασαν τον CB1 περιορίζονταν στην THC και μερικά άλλα φυτοκανναβινοειδή (κανναβινόλη, D8-THC, τετραϋδροκανναβιβαρίνη), αλλά αυτή η κατάσταση έχει αλλάξει αργά, καθώς άλλα φυτά που ρυθμίζουν τον υποδοχέα αξίζουν εξέταση. Σε αυτήν την εποχή των γενετικά τροποποιημένων οργανισμών (ΓΤΟ), οι πειραματισμοί έφεραν διαγονιδιακά Pichia spp. ζυμομύκητες που εκφράζουν συνθάση τετραϋδροκανναβινολικού οξέος (THCA)[9,10], το βιοσυνθετικό ένζυμο που καταλύει τον σχηματισμό THCA, του παράγοντα στην κάνναβη που γίνεται THC κατά τη θέρμανση και την αποκαρβοξυλίωση, και αυτή η προσπάθεια μπορεί να επεκταθεί στο μέλλον σε προσπάθειες σύνθεσης νέων κανναβινοειδών.
Παρόλα αυτά, έχουν ξεκινήσει προσπάθειες για τον εντοπισμό παρόμοιων ψυχοδραστικών μορίων σε άλλα φυτά. Μια τέτοια προσπάθεια αφορούσε το Salvia divinorum (Ιερή φασκομηλιά), ένα ψυχοδραστικό μαντικό φυτό του Μεξικού που καπνίζεται ή καταναλώνεται ως διασπαστικό παραισθησιογόνο. Αυτός ο παράγοντας είχε προηγουμένως δοκιμαστεί αρνητικά σε ένα NovaScreenTM για τους υποδοχείς νευροδιαβιβαστών[11]. Είναι ενδιαφέρον ότι, αν και η σαλβινορίνη Α (salvinorin A), το κύριο ενεργό μόριο στο φυτό ήταν αρνητικό για δραστηριότητα στον CB1, τα εκχυλίσματα ολόκληρων φύλλων ήταν θετικά[12] (Εικόνα 1). Λίγο μετά την αναφορά αυτή, η σαλβινορίνη Α αναγνωρίστηκε ως ειδικός αγωνιστής κ-οπιοειδών[13]. Μεταγενέστερες εργασίες κατέδειξαν ότι αυτή η ουσία είχε χαμηλή συγγένεια με CB1 και καμία επίδραση στην αποικοδόμηση των ενδοκανναβινοειδών[14], και το επόμενο έτος η σαλβινορίνη Α αποδείχθηκε ότι αλληλεπιδρά με τα διμερή υποδοχέα CB1/k-οπιοειδών[15], υποδεικνύοντας πιθανώς ότι τα δύο συστήματα μπορεί να παράγουν συγκλίνουσες επιδράσεις στην ίδια οδό και υποδεικνύοντας ότι μια πολύπλοκη σχέση του Salvia με το ΕΚΣ αξίζει να διευκρινιστεί πληρέστερα.
Ένα άλλο κοινό τρόφιμο, το καρότο, το Daucus carota, περιέχει φαλκαρινόλη (falcarinol) (καροτατοξίνη / carotatoxin), ένα φυσικό φυτοφάρμακο και μυκητοκτόνο, σε συγκεντρώσεις 2mg/kg[16], το οποίο δεσμεύει ομοιοπολικά τον CB1 (Ki = 594nM) (Εικόνα 1), δρώντας ως ένας αντίστροφος αγωνιστής, που αναστέλλει το ΑΕΑ στα κερατινοκύτταρα και προκαλεί δερματίτιδα εξ επαφής παρουσία ισταμίνης. Η ιδιαίτερη συνάφεια αυτών των ευρημάτων μένει να καθοριστεί και θα περιλαμβάνει την εξέταση του κατά πόσον τα καρότα ενέχουν ιδιαίτερο κίνδυνο αλλεργίας ή, παρά τον υψηλό γλυκαιμικό τους δείκτη, ο ανταγωνισμός CB1 μπορεί να υποδηλώνει τη χρήση τους ως κατασταλτικό της όρεξης εάν η καροτατοξίνη απορροφάται ακόμη και μέσω του γαστρεντερικού σωλήνα.
Το Kava kava, το Piper methysticum, το “μυστικιστικό πιπέρι”, είναι ένα ευχάριστο ρόφημα των Νήσων του Νότιου Ειρηνικού που προέρχεται από τις ρίζες του φυτού[17,18], του οποίου τα ενεργά συστατικά είναι λιποδιαλυτές καβαλακτόνες (lipid-soluble kavalactones). Τα αποξηραμένα ριζώματα μπορούν να μασηθούν ή, εναλλακτικά, να εκχυλιστούν σε νερό, μερικές φορές με την προσθήκη αιθανόλης ή ακετόνης. Οι κλινικές μελέτες έχουν πραγματοποιηθεί συνήθως με ένα τυποποιημένο εκχύλισμα, το WS1490. Οι καβαλακτόνες έχουν συσχετιστεί πιο στενά με τη δραστηριότητα του υποδοχέα GABAB που επηρεάζει το άγχος και τον μυϊκό τόνο, αλλά ένα σημαντικό τέτοιο συστατικό, η γιαγκονίνη (yangonin), έχει πρόσφατα δείξει σημαντική δραστηριότητα δέσμευσης του CB1 (Ki = 729nM, με 65,4% μετατόπιση του CP55940 στα 10mM και 98,4% στα 25mM)[19] (Εικόνα 1). Το εάν η γιαγκονίνη είναι αγωνιστής ή ανταγωνιστής CB1 είναι υπό τρέχουσα διερεύνηση. Δεν έδειξε σημαντική δέσμευση στον CB2 και άλλες καβαλακτόνες ήταν ανενεργές και στους δύο υποδοχείς. Δεδομένου ότι η γιαγκονίνη έχει λίγες υποχρεώσεις εκτός στόχου (αναστολή COX-2, 34% μετατόπιση μόνο σε υψηλή συγκέντρωση, 387mM[20]), αυτό το συστατικό αξίζει πρόσθετη μελέτη, ειδικά επειδή το γεγονός ότι η παραδοσιακή παρασκευή του kava μπορεί να αποφέρει 250–1250mg γιαγκονίνης ανά μερίδα, η οποία θεωρήθηκε ότι είναι φαρμακολογικά σημαντική (Alessia Ligresti, 2014, προσωπική επικοινωνία). Ασφαλώς, ενδείκνυται επιπρόσθετη μελέτη επιλεκτικά εκτρεφόμενων χημειοποικιλιών kava με υψηλότερη περιεκτικότητα σε γιαγκονίνη, μαζί με διερεύνηση διαφόρων μεθόδων εκχύλισης για μεγαλύτερη απόδοση.
Μια άλλη οικογένεια φυτών που παράγει πιθανούς κανναβιμιμητικούς υποκαταστάτες του CB1 είναι το ιαπωνικό μαρσαντιόφυτο (japanese liverwort), το Radula perrottetii, που παράγει το δομικό ανάλογο THC, το περοττετινένιο (perrottetinene)[21] και το μαρσαντιόφυτο της Νέας Ζηλανδίας, (New Zealand liverwort) το Radula marginata, που παράγει περοττετινενικό οξύ (perrottetinenic acid)[22] (Εικόνα 1). Αυτά τα ευρήματα έχουν πυροδοτήσει μια σειρά από “trip reports” στο διαδίκτυο από ερασιτέχνες ψυχοναύτες που τεκμηριώνουν ποικίλα εξέχοντα ψυχοδραστικά αντί για κανένα αποτέλεσμα μετά το κάπνισμα αυτών των παραγόντων. Ωστόσο, πρόσφατη πρόσθετη έρευνα επιβεβαιώνει την αγωνιστική δραστηριότητα στον CB1 (Jürg Gertsch, 2016, προσωπική επικοινωνία) που, ελπίζουμε, θα παρέχει σχετικό πλαίσιο για τη σχετική ισχύ και πιθανές θεραπευτικές δυνατότητες αυτού του βοτανικού παράγοντα.
Ένα Ν-βενζυλαμίδιο (N-benzylamide) από το Lepidium meyenii (Μάκα, βλέπε παρακάτω) δεσμεύεται στον CB1 (Ki = 480nM) (Εικόνα 1) χωρίς όμως αναφορά λειτουργικών επιδράσεων. Μόνο πρόσθετη έρευνα θα δείξει εάν αυτό το εύρημα έχει φαρμακολογική συνάφεια. Ένα Ν-μεθυλοβουταναμίδιο (N-methylbutanamide) από το Heliopsis helianthoides var. Scabra (ψευδής ηλίανθος) ήταν ακόμη πιο ισχυρό (Ki = 310nM) χωρίς παρατηρημένες επιδράσεις στην πρόσληψη AEA ή στην FAAH αναστολή[23], αλλά για άλλη μια φορά η κλινική εφαρμογή, εάν υπάρχει, μένει να καθοριστεί.
Κανναβιδιόλη και TRPV1 αγωνιστές / απευαισθητοποιητές και μιμητές
Η κανναβιδιόλη (CBD) είναι ένα μη μεθυστικό φυτοκανναβινοειδές που, αν και μετά βίας δεσμεύεται στις ορθοστερικές θέσεις CB1 και CB2[24], επιδεικνύει την ικανότητα να ανταγωνίζεται αυτούς τους υποδοχείς ακόμη και σε χαμηλές συγκεντρώσεις nM. Αυτή η ικανότητα αποδόθηκε πρόσφατα στην κατάστασή του ως αρνητικού αλλοστερικού διαμορφωτή στον CB1[25]. Παρόλο που αναφέρθηκαν ενώσεις που μοιάζουν με κανναβινοειδή με αντιφλεγμονώδη δράση από το λινάρι (Linum usitatissimum)[26], η CBD δεν έχει προσδιοριστεί οριστικά σε άλλα φυτά. Η CBD επιδεικνύει έναν εκπληκτικό αριθμό άλλων φαρμακολογικών στόχων ιατρικής σημασίας (ανασκόπηση[27]), συμπεριλαμβανομένης της ικανότητάς της, από κοινού με το AEA, ως αγωνιστής TRPV1[28] με EC50 3,2–3,5mM (Εικόνα 2), πολύ σύμφωνα με την αρχετυπική ουσία, την καψαϊκίνη από τις πιπεριές τσίλι (Capsicum annuum, μεταξύ άλλων) (Εικόνα 2). Ο αγωνιστής του TRPV1 είναι ένα χαρακτηριστικό που μοιράζεται με άλλα κοινά τρόφιμα, το τζίντζερ (Zingiber officinale), το μαύρο πιπέρι (Piper nigrum) και το λατέξ της βόρειας Αφρικής (Euphorbia resinifera) (Εικόνα 2)[29]. Η φερουγκινίνη Β (ferruginene B), από το αλπικό Rhododendron ferrugineum (Ροδόδενδρο το σιδηρόχρουν), έδειξε επίσης ασθενή δραστηριότητα TRPV1 (>20mM)[30], πιθανότατα αποκλείοντας τη φαρμακολογική συνάφεια.
Οι αγωνιστές TRPV1 εμπίπτουν σε δύο κατηγορίες, τις πικάντικες ή καυστικές ουσίες (καψαϊκίνη, πιπερίνη) και εκείνες που δεν είναι ερεθιστικές (CBD). Ενώ οι πρώτες ουσίες προκαλούν πόνο κατά την εφαρμογή, η συνεχής έκθεση σε αγωνιστές TRPV1 προκαλεί διαμορφωτική αλλαγή στον υποδοχέα και μια ανθεκτική κατάσταση λόγω απευαισθητοποίησης του υποδοχέα, καθιστώντας τους ως λειτουργικούς ανταγωνιστές κατά τη χρόνια εφαρμογή[31]. Αυτή η ταχυφυλαξία ή η φθίνουσα απόκριση μετά από επαναλαμβανόμενη έκθεση αντιπροσωπεύει μια μετάβαση από μια κατάσταση ανοιχτού σε κλειστό υποδοχέα[32]. Ιδανικά, ένας θεραπευτικός παράγοντας αυτής της κατηγορίας δεν θα προκαλούσε οξύ πόνο, αλλά θα απευαισθητοποιούσε τον υποδοχέα και θα παρουσίαζε μια ευνοϊκή αναλογία απευαισθητοποίησης / ερεθισμού[33]. Η CBD φαίνεται κατάλληλη και για τα δύο κριτήρια, καθώς, εκτός από την ισχύ της, απευαισθητοποιεί τον TRPV1 στα 10mM[28], δυνητικά “μειώνοντας τη θερμότητα και τον πόνο”[29]. Πιθανοί θεραπευτικοί στόχοι για την CBD ή παρόμοιους παράγοντες θα περιλαμβάνουν: νευροπαθητικό πόνο (αιτιολογία, σύνδρομο σύνθετου περιφερειακού πόνου, ημικρανία), εγκαύματα, ευερέθιστη κύστη, διάμεση κυστίτιδα, προστατίτιδα, χρόνιο πυελικό άλγος, ινομυαλγία, φλεγμονώδη νόσο του εντέρου, ερεθισμό του εντέρου και διάφορες δερματολογικές κνησμώδεις καταστάσεις.
Κανναβιγερόλη, ένα παραμελημένο φυτοκανναβινοειδές
Η κανναβιγερόλη είναι ένα “μικρό φυτοκανναβινοειδές” του οποίου ο πρόδρομος, το κανναβιγερολικό οξύ, είναι η μητρική ένωση της THC, της CBD και της κανναβιχρωμένης (ή κανναβιχρωμίνης), πριν από την αποκαρβοξυλίωση, αλλά κανονικά υπάρχει στην κάνναβη μόνο σε ίχνη, καθώς κανονικά διοχετεύεται γρήγορα στις κατάντη ουσίες[27]. Εμφανίζει συναρπαστική φαρμακολογία από μόνη της, συμπεριλαμβανομένης της αναστολής του GABA[34], των αντικαταθλιπτικών επιδράσεων σε τρωκτικά[35], τα εξέχοντα χημειοθεραπευτικά οφέλη[36], της αναστολής του πολλαπλασιασμού των κερατινοκυττάρων[37], των αντιβιοτικών επιδράσεων μεταξύ άλλων κατά του MRSA[38], α-2 αδρενεργικό αγωνισμό[39], αναστολή επαναπρόσληψης AEA[40] και ανταγωνισμός TRPM8[41]. Ενώ, η έρευνα και η θεραπευτική εφαρμογή αυτής της ουσίας έχουν παρεμποδιστεί από την απαγορευμένη κατάσταση σε ορισμένες χώρες όπως οι ΗΠΑ λόγω της συνήθους πηγής της, μια πιθανή εναλλακτική είναι παρούσα εδώ και δεκαετίες στο Helichrysum (Ελίχρυσο) umbraculigerum, ανθοφόρο φυτό της Νότιας Αφρικής που παράγει κανναβιγερόλη και κανναβιγερολικό οξύ στα εναέρια μέρη του[42]. Αυτό το είδος ήταν επομένως το πρώτο πέρα από την κάνναβη που αποδείχθηκε ότι φιλοξενεί φυτοκανναβινοειδή, αλλά, δυστυχώς, η αρχική δημοσίευση δεν έκανε καμία αναφορά σε σχετικές συγκεντρώσεις. Αυτό το θέμα βρίσκεται υπό τρέχουσα διερεύνηση. Ολόκληρο το γένος αξίζει πρόσθετη έρευνα, καθώς περιέχει πολυάριθμα μοναδικά φυτοχημικά[43], μερικά από τα οποία καπνίζονται από αυτόχθονες πληθυσμούς της Νότιας Αφρικής[44], υποδηλώνοντας ψυχοφαρμακολογικές επιδράσεις.

Εικόνα 1. Αγωνιστές CB1 με βάση φυτά.
(Όλες οι εικόνες: EBR, εκτός από το maca tuber, ευγενική προσφορά της Wikipedia: https://en.wikipedia.org/wiki/Lepidium_meyenii#/media/File:Maca.gif, public domain)
β-Καρυοφυλλένιο, ταυτόχρονα ένα σεσκιτερπενοειδές και ένα φυτοκανναβινοειδές
Το β-καρυοφυλλένιο είναι ένα σεσκιτερπενοειδές που είναι συχνά το πιο άφθονο τερπενοειδές στα εκχυλίσματα κάνναβης[27] (Εικόνα 3). Είναι γνωστό εδώ και πολύ καιρό για τις εξέχουσες αντιφλεγμονώδεις ιδιότητές του στην πειραματικά επαγόμενη ίνωση, συγκρίσιμο σε ισχύ με τη φαινυλβουταζόνη (phenylbutazone)[45], το μη στεροειδές αντιφλεγμονώδες φάρμακο (ΜΣΑΦ) της ιατρικής των ιπποειδών. Το καρυοφυλλένιο, σε αντίθεση με τα ΜΣΑΦ, είναι προστατευτικό της γαστρικής επένδυσης[46]. Πριν από περίπου μια δεκαετία, παρατηρήθηκε ότι το καρυοφυλλένιο είναι ένας εκλεκτικός πλήρης αγωνιστής (100nM) στον CB2[47], του οποίου η διατροφική πρόσληψη σε μόλις 4mg/kg/ημέρα μπορεί να το καταστήσει αποτελεσματικό αντιφλεγμονώδες[48]. Άλλες πιθανές εφαρμογές είναι στην legion, από κνησμό στη δερματίτιδα[49], έως την ίνωση στο ήπαρ, καρδιά, και άλλα όργανα[50]. Αυτό το δυναμικό είναι πιο πιθανό λαμβάνοντας υπόψη το γεγονός ότι το συγκεκριμένο φυτοκανναβινοειδές είναι ευρέως διαδεδομένο στα αιθέρια έλαια του φυτικού βασιλείου (Εικόνα 3), με τα βάλσαμα Copaiba spp. (έως 53,3%) να είναι η πλουσιότερη πηγή, αλλά περιλαμβάνεται επίσης σε μαύρο πιπέρι (P. nigrum) (έως 35%), σε βάλσαμο λεμονιού (Μελισσόχορτο, Melissa officinalis) (έως 19,1%), σε γαρίφαλο (Syzygium aromaticum) (έως 12,4% ) και σε λυκίσκο, τον πλησιέστερο βοτανικό συγγενή της κάνναβης (Humulus lupulus) (έως 9,8%)[51].
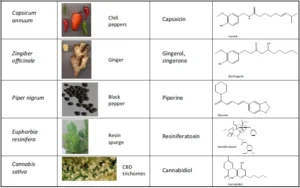
Εικόνα 2. Φυτικές πηγές δυνητικών αγωνιστών παροδικού υποδοχέα βανιλλοειδούς 1 (TRPV1).
(Όλες οι εικόνες: EBR.)
Πρόσθετοι παράγοντες CB2: Echinacea Alkamides και άλλα
Ορισμένα αλκυλαμίδια (“αλκαμίδια”) της Echinacea spp. (Εχινάκεια), που χρησιμοποιούνται για τη θεραπεία του κοινού κρυολογήματος και ως ενισχυτικά γενικής ανοσίας, παρατηρήθηκε ότι μοιάζουν με τις δομές των AEA και 2-AG[52]. Αυτό ώθησε τη διερεύνηση πρόσθετων δραστηριοτήτων αυτών των ενώσεων, συμπεριλαμβανομένης μιας 11-πλάσιας επαγωγής του παράγοντα νέκρωσης όγκου-άλφα (TNF-α), σε ανθρώπινα μονοκύτταρα και μακροφάγα ενώ ρυθμίζει προς τα πάνω την έκφραση του mRNA σε συγκεντρώσεις nM, με τη μεσολάβηση μέσω CB2, αλλά ακόμη και σε ανασταλτική πρωτεΐνη TNF-α που διεγείρεται από λιποπολυσακχαρίτες (LPS). Τα αλκαμίδια Echinacea κατέδειξαν επίσης αγωνιστική δράση CB2 (που μπλοκαρίστηκε από το SR144528) και την ικανότητα να ρυθμίζουν το κυκλικό AMP. Συνολικά, αυτές οι διπλές ανοσοτροποποιητικές δράσεις των αλκαμιδίων υπογραμμίζουν τον χαρακτηρισμό τους ως τα “ενεργά συστατικά” της Echinacea.
Η επακόλουθη έρευνα διευκρίνισε την αλληλεπίδραση αλκαμιδίου στον CB2[53], την ικανότητα αναστολής της επαναπρόσληψης AEA in vitro[54], τη δραστηριότητα στον υποδοχέα που ενεργοποιείται από πολλαπλασιαστή υπεροξισώματος (PPAR)-g, έναν πυρηνικό υποδοχέα[55], ως αγχολυτική δράση σε μοντέλα ζώων[56] και επιδράσεις μερικού και αντίστροφου αγωνιστή στον CB1[57]. Η τελευταία δραστηριότητα θα μπορούσε να υποδηλώνει πιθανά οφέλη για το μεταβολικό σύνδρομο, αλλά και πιθανές ανεπιθύμητες ενέργειες λόγω άγχους, κατάθλιψης και άλλων συνεπειών[58]. Είναι πολύ πιθανό αυτός ο ιθαγενής Αμερικανός φυτικός παράγοντας να δει πολύ ευρύτερη κλινική εφαρμογή στο μέλλον, καθώς αυτά Τα υπόλοιπα ζητήματα ταξινομούνται και αντιμετωπίζονται.
Οι αρχικές αναφορές υποστήριζαν ότι η επιγαλλοκατεχίνη 4-γαλλική (epigallocatechin 4-gallate) και (–)-επιγαλλοκατεχίνη ((–)-epigallocatechin) στο πράσινο τσάι (Camellia sinensis) δέσμευαν τον CB2 σε υψηλές συγκεντρώσεις[59], αλλά αυτό το εύρημα στη συνέχεια αμφισβητήθηκε[60]. Η φερουγκινίνη C (ferruginene C), ένα μείγμα ισομερών από το R. Ferrugineum (Ροδόδενδρο το σιδηρόχρουν), έδειξε ασθενή δράση CB2 και IC50 13,7mM για κυτταροτοξικές επιδράσεις στα ανθρώπινα κύτταρα προμυελοκυτταρικής λευχαιμίας HL-60[30].

Εικόνα 3. β-Καρυοφυλλένιο, ένας αγωνιστής CB2, και οι πηγές αιθέριων ελαίων του. (A) μόριο β-καρυοφυλλενίου. (B) μη γονιμοποιημένο θηλυκό λουλούδι, Cannabis sativa. (C) βάλσαμο copaiba από την Copaifera officinalis. (D) κόκκοι πιπεριού, Piper nigrum. (E) βάλσαμο λεμονιού, Melissa officinalis. (F) γαρίφαλο, Syzygium aromaticum, (G) λυκίσκος, Humulus lupulus.
(Όλες οι εικόνες: EBR.)
Φυτικοί αναστολείς της υδρολάσης αμιδίου λιπαρών οξέων
Το Kaempferia galanga, ή galanga (Κενσούρ), είναι συγγενές του τζίντζερ, του οποίου τα ριζώματα παράγουν ένα φλαβονοειδές, την καμπφερόλη (kaempferol), που βρίσκεται επίσης στα μήλα, τα βατόμουρα και πολλά άλλα φυτά. Η καμπφερόλη αποδείχθηκε ότι είναι αναστολέας του FAAH, της υδρολάσης της σερίνης που διασπά το ΑΕΑ (Ki=5mM) [61] (Εικόνα 4). Είναι πιθανό ότι η υψηλή διατροφική πρόσληψη αυτής της ουσίας θα μπορούσε να ενισχύσει τα επίπεδα AEA στον ορό.
Η μάκα (maca, L. meyenii) είναι ένας συγγενής του ραπανιού και τροφή των υψηλών Άνδεων, που μερικές φορές αποκαλείται “περουβιανό τζίνσενγκ” για τη χρήση του ως προσαρμογόνο, περιέχει Ν-βενζυλαμίδια λιπαρών οξέων μακράς αλυσίδας που ονομάζονται “μακαμίδια”[62], δύο από τα οποία έδειξαν αναστρέψιμη αναστολή FAAH στα 10mM (Εικόνα 4). Θεωρήθηκε ότι η δομή αυτών των φυσικών ενώσεων θα επέτρεπε τη διέλευση μέσω του αιματοεγκεφαλικού φραγμού και ότι παρά τη χαμηλή τους ισχύ, η τακτική κατανάλωση θα μπορούσε να προκαλέσει αλλαγές στη σηματοδότηση αμιδίου στο ΚΝΣ, αλλά αυτό μένει να καθοριστεί. Ομοίως, ένα Ν-βενζυλαμίδιο του ίδιου είδους ήταν ένας αναστολέας FAAH (IC50 = 4mM) και αναστολέας της πρόσληψης AEA (IC50 = 670nM), που χαρακτηρίστηκε “μίμηση υποστρώματος ενδοκανναβινοειδούς”[23]. Ένα σχετικό Ν-μεθυλοβουταναμίδιο έδειξε ασθενή αναστολή FAAH.
Σε αντίθεση με τη δημοφιλή πεποίθηση, δεν υπάρχουν ενδοκανναβινοειδή στη σοκολάτα, που προέρχονται από το Theobroma cacao (Κακαόδεντρο), αλλά περιέχει Ν-λινελαιοαιθανολαμίδιο (N-linoleoylethanolamide) και Ν-ελαιολαιθανολαμίδιο (N-oleoylethanolamide)[63], τα οποία παράγουν αναστολή FAAH[64] (Εικόνα 4).

Εικόνα 4. Φυτικές πηγές Αναστολής υδρολάσης αμιδίου λιπαρών οξέων (FAAH).
(Όλες οι εικόνες: EBR.)
Πρεβιοτικά και προβιοτικά
Ενώ τα βακτήρια θεωρούνται πλέον ότι αξίζουν έναν δικό τους ταξινομικό τομέα και ονομάζονται σωστά μικροβίωμα (microbiota), παρά μικροχλωρίδα (microflora), αυτά που κατοικούν στο ανθρώπινο έντερο έχουν μια έμφυτη σχέση με το ΕΚΣ και, για αυτόν τον λόγο, ο συγγραφέας θα ήθελε να επιστήσει την προσοχή σχετικά με το ζήτημα και τον τρόπο με τον οποίο τα διαιτητικά φυτά μπορούν να ρυθμίσουν την ανάπτυξη και τα αποτελέσματά τους.
Τα ωφέλιμα βακτήρια στο έντερο μπορούν να χορηγηθούν ως από του στόματος συμπληρώματα που ονομάζονται προβιοτικά. Ένα τέτοιο στέλεχος, το Lactobacillus acidophilus NCFM προκάλεσε έκφραση mRNA CNR2 σε ανθρώπινα επιθηλιακά κύτταρα HT-29 (P <0,01), μαζί με ανακούφιση από τον πόνο σε αρουραίους (P <0,001) που μειώθηκε από τον CB2 ανταγωνισμό, AM-630 (Ρ < 0,001)[65]. Μια ανάλυση προβιοτικών σε ανθρώπους για τη θεραπεία του συνδρόμου ευερέθιστου εντέρου έδειξε όφελος στα συμπτώματα σε 34 από τις 42 κλινικές δοκιμές[66]. Πρόσθετες ενδείξεις για τη σχέση του “άξονα μικροβιώματος-έντερου-εγκεφάλου” υποστηρίζονται από την ικανότητα της THC να επηρεάζει τη βακτηριακή αναλογία Firmicutes:Bacteroidetes (P = 0,021) και την αύξηση βάρους στα τρωκτικά παρά τη δίαιτα με υψηλή περιεκτικότητα σε λιπαρά[67]. Η βέλτιστη διατήρηση του εντερικού μικροβιώματος ενισχύεται με τη διατροφική πρόσληψη ή τη συμπλήρωση με πρεβιοτικά, είδη βλάστησης πλούσια σε ινουλίνη (inulin) και φρουκτοολιγοσακχαρίτες (fructooligosaccharides, FOS), που αντιστέκονται στο γαστρικό οξύ και διεγείρουν την υγεία και την ανάπτυξη ωφέλιμων βακτηρίων που τα χρησιμοποιούν ως υποστρώματα ζύμωσης[68]. Τέτοια λαχανικά, ιδίως οι ίνες ακακίας (αραβικό κόμμι), η ρίζα κιχωρίου, η κολλιτσίδα, οι λιακάδες, τα χόρτα πικραλίδας, τα κρεμμύδια, το σκόρδο και τα πράσα (Εικόνα 5), αναφέρεται ότι βοηθούν στην πρόληψη της λοιμώδους διάρροιας, στη μείωση των συμπτωμάτων της φλεγμονώδους νόσου του εντέρου και στον κίνδυνο καρκίνου, στην απορρόφηση μετάλλων και μείωση της παχυσαρκίας[68]. Μια επίσημη μελέτη για τις ίνες Acacia senegal (Σενεγαλία) σε 54 υγιείς εθελοντές για 4 εβδομάδες έδειξε ότι η πρόσληψη 10g/ημέρα ήταν η βέλτιστη για την αύξηση του αριθμού των Bifidobacteria 40 φορές έναντι του νερού (P <0,01) και 10 φορές έναντι της ινουλίνης (P <0,05)[69]. Επιπλέον, οι λακτοβάκιλλοι αυξήθηκαν 6 φορές έναντι νερού (P < 0,05) και 7 φορές σε σχέση με τις θεραπείες ινουλίνης (P <0,03). Το παθογόνο του παχέος εντέρου, Clostridium difficile, μειώθηκε επίσης σημαντικά (P <0,01).
Είναι ολοένα και πιο προφανές ότι οι σωστές διατροφικές επιλογές που περιλαμβάνουν πρεβιοτικά λαχανικά και τρόφιμα που έχουν υποστεί ζύμωση μπορεί να διαδραματίσουν σημαντικό ρόλο σε μελλοντικές θεραπείες που στοχεύουν το ΕΚΣ.
Διάφορα και κάποια άλλα φυτά που επηρεάζουν το ΕΚΣ
Ένα άλλο φυτό που εξετάστηκε για πιθανή δράση κανναβινοειδών ήταν το Columnea ericae (Dalbergia picta), ένα επίφυτο gesneriad του Αμαζονίου που καπνίζουν οι αυτόχθονες πληθυσμοί Siona-Secoya όπως το ταμπάκο[70] (Εικόνα 6). Το φυτό εμφάνισε κάποια δραστηριότητα υποδοχέα σεροτονίνης 2Α, ενώ καμία δεν εμφανίστηκε στον CB1[12].

Εικόνα 5. Συστοιχία Πρεβιοτικών Φυτών. (A) Αραβικό κόμμι, Ακακία Σενεγάλης, (B) Ρίζα κιχωρίου, Cichorium intybus, (C) Σουντσούκ (αγκινάρες Ιερουσαλήμ), Helianthus tuberosus, (D) Χόρτα πικραλίδας, Taraxacum officinale, (E) Κολιτσίδα, Arctium lappa, (F) Πράσο, Allium ampeloprasum, Σκόρδο, Allium sativum και Κρεμμύδι, Allium cepa.
(Όλες οι εικόνες: EBR.)
Η κουρκουμίνη, ένα συστατικό του κοινού μπαχαρικού, του κουρκουμά, από το Curcuma longa, αναφέρθηκε προηγουμένως ότι είναι ένας υψηλής δραστικότητας αντίστροφος αγωνιστής στον CB1 παρόμοιος με το συνθετικό rimonabant (SR141716A)[71], αλλά αυτό το έγγραφο στη συνέχεια ανακλήθηκε[72]. Αυτός ο παράγοντας επανεξετάστηκε[60] και βρέθηκε ότι δεσμεύεται μόνο σε πολύ υψηλές συγκεντρώσεις mM (Εικόνα 6), θέτοντας υπό αμφισβήτηση εάν η διατροφική πρόσληψη θα ήταν επαρκής για να προκαλέσει ένα τέτοιο αποτέλεσμα.
Ορισμένες διαμάχες περιβάλλουν την πιθανή δράση στο ΕΚΣ των αμυρινών, των πεντακυκλικών τριτερπενίων από το Protium heptaphyllum. Η αρχική αναφορά[73] έδειξε ότι οι δόσεις 30mg/kg μείωσαν τη φλεγμονή και την υπεραλγησία μετά από απολίνωση του ισχιακού νεύρου ποντικού. Λέγεται ότι τα αποτελέσματα αντιστράφηκαν και από τους ανταγωνιστές CB1 και CB2, αν και οι σταθερές διάστασης ήταν διαφορετικές, Ki = 1989nM για τον CB2 και Ki = 0,13nM για τον CB1, και δεν ήταν εμφανή αποτελέσματα συμπεριφοράς στην κανναβινοειδή τετράδα. Η επακόλουθη έρευνα από μια άλλη πολύ έμπειρη ομάδα[74], αντίθετα, δεν έδειξε δέσμευση σε κανέναν από τους δύο υποδοχείς αλλά, μάλλον, μια ισχυρή αναστολή της υδρόλυσης 2-AG.
Το λιβάνι, Boswellia carterii, εμφανίζει στον άνθρωπο ιδιότητες που μοιάζουν με αυτές της κάνναβης (την κανναβινοειδή τετράδα της αναλγησίας, της υποθερμίας, της καταληψίας, της υποκινητικότητας), καθώς και αντιφλεγμονώδη, αντιοξειδωτικά και αντισηπτικά αποτελέσματα[75]. Μεταγενέστερες έρευνες κατέδειξαν ισχυρό συναγωνισμό του συστατικού του, οξικού θυμιάματος, στο TRPV3, που προκαλεί συναισθήματα ή ζεστασιά στο δέρμα και το μυαλό, αγχολυτικά και αντικαταθλιπτικά αποτελέσματα, καθώς και ενεργοποίηση πρωτο-ογκογονιδίου c-Fos[76] και πυρηνικό παράγοντα κάπα Β (NF -kB) αναστολή με νευροπροστατευτικά αποτελέσματα μετά από εγκεφαλικό τραύμα σε ποντίκια[77] (Εικόνα 6).

Εικόνα 6. Διάφορα χτυπήματα και αστοχίες φυτών που επηρεάζουν το ενδοκανναβινοειδές σύστημα.
(Όλες οι εικόνες: EBR.)
Πέρα από το καρυοφυλλένιο και τον συναγωνισμό του CB2, το μαύρο πιπέρι ρυθμίζει επίσης το ΕΚΣ μέσω του n-ισοβουτυλαμιδίου (n-isobutylamide), γουινενσίνη (guineensine)[78] (Εικόνα 6), η οποία ανέστειλε την πρόσληψη του ΑΕΑ ανάλογα με τη δόση (EC50 = 290nM) χωρίς σημαντική επίδραση στο FAAG, στα κανναβινοειδή, στους MAG υποδοχείς ή στην πρωτεΐνη που δεσμεύει λιπαρά οξέα 5. Εμφάνισε κανναβιμιμητικά αποτελέσματα σε ποντίκια BALB/c σε 2,5–10mg/kg μεγαλύτερα από το εικονικό φάρμακο (P < 0,001) και με σχετιζόμενες τετραδικές επιδράσεις.
Παρατήρησα μεγάλη επικάλυψη στα αναφερόμενα οφέλη του δημοφιλούς προσαρμογόνου, Rhodiola rosea (Ροδιόλα η ροδόχρους), σε σύγκριση με την CBD, συμπεριλαμβανομένης της αυξημένης εγρήγορσης, της μειωμένης κατάθλιψης, του άγχους, μεταξύ άλλων, υποδεικνύοντας το ως υποτιθέμενο διαμορφωτή ΕΚΣ. Η επακόλουθη ανάλυση[79], που πραγματοποιήθηκε από την Alessia Ligresti το 2014, απέτυχε να καταδείξει σημαντική δέσμευση ή μετατόπιση CB1 ή CB2, ούτε αναστολή FAAH δύο υποτιθέμενων βασικών συστατικών, της ροζαβίνης (rosavin) και της σαλιδροζίδης (salidroside) (Εικόνα 6).
Τέλος, μια πρόσφατη έρευνα ανέφερε την παρουσία ενδοκανναβινοειδών βιοσυνθετικών και καταβολικών ενζύμων και AEA, αλλά όχι υποδοχείς 2-AG ούτε κανναβινοειδών, σε μαύρες τρούφες, Tuber melanosporum[80] (Εικόνα 6). Η συγκέντρωση AEA αυξήθηκε pari passu με την ανάπτυξη μελάγχρωσης μελανίνης στις τρούφες, φτάνοντας σε συγκέντρωση 300-400nM που θεωρήθηκε επαρκής για την ενεργοποίηση των CB1 και CB2. Δύο συνέπειες, μεταξύ πολλών από αυτό το έργο, θα ήταν μια εξήγηση γιατί οι τρούφες είναι τόσο ακριβές και η απόδειξη ότι οι μύκητες είναι περισσότερο ζωικοί παρά φυτικοί. Vegans προσοχή!
Πέρα από το χιούμορ, είναι σαφές ότι τα ενδοκανναβινοειδή αποτελούν ένα υποσύνολο των Ν-ακυλαιθανολαμινών[81], που είναι ευρέως διαδεδομένες στα φυτά και ότι μένει να μάθουμε πολλά σχετικά με τις πιθανές φαρμακολογικές επιδράσεις τους στη σηματοδότηση των κυττάρων που μπορεί να έχουν σημαντικές επιπτώσεις όχι μόνο για ανάπτυξη και ανάπτυξη των φυτών αλλά και για την ανθρώπινη υγεία. Η αναζήτηση συνεχίζεται.
Τελικές παρατηρήσεις
Αυτή η ανασκόπηση εξέτασε εν συντομία διάφορα συστατικά του ΕΚΣ και πώς μπορεί να επηρεαστούν από κοινά τρόφιμα και φαρμακευτικά φυτά. Μαζί με άλλους παράγοντες του τρόπου ζωής, όπως η αερόβια άσκηση, οι διατροφικές προσαρμογές και τα συμπληρώματα μπορεί να αποτελέσουν σημαντικές στρατηγικές σε αυτό που εύστοχα ονομάζεται “φροντίδα και σίτιση του ενδοκανναβινοειδούς συστήματος”[4]. Η διερεύνηση άλλων φυτών που δρουν στο ΕΚΣ θα πρέπει να προχωρήσει (βλ. στο Εκκρεμείς ερωτήσεις), με έρευνα για ιδιαίτερα υποσχόμενους υποψηφίους μεταξύ των βοτάνων που παράγουν τερπενοειδή και άλλων φυτών που φέρουν αδενικά τριχώματα, παράγουν λιπίδια ή λατέξ. Τα υποψήφια γένη και οι οικογένειες μπορεί να περιλαμβάνουν τα: Salvia, Piper, Rutaceae (εσπεριδοειδή), Radula και άλλα liverworts, Helichrysum και Zingiberaceae (η μεγαλύτερη οικογένεια Ginger). Πέρα από τις έρευνες άμεσης δραστηριότητας στους CB1, CB2 και TRPV1, η εστίαση θα πρέπει επίσης να επεκταθεί στην αλλοστερική διαμόρφωση των υποδοχέων, στην αναστολή FAAH και MAGL, ακόμη και σε πιθανές ρυθμιστικές επιδράσεις στα υποτιθέμενα μόρια μεταφορέα ενδοκανναβινοειδών.
Δεδομένου ότι η κάνναβη είναι μια τέτοια δεξαμενή δυνητικά θεραπευτικών συστατικών από μόνη της[27], θα μπορούσε κανείς να αμφισβητήσει την ανάγκη επέκτασης της έρευνας σε άλλα φυτά, αλλά αυτό θα ήταν κοντόφθαλμο. Σίγουρα, εάν τα κοινά τρόφιμα ρυθμίζουν το ΕΚΣ, το πώς και το γιατί αυτών των μηχανισμών αξίζει διερεύνησης, ώστε να διευκρινιστούν οι συνεισφορές και οι παγίδες τους. Ίσως μια τέτοια έρευνα μπορεί να αποκαλύψει μόρια που υποδεικνύουν πρόσθετους υποτύπους υποδοχέων κανναβινοειδών ή που προσφέρουν φαρμακολογικό πλεονέκτημα με λιγότερες παρενέργειες, όπως θεραπεία νευροπαθητικού πόνου χωρίς συνακόλουθη ψυχοδραστηριότητα, όπως θα μπορούσε να γίνει αντιληπτό από φυτά που παράγουν καρυοφυλλένιο (βλ. παραπάνω).
Πολλά σημαντικά ερωτήματα παραμένουν. Πρώτον, γιατί χρειάστηκε τόσος καιρός για να ανακαλύψουμε το ΕΚΣ και τα φυτά που το επηρεάζουν και γιατί είναι σχετικά σπάνια μέχρι σήμερα; Οι παράγοντες είναι πολλαπλοί και το ιστορικό πλαίσιο διαφωτιστικό. Ενώ η μορφίνη, ένα αλκαλοειδές, αναγνωρίστηκε για πρώτη φορά το 1806, παρά τις καλύτερες προσπάθειες πολλών επιστημόνων, οι πραγματικές δομές της THC και της CBD δεν ανακαλύφθηκαν για άλλα 150 χρόνια. Αντίστοιχα, το ενδογενές σύστημα οπιοειδών, οι ενδορφίνες και οι εγκεφαλίνες (απλά πεπτίδια) ανακαλύφθηκαν τη δεκαετία του ‘70, ενώ σχεδόν άλλες δύο δεκαετίες χρειάστηκαν για τον προσδιορισμό των συστατικών και της φυσιολογίας των ενδοκανναβινοειδών και άλλων συστατικών του ΕΚΣ. Εν ολίγοις, αυτά τα “κολλώδη” λιπόφιλα κανναβινοειδή ήταν πολύ πιο δύσκολο στην έρευνα, και μόνο τώρα, στην επόμενη γενιά, η προσοχή στράφηκε σε φυτά πέρα από την κάνναβη που μπορεί επίσης να ρυθμίσουν το σύστημα. Καλώς ή κακώς, η φαρμακολογική έρευνα είναι δαπανηρή, η χρηματοδότηση είναι άπιαστη και τα ζητήματα πνευματικής ιδιοκτησίας υπαγορεύουν ότι οι εταιρείες θα προτιμούσαν τις περισσότερες φορές να κατασκευάσουν ένα μόριο de novo έχοντας κατά νου έναν συγκεκριμένο στόχο υποδοχέα αντί να ερευνήσουν φυσικές ενώσεις από ένα βοτανικό που μπορεί να είναι ελεύθερα διατίθεται στη φύση και δεν υπάρχει δυνατότητα προστασίας με δίπλωμα ευρεσιτεχνίας. Όταν οι εμπλεκόμενες ουσίες μπορεί επίσης να περιλαμβάνουν δυνητικά απαγορευμένες ουσίες που μοιάζουν με THC, οι οποίες υπόκεινται σε ρυθμιστικό προγραμματισμό, τα εμπόδια στην έρευνα γίνονται ακόμη μεγαλύτερα. Μπορεί κανείς να αναρωτηθεί, ωστόσο, πόσος επιπλέον χρόνος μπορεί να χρειαζόταν για να ανακαλύψει κανείς ότι το ΕΚΣ δεν ήταν εκεί η κάνναβη για να πρωτοστατήσει. Παρά τη φαινομενική πανταχού παρουσία του και την προφανή σημασία του ως ομοιοστατικού ρυθμιστή της ανθρώπινης φυσιολογίας, το θέμα του ΕΚΣ λαμβάνει σύντομη αλλαγή στη σύγχρονη ιατρική εκπαίδευση, αν αναφέρεται και καθόλου. Αυτό το εκπαιδευτικό έλλειμμα, που γεννήθηκε ίσως από παρατεταμένη προκατάληψη απέναντι σε ένα φυτό που ονομάζεται κάνναβη, πρέπει σίγουρα να τελειώσει σύντομα, καθώς είναι αντίθετο και επιζήμιο για πιθανές σημαντικές συνεισφορές στη δημόσια υγεία.
Πέρα από τα εμπόδια, αυτή η έρευνα για τα φυτά που επηρεάζουν το ΕΚΣ προμηνύεται ότι θα οδηγήσει σε σημαντικές προόδους στον τόνο των ενδοκανναβινοειδών, καθώς και σε καλύτερη κατανόηση της περίπλοκης θέσης των οικολογικών ρόλων των φυτοχημικών και των αλληλεπιδράσεών τους με τη δική μας βιοχημεία και παθοφυσιολογικούς μηχανισμούς.
Ευχαριστίες
Ο συγγραφέας εκτιμά πολύ τον εκδότη και τους κριτικούς ενδιαφέρουσες ερωτήσεις και συναρπαστικές προτάσεις που συνέβαλαν σημαντικά σε αυτήν την ανασκόπηση.
Γλωσσάριο
Προσαρμογόνο: ένας βοτανικός παράγοντας που προάγει την ομοιόσταση, ανακουφίζει από την κόπωση, το άγχος και την αγωνία και βελτιώνει τις καθημερινές λειτουργίες χωρίς να προκαλεί εμφανή ανεπιθύμητα συμβάντα.
Αλλοστερικός διαμορφωτής: ένας παράγοντας που δεσμεύεται σε ξεχωριστή θέση σε έναν υποδοχέα από την κύρια (ορθοστερική) θέση που μεταβάλλει τις δεσμευτικές του ιδιότητες. Το αποτέλεσμα μπορεί να αυξήσει (θετικός αλλοστερικός διαμορφωτής, PAM) ή να μειώσει (αρνητικός αλλοστερικός διαμορφωτής, ΝΑΜ) τις ιδιότητες δέσμευσης.
Ανανδαμίδιο (αραχιδονυλαιθανολαμίδιο, ΑΕΑ): είναι ένας ενδογενής συνδέτης για τον υποδοχέα CB1, από το Ananda, τη σανσκριτική λέξη για την “ευδαιμονία”.
2-Αραχιδονοϋλογλυκερόλη (2-AG): ένα ενδοκανναβινοειδές που είναι πλήρης αγωνιστής στους υποδοχείς CB1 και CB2.
Κανναβιμιμητικό: ουσία που μιμείται τις επιδράσεις της κάνναβης ή ενός κανναβινοειδούς.
Κανναβινοειδή: είναι τριών τύπων, τα φυτοκανναβινοειδή που είναι χημικές ουσίες φυτικής προέλευσης στην κάνναβη και σπάνια σε άλλα φυτά, τα ενδοκανναβινοειδή που είναι ενδογενείς χημικές ουσίες σε χορδές που δεσμεύουν τους υποδοχείς κανναβινοειδών, ενώ τα συνθετικά κανναβινοειδή αναπτύχθηκαν για να αλληλεπιδρούν με αυτά τα συστήματα.
Κανναβινοειδείς υποδοχείς: Υποδοχείς συζευγμένοι με G-πρωτεΐνη όπου δεσμεύεται το ένα ή το άλλο από THC, ανανδαμίδιο και 2-AG. Οι πιο γνωστοί είναι ο CB1, ο ψυχοδραστικός, νευροτροποποιητικός και αναλγητικός υποδοχέας, και ο CB2, ένας αντιφλεγμονώδης ανοσοτροποποιητικός υποδοχέας, αλλά και ο TRPV1, ο ιοντοτροπικός υποδοχέας κανναβινοειδών για την καψαϊκίνη που ρυθμίζει τις αντιδράσεις της θερμοκρασίας και του πόνου.
Κανναβινοειδής τετράδα: ένα σύνολο τεσσάρων ενδείξεων σε πειράματα σε ζώα ότι μια ουσία διεγείρει τον CB1: υποκινητικότητα, καταληψία, αναλγησία και υποθερμία.
Απευαισθητοποίηση: όταν η συνεχής παρουσία ενός αγωνιστή στον υποδοχέα μειώνει τα αποτελέσματά του και γίνεται λειτουργικά ανταγωνιστής.
Ενδοκανναβινοειδής τόνος: η κατάσταση του ΕΚΣ ενός ατόμου με βάση τα επίπεδα AEA και 2-AG στον ορό ή τους ιστούς, την πυκνότητα των υποδοχέων κανναβινοειδών και τη διαθεσιμότητα της καταβολικής ενζυματικής δραστηριότητας FAAH και MAGL.
Υδρολάση αμιδίου λιπαρού οξέος (FAAH): ένζυμο που συνδέεται με τη μεμβράνη που διασπά το AEA σε αιθανολαμίνη και αραχιδονικό οξύ. Διάφορες ενώσεις μπορεί να αναστείλουν το FAAH και να αυξήσουν τα επίπεδα AEA, αυξάνοντας έτσι τον “ενδοκανναβινοειδή τόνο”.
Φρουκτοολιγοσακχαρίτες (FOS): σύνθετα πολυμερή φυτικής ζάχαρης, η προτιμώμενη πρώτη ύλη για τα ωφέλιμα εντερικά βακτήρια.
Γενετικά τροποποιημένος οργανισμός (ΓΤΟ): φυτό ή ζώο που έχει τροποποιηθεί ο γενετικός του κώδικας ή που φιλοξενεί DNA που έχει μεταφερθεί από άλλο οργανισμό.
Ομοιόσταση: μια κατάσταση φυσικής φυσιολογικής ισορροπίας στην οποία δεν υπάρχει ούτε περίσσεια ούτε έλλειμμα δραστηριότητας.
Μονοακυλογλυκερολλιπάση (MAGL): ένζυμο που διασπά την 2-AG. Οι αναστολείς της δράσης του μπορεί να ενισχύσουν ή να παρατείνουν τα αποτελέσματά του.
Πρεβιοτικό: φυτική τροφή, συνήθως πλούσια σε ινουλίνη ή/και φρουκτοολιγοσακχαρίτες, που προάγει τα ωφέλιμα εντερικά βακτήρια.
Προβιοτικό: τρόφιμο (ξινολάχανο, γιαούρτι, κεφίρ) ή συμπλήρωμα διατροφής που προμηθεύει ωφέλιμα βακτήρια (Bifidobacteria, Lactobacilli) στο κόλον.
Τερπενοειδή: τα πιο κοινά φυτικά χημικά. Τα μονοτερπενοειδή έχουν 10 άνθρακες, τα σεσκιτερπενοειδή 15, τα διτερπενοειδή 20, τα τριτερπενοειδή, 30 και ούτω καθεξής, συχνά υπεύθυνα για την οσμή, τη γεύση και τις φαρμακευτικές επιδράσεις.
Βανιλλοειδές δυναμικού παροδικού υποδοχέα 1 (TRPV1): κανάλι διαμεμβρανικού υποδοχέα που ενεργοποιείται από θερμότητα, οξύ, αιθανόλη και ΑΕΑ. το σημείο όπου δραστηριοποιείται η καψαϊκίνη, το πικάντικο συστατικό της πιπεριάς τσίλι.
Εκκρεμείς ερωτήσεις
*Θα πρέπει τα φυτά που εκφράζουν αγωνιστική δραστηριότητα CB1 να υποστούν νομικό έλεγχο ως πιθανά φάρμακα κατάχρησης;
* Μπορούν οι φυτικοί αγωνιστές TRPV1 και άλλα διατροφικά συστατικά να απευαισθητοποιήσουν τον υποδοχέα και να ρυθμίσουν τα σύνδρομα πόνου και άλλες διαταραχές;
* Πρέπει τα άτομα με χρόνιο πόνο ή αρθρίτιδα να προσπαθήσουν να αυξήσουν τη διατροφική τους πρόσληψη σε βήτα-καρυοφυλλένιο σε μια προσπάθεια να θεραπεύσουν την κατάστασή τους;
* Μπορεί η Echinacea να χρησιμοποιηθεί για τη θεραπεία καταστάσεων πέρα από το κοινό κρυολόγημα, όπως αυτοάνοσα νοσήματα ή παχυσαρκία/ μεταβολικό σύνδρομο;
* Μπορούν τα τερπενοειδή στην κάνναβη ή από άλλες πηγές να δράσουν ως θετικοί ή αρνητικοί αλλοστερικοί ρυθμιστές σε υποδοχείς κάνναβης ή σε άλλους υποδοχείς;
* Μπορεί η διατροφή μας να επηρεάσει σημαντικά τα επίπεδα AEA και 2-AG, αυξάνοντας έτσι τον τόνο ενδοκανναβινοειδών;
* Μπορούν να αναπτυχθούν διατροφικές οδηγίες για τη βελτιστοποίηση της λειτουργίας του ΕΚΣ; Ποιος είναι ο ρόλος των προβιοτικών σε αυτή την προσπάθεια; Και τα πρεβιοτικά;
* Μπορούν τα πρεβιοτικά και τα προβιοτικά να επιδεικνύονται για τη ρύθμιση των επιπέδων ενδοκανναβινοειδών στον ορό και τον εγκέφαλο;
* Μπορούν να αποδειχθούν προσαρμογόνα (πχ. R. rosea, Panax ginseng, Eleuthero senticosus, μεταξύ άλλων) ότι ρυθμίζουν το ΕΚΣ με τακτική χρήση;
* Μπορούν οι χοίροι ή οι σκύλοι να αναγνωρίσουν το ΑΕΑ στο άρωμα της τρούφας και μπορεί αυτό να επηρεάσει τον ενθουσιασμό τους για το κυνήγι καθώς το αναζητούν επιλεκτικά;
* Εκφράζουν επίσης ανανδαμίδιο κατά την ανάπτυξή τους άλλοι μύκητες με σκούρα χρωματισμό (πχ. μορέλ, Morchella spp.);
* Θα αποδώσουν άλλα είδη φυτών πολύτιμους ρυθμιστές ΕΚΣ;
* Μπορούν τα φυτοχημικά να επηρεάσουν τη λειτουργία του υποτιθέμενου μεταφορέα ανανδαμιδίου;
* Θα βοηθήσει η γνώση των επιπτώσεων στο ΕΚΣ φυτών εκτός της κάνναβης να μετριάσει την πόλωση απόψεις για την ιατρική με βάση την κάνναβη;
Βιβλιογραφικές αναφορές
- [1]. Pacher, P. and Kunos, G. (2013) Modulating the endocannabinoid system in human health and disease–successes and failures. FEBS J. 280, 1918–1943
- [2]. Russo, E. B. et al. (2015) Current status and future of cannabis research. Clin. Res. 58–63 April
- [3]. Maccarrone, M. et al. (2015) Endocannabinoid signaling at the periphery: 50 years after THC. Trends Pharmacol. Sci. 36,277–296
- [4]. McPartland, J. M. et al. (2014) Care and feeding of the endocannabinoid system: a systematic review of potential clinical interventions that upregulate the endocannabinoid system. PLoS ONE 9, e89566
- [5]. Russo, E. B. (2004) Clinical endocannabinoid deficiency (CECD): can this concept explain therapeutic benefits of cannabis in migraine, fibromyalgia, irritable bowel syndrome and other treatment-resistant conditions? Neuroendocrinol. Lett. 25, 31–39
- [6]. Devane, W. A. et al. (1988) Determination and characterization of a cannabinoid receptor in rat brain. Mol. Pharmacol. 34, 605–613
- [7]. Glass, M. et al. (1997) Cannabinoid receptors in the human brain: a detailed anatomical and quantitative autoradiographic study in the fetal, neonatal and adult human brain. Neuroscience 77, 299–318
- [8]. Di Marzo, V. (1998) ‘Endocannabinoids’ and other fatty acid derivatives with cannabimimetic properties: biochemistry and possible physiopathological relevance. Biochim. Biophys. Acta 1392, 153–175
- [9]. Taura, F. et al. (2007) Phytocannabinoid sin Cannabis sativa: recent studies on biosynthetic enzymes. Chem. Biodivers. 4, 1649–1663
- [10]. Zirpel, B. et al. (2015) Production of Delta9-tetrahydrocannabinolic acid from cannabigerolic acid by whole cells of Pichia (Komagataella) pastoris expressing Delta9-tetrahydrocannabinolic acid synthase from Cannabis sativa L. Biotechnol. Lett. 37, 1869–1875
- [11]. Siebert, D. J. (1994) Salvia divinorum and salvinorin A: newpharmacologic findings. J. Ethnopharmacol. 43, 53–56
- [12]. Russo, E. et al. (2002) In search of plants, other than Cannabis sativa, with cannabinoid receptor activity. In In Symposium on the Cannabinoids. International Cannabinoid Research Society, p. 46
- [13]. Roth, B. L. et al. (2002) Salvinorin A: a potent naturally occurring nonnitrogenous kappa opioid selective agonist. Proc. Natl. Acad. Sci. U.S.A. 99, 11934–11939
- [14]. Capasso, R. et al. (2008) Inhibitory effect of salvinorin A, from Salvia divinorum, on ileitis-induced hypermotility: cross-talk between kappa-opioid and cannabinoid CB(1) receptors. Br. J. Pharmacol. 155, 681–689
- [15]. Fichna, J. et al. (2009) Salvinorin A inhibits colonic transit and neurogenic ion transport in mice by activating kappa-opioid and cannabinoid receptors. Neurogastroenterol. Motil. 21, 1326-e1128
- [16]. Leonti, M. et al. (2010) Falcarinol is a covalent cannabinoid CB1 receptor antagonist and induces pro-allergic effects in skin. Biochem. Pharmacol. 79, 1815–1826
- [17]. Lebot, V. et al. (1997) Kava–The Pacific Elixir: The Definitive Guide to its Ethnobotany, History, and Chemistry, Healing Arts Press
- [18]. Russo, E. B. (2001) Handbook of Psychotropic Herbs: A Scientific Analysis of Herbal Remedies for Psychiatric Conditions, Haworth Press
- [19]. Ligresti, A. et al. (2012) Kavalactones and the endocannabinoid system: the plant-derived yangonin is a novel CB1 receptor ligand. Pharmacol. Res. 66, 163–169
- [20]. Wu, D. et al. (2002) Cyclooxygenase enzyme in hibitory compounds with antioxidant activities from Piper methysticum (kava kava) roots. Phytomedicine 9, 41–47
- [21]. Toyota, M. et al. (1994) Bibenzyl cannabinoid and bisbibenzyl derivative from the liverwort Radula perrottetii. Phytochemistry 37, 859–862
- [22]. Toyota, M. et al. (2002) New bibenzyl cannabinoid from the New Zealand liverwort Radula marginata. Chem. Pharm. Bull. 50, 1390–1392
- [23]. Hajdu, Z. et al. (2014) Identification of endocannabinoid system-modulating N-alkylamides from Heliopsis helianthoides var. scabra and Lepidium meyenii. J. Nat.Prod. 77, 1663–1669
- [24]. Thomas, A. et al. (2007) Cannabidiol displays unexpectedly high potency as anantagonist of CB1 and CB2 receptor agonists in vitro. Br. J. Pharmacol. 150, 613–623
- [25]. Laprairie, R. B. et al. (2015) Cannabidiol is a negative allosteric modulator of the type 1 cannabinoid receptor. Br. J. Pharmacol. 172, 4790–4805
- [26]. Styrczewska, M. et al. (2012) Cannabinoid-like anti-inflammatory compounds from flax fiber. Cell. Mol. Biol. Lett. 17, 479–499
- [27]. Russo, E. B. (2011) Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. Br. J. Pharmacol. 163, 1344–1364
- [28]. Bisogno, T. et al. (2001) Molecular targets for cannabidiol and its synthetic analogues: effect on vanilloid VR1 receptors and on the cellular uptake and enzymatic hydrolysis of anandamide. Br. J. Pharmacol. 134, 845–852
- [29]. Russo, E. (2011) Cannabidiol and TRPV1: turning down the heat (and pain). In 6th Conference on Cannabis in Medicine. International Association for Cannabinoid Medicines, pp. 35
- [30]. Seephonkai, P. et al. (2011) Ferruginenes A–C from Rhododendron ferrugineum and their cytotoxic evaluation. J. Nat. Prod. 74, 712–717
- [31]. Kissin, I. and Szallasi, A. (2011) Therapeutic targeting of TRPV1 by resiniferatoxin, from preclinical studies to clinical trials. Curr. Top. Med. Chem. 11, 2159–2170
- [32]. Szallasi, A. and Blumberg, P. M. (1999) Vanilloid (Capsaicin) receptors and mechanisms. Pharmacol. Rev. 51, 159–212
- [33]. Palazzo, E. et al. (2010) Moving towards supraspinal TRPV1 receptors for chronic pain relief. Mol. Pain 6, 66
- [34]. Banerjee, S. P. et al. (1975) Cannabinoids: influence on neurotransmitter uptake in rat brain synaptosomes. J. Pharmacol. Exp. Ther. 194, 74–81
- [35]. Musty, R. E. and Deyo, R. A. (2006) A cannabigerol extract alters behavioral despair in an animal model of depression. In Symposium on the Cannabinoids. International Cannabinoid Research Society, pp. 32
- [36]. Ligresti, A. et al. (2006) Antitumor activity of plant cannabinoids with emphasis on the effect of cannabidiol on human breast carcinoma. J. Pharmacol. Exp. Ther. 318, 1375–1387
- [37]. Wilkinson, J. D. and Williamson, E. M. (2007) Cannabinoids inhibit human keratinocyte proliferation through an on-CB1/CB2 mechanism and have a potential therapeutic value in the treatment of psoriasis. J. Dermatol. Sci. 45, 87–92
- [38]. Appendino, G. et al. (2008) Antibacterial cannabinoids from Cannabis sativa: a structure–activity study. J. Nat. Prod. 71, 427–1430
- [39]. Cascio, M. G. et al. (2010) Evidence that the plant cannabinoid cannabigerol is a high lypotent α2-adrenoceptor agonist and moderately potent 5HT1A receptor antagonist. Br. J. Pharmacol. 159, 129–141
- [40]. De Petrocellis, L. et al. (2011) Effects of cannabinoids and cannabinoid-enriched Cannabis extracts on TRP channels and endocannabinoid metabolic enzymes. Br. J. Pharmacol. 163, 1479–1494
- [41]. De Petrocellis, L. and DiMarzo, V. (2010) Non-CB1, non-CB2 receptors for endocannabinoids, plant cannabinoids, and synthetic cannabimimetics: focus on G-protein-coupled receptors and transient receptor potential channels. J. Neuroimmune Pharmacol. 5, 103–121
- [42]. Bohlmann, F. and Hoffmann, E. (1979) Cannabigerol-Ahnliche Verbindungen aus Helichrysum umbraculigerum. Phytochemistry 18, 1371–1374
- [43]. Appendino, G. et al. (2015) Helichrysum italicum: the sleeping giant of Mediterranean herbal medicine. Herbal Gram 105, 34–45
- [44]. Lourens, A. C. et al. (2008) South African Helichrysum species: a review of the traditional uses, biological activity and phytochemistry. J. Ethnopharmacol. 119, 630–652
- [45]. Basile, A. C. et al. (1988) Anti-inflammatory activity of oleoresin from Brazilian Copaifera. J. Ethnopharmacol. 22, 101–109
- [46]. Tambe, Y. et al. (1996) Gastric cytoprotection of thenon-steroidal anti-inflammatory sesquiterpene, b-caryophyllene. Planta Med. 62, 469–470
- [47]. Gertsch, J. et al. (2008) Beta-caryophyllene is a dietary cannabinoid. Proc. Natl. Acad. Sci. U.S.A. 105, 9099–9104
- [48]. Gertsch, J. (2008) Anti-inflammatory cannabinoids in diet: towards a better understanding of CB2 receptor action? Commun. Integr. Biol. 1, 26–28
- [49]. Karsak, M. et al. (2007) Attenuation of allergic contact dermatitis through the endocannabinoid system. Science 316, 1494–1497
- [50]. Pacher, P. and Mechoulam, R. (2011) Is lipid signaling through cannabinoid 2 receptors part of a protective system? Prog. Lipid Res. 50, 193–211
- [51]. Tisserand, R. and Young, R. (2014) Essential Oil Safety, Churchill Livingstone Elsevier
- [52]. Gertsch, J. et al. (2004) Echinacea alkylamides modulate TNF-α gene expression via cannabinoid receptor CB2 and multiple signal transduction pathways. FEBS Lett. 577, 563–569
- [53]. Raduner, S. et al. (2006) Alkylamides from Echinacea are a new class of cannabinomimetics. Cannabinoid type 2 receptor-dependent and-independent immunomodulatory effects. J. Biol. Chem. 281, 14192–14206
- [54]. Chicca, A. et al. (2009) Synergistic immunomopharmacological effects of N-alkylamides in Echinacea purpurea herbal extracts. Int. Immunopharmacol. 9, 850–858
- [55]. Spelman, K. et al. (2009) Role for PPARg in IL-2 inhibition in T cells by Echinacea-derived undeca-2E-ene-8,10-diynoicacidisobuty-lamide. Int. Immunopharmacol. 9, 1260–1264
- [56]. Haller, J. et al. (2010) The effect of Echinacea preparations in three laboratory tests of anxiety: comparison with chlordiazepoxide. Phytother. Res. 24, 1605–1613
- [57]. Hohmann, J. et al. (2011) Alkamides and aneolignan from Echinacea purpurea roots and the interaction of alkamides with G-protein-coupled cannabinoid receptors. Phytochemistry 72, 1848–1853
- [58]. McPartland, J. M. et al. (2015) Are cannabidiol and D9-tetrahydrocannabivarin negative modulators of the endocannabinoid system?. A systematic review. Br. J. Pharmacol. 172, 737–753
- [59]. Korte, G. et al. (2010) Tea catechins’ affinity for human cannabinoid receptors. Phytomedicine 17, 19–22
- [60]. Gertsch, J. et al. (2010) Phytocannabinoids beyond the Cannabis plant – do they exist? Br. J. Pharmacol. 160, 523–529
- [61]. Thors, L. et al. (2008) Inhibition of fatty acid amide hydrolase by kaempferol and related naturally occurring flavonoids. Br. J.Pharmacol. 155, 244–252
- [62]. Wu, H. et al. (2013) Macamides and their synthetic analogs: evaluation of in vitro FAAH inhibition. Bioorg. Med. Chem. 21, 5188–5197
- [63]. Di Marzo, V. et al. (1998) Trick or treat from food endocannabinoids? Nature 396, 636–637
- [64]. Maurelli, S. et al. (1995) Two novel classes of neuroactive fatty acid amides are substrates for mouse neuroblastoma ‘anandamide amidohydrolase’. FEBS Lett. 377, 82–86
- [65]. Rousseaux, C. et al. (2007) Lactobacillus acidophilus modulates intestinal pain and induces opioid and cannabinoid receptors. Nat. Med. 13, 35–37
- [66]. Clarke, G. et al. (2012) Probiotics for the treatment of irritable bowel syndrome – focus on lactic acid bacteria. Aliment. Pharmacol. Ther. 35, 403–413
- [67]. Cluny, N. L. et al. (2015) Prevention of diet-induced obesity effects on body weight and gut microbiota in mice treated chronically with D9-tetrahydrocannabinol. PLoS ONE 10, e0144270
- [68]. Slavin, J. (2013) Fiber and prebiotics: mechanisms and health benefits. Nutrients 5, 1417–1435
- [69]. Calame, W. et al. (2008) Gum arabic establishes prebiotic functionality in healthy human volunteers in a dose-dependent manner. Br. J. Nutr. 100, 1269–1275
- [70]. Vickers, W. T. and Plowman, T. (1984) Useful plants of the Siona and Secoya Indians of eastern Ecuador. Fieldiana 15, 1–63
- [71]. Seely, K. A. et al. (2009) The dietary polyphenols trans-resveratrol and curcumin selectively bind human CB1 cannabinoid receptors with nanomolar affinities and function as antagonists/inverse agonists. J. Pharmacol. Exp. Ther. 330, 31–39
- [72]. Prather, P. L. et al. (2009) Notice of retraction. J. Pharmacol. Exp. Ther. 331, 1147
- [73]. da Silva, K. A. et al. (2011) Activation of cannabinoid receptors by the pentacyclic triterpene alpha, beta-amyrin inhibits inflammatory and neuropathic persistent pain in mice. Pain 152, 1872–1887
- [74]. Chicca, A. et al. (2012) The antinociceptive triterpene beta-amyrin inhibits 2-arachidonoylglycerol (2-AG) hydrolysis without directly targeting cannabinoid receptors. Br. J. Pharmacol. 167, 1596–1608
- [75]. Moussaieff, A. et al. (2005) The Jerusalem balsam: from the Franciscan Monastery in the old city of Jerusalem to Martindale 33. J. Ethnopharmacol. 101, 16–26
- [76]. Moussaieff, A. et al. (2008) Incensole acetate, an incense component, elicits psychoactivity by activating TRPV3 channels in the brain. FASEB J. 22, 3024–3034
- [77]. Moussaieff, A. et al. (2008) Incensole acetate: a novel neuroprotective agent isolated from Boswellia carterii. J. Cereb. BloodFlow Metab. 28, 1341–1352
- [78]. Nicolussi, S. et al. (2014) Guineensine is a novel inhibitor of endocannabinoid uptake showing cannabimimetic behavioral effects in BALB/c mice. Pharmacol. Res. 80, 52–65
- [79]. Russo, E. B. (2015) The endocannabinoid system in health and disease: herbalism for the future. In 26th Annual American Herbalists Guild Symposium, American Herbalists Guild
- [80]. Pacioni, G. et al. (2015) Truffles contain endocannabinoid metabolic enzymes and anandamide. Phytochemistry 110, 104–110
- [81]. Blancaflor, E. B. et al. (2014) N-Acylethanolamines: lipidmetabolites with functions in plant growth and development. Plant J. 79, 568–583



