[Άρθρο 1 από 3]
(Αναδημοσίευση με μετάφραση από: “Immune system” https://en.wikipedia.org/wiki/Immune_system, From Wikipedia, the free encyclopedia)
Το ανοσοποιητικό σύστημα είναι ένα οικείο (ενδογενές) σύστημα άμυνας που περιλαμβάνει πολλές βιολογικές δομές και διεργασίες εντός ενός οργανισμού και που προστατεύει από τις ασθένειες όλα όσα αποτελούν έναν οργανισμό, πχ. το σώμα μας, ονομάζονται self (οικεία). Για να λειτουργήσει σωστά, ένα ανοσοποιητικό σύστημα πρέπει να ανιχνεύσει μια μεγάλη ποικιλία παραγόντων, γνωστών ως παθογόνα, από ιούς έως παρασιτικούς σκώληκες (όλα αυτά ονομάζονται non-self [μη οικεία], δηλαδή δεν αποτελούν κομμάτι του οργανισμού) και να τα διακρίνει από τον υγιή ιστό του οργανισμού. Σε πολλά είδη, υπάρχουν δύο σημαντικά υποσυστήματα του ανοσοποιητικού συστήματος: το έμφυτο ανοσοποιητικό σύστημα και το προσαρμοστικό ανοσοποιητικό σύστημα. Και τα δύο υποσυστήματα χρησιμοποιούν την χυμική ανοσία (δηλαδή την ανοσία που σχετίζεται με τα αντισώματα, χρησιμοποιείται το χυμική αντί του χημική γιατί η λέξη προέρχεται από τους χυμούς του σώματος και όχι από το χημικές ενώσεις) και την κυτταρομεσολαβούμενη ανοσία για την εκτέλεση των λειτουργιών τους. Στον άνθρωπο, ο φραγμός αίματος-εγκεφάλου, ο φραγμός αίματος-εγκεφαλονωτιαίου υγρού και παρόμοιοι φραγμοί ρευστών με τον εγκέφαλο διαχωρίζουν το περιφερικό ανοσοποιητικό σύστημα από το νευροανοσοποιητικό σύστημα, το οποίο προστατεύει τον εγκέφαλο.
Τα παθογόνα μπορούν να εξελιχθούν και να προσαρμοστούν γρήγορα, αποφεύγοντας έτσι την ανίχνευση και την εξουδετέρωση από το ανοσοποιητικό σύστημα. Ωστόσο, πολλοί αμυντικοί μηχανισμοί έχουν επίσης εξελιχθεί για να αναγνωρίσουν και να εξουδετερώσουν τους παθογόνους παράγοντες. Ακόμη και οι απλοί μονοκύτταροι οργανισμοί όπως τα βακτήρια διαθέτουν ένα στοιχειώδες ανοσοποιητικό σύστημα με τη μορφή ενζύμων που τα προστατεύουν από λοιμώξεις από βακτηριοφάγους. Άλλοι βασικοί ανοσοποιητικοί μηχανισμοί εξελίχθηκαν στους αρχαίους ευκαρυώτες και παραμένουν στους σύγχρονους απογόνους τους, όπως είναι τα φυτά και τα ασπόνδυλα. Αυτοί οι μηχανισμοί περιλαμβάνουν τη φαγοκυττάρωση, τα αντιμικροβιακά πεπτίδια που ονομάζονται αμυντικά και το συμπληρωματικό σύστημα. Τα σπονδυλωτά, συμπεριλαμβανομένων των ανθρώπων, έχουν ακόμη πιο εξελιγμένους μηχανισμούς άμυνας, συμπεριλαμβανομένης της ικανότητας προσαρμογής με την πάροδο του χρόνου για την αποτελεσματικότερη αναγνώριση συγκεκριμένων παθογόνων παραγόντων. Η προσαρμοστική (ή επίκτητη) ανοσία δημιουργεί ανοσολογική μνήμη μετά από μια αρχική απόκριση σε συγκεκριμένο παθογόνο, οδηγώντας σε ενισχυμένη ανταπόκριση σε επακόλουθες επαφές με το ίδιο παθογόνο. Αυτή η διαδικασία της επίκτητης ανοσίας είναι και η βάση του εμβολιασμού.
Διαταραχές του ανοσοποιητικού συστήματος μπορεί να οδηγήσουν σε αυτοάνοσες ασθένειες, φλεγμονώδεις ασθένειες και καρκίνο. Η ανοσοανεπάρκεια εμφανίζεται όταν το ανοσοποιητικό σύστημα είναι λιγότερο ενεργό από το φυσιολογικό, με αποτέλεσμα την εμφάνιση επαναλαμβανόμενων και απειλητικών για τη ζωή λοιμώξεων. Στον άνθρωπο, η ανοσοανεπάρκεια μπορεί να είναι είτε αποτέλεσμα γενετικής νόσου όπως σοβαρή συνδυασμένη ανοσοανεπάρκεια, επίκτητες καταστάσεις όπως τον HIV/AIDS ή λόγω της χρήσης ανοσοκατασταλτικών φαρμάκων. Αντιθέτως, η αυτοανοσία προκύπτει από ένα υπερδραστικό ανοσοποιητικό σύστημα που επιτίθεται σε φυσιολογικούς ιστούς σαν αυτοί να ήταν ξένοι μικροοργανισμοί. Οι κοινές αυτοάνοσες ασθένειες περιλαμβάνουν τη θυρεοειδίτιδα Hashimoto, τη ρευματοειδή αρθρίτιδα, τον σακχαρώδη διαβήτη τύπου 1, τον συστηματικό ερυθηματώδη λύκο (ΣΕΛ) και αρκετές άλλες. Η ανοσολογία καλύπτει τη μελέτη όλων των πτυχών του ανοσοποιητικού συστήματος.
Διαστρωμάτωση της άμυνας
Το ανοσοποιητικό σύστημα προστατεύει τους οργανισμούς από τη μόλυνση με πολυεπίπεδη άμυνα αυξανόμενης ειδικότητας. Με απλά λόγια, τα φυσικά εμπόδια, εμποδίζουν την είσοδο παθογόνων οργανισμών, όπως τα βακτήρια και οι ιοί, στον οργανισμό. Εάν ένα παθογόνο παραβιάσει αυτά τα εμπόδια, το έμφυτο ανοσοποιητικό σύστημα παρέχει μια άμεση αλλά μη ειδική απάντηση. Ενδογενή ανοσοποιητικά συστήματα βρίσκονται σε όλα τα φυτά και τα ζώα. Εάν τα παθογόνα αποφύγουν επιτυχώς την έμφυτη απόκριση, τα σπονδυλωτά διαθέτουν ένα δεύτερο στρώμα προστασίας, το προσαρμοστικό ανοσοποιητικό σύστημα, το οποίο ενεργοποιείται από την έμφυτη απόκριση. Εδώ, το ανοσοποιητικό σύστημα προσαρμόζει την απόκριση του κατά τη διάρκεια μιας μόλυνσης για να βελτιώσει την αναγνώριση του παθογόνου παράγοντα. Αυτή η βελτιωμένη απόκριση στη συνέχεια διατηρείται μετά την εξάλειψη του παθογόνου παράγοντα, με τη μορφή μίας ανοσολογικής μνήμης, και επιτρέπει στο προσαρμοστικό ανοσοποιητικό σύστημα να τοποθετεί γρηγορότερες και ισχυρότερες επιθέσεις κάθε φορά που αντιμετωπίζεται αυτός ο παθογόνος παράγοντας.
Στοιχεία του ανοσοποιητικού συστήματος
Έμφυτο ανοσοποιητικό σύστημα
* Η απάντηση είναι μη συγκεκριμένη
* Η έκθεση οδηγεί σε άμεση μέγιστη ανταπόκριση
* Κυτταρομεσολαβούμενα και χυμικά συστατικά
* Δεν υπάρχει ανοσολογική μνήμη
* Βρέθηκε σε όλες σχεδόν τις μορφές ζωής
Προσαρμοστικό ανοσοποιητικό σύστημα
* Ειδική απάντηση παθογόνου και αντιγόνου
* Χρονική διάρκεια μεταξύ της έκθεσης και της μέγιστης απόκρισης
* Κυτταρομεσολαβούμενα και χυμικά συστατικά
* Η έκθεση οδηγεί σε ανοσολογική μνήμη
* Βρέθηκε μόνο στα σπονδυλωτά
Τόσο η έμφυτη όσο και η προσαρμοστική ανοσία εξαρτώνται από την ικανότητα του ανοσοποιητικού συστήματος να διακρίνει μεταξύ των οικείων (self) και μη οικείων (non-self) μορίων. Στην ανοσολογία, τα οικεία μόρια είναι εκείνα τα συστατικά του σώματος ενός οργανισμού που μπορούν να διακριθούν από τις ξένες ουσίες από το ανοσοποιητικό σύστημα. Αντιστρόφως, τα μη οικεία μόρια είναι αυτά που αναγνωρίζονται ως ξένα μόρια. Μία τάξη μη οικείων μορίων ονομάζονται αντιγόνα και ορίζονται ως ουσίες που δεσμεύονται σε συγκεκριμένους ανοσολογικούς υποδοχείς και προκαλούν ανοσοαπόκριση.
Τα νεογνά δεν έχουν πρότερη έκθεση σε μικρόβια και είναι ιδιαίτερα ευάλωτα σε λοίμωξη. Διάφορα στρώματα παθητικής προστασίας παρέχονται από τη μητέρα. Κατά τη διάρκεια της εγκυμοσύνης, ένας συγκεκριμένος τύπος αντισώματος, που ονομάζεται IgG, μεταφέρεται από τη μητέρα στο μωρό απευθείας στον πλακούντα, έτσι τα ανθρώπινα μωρά έχουν υψηλά επίπεδα αντισωμάτων ακόμη και κατά τη γέννηση, με το ίδιο φάσμα εξειδικευμένων αντιγόνων όπως και αυτά στην μητέρα τους. Το μητρικό γάλα ή το πρωτόγαλα περιέχει επίσης αντισώματα που μεταφέρονται στο έντερο του βρέφους και το προστατεύουν από βακτηριακές λοιμώξεις έως ότου το νεογέννητο να συνθέσει τα δικά του αντισώματα. Πρόκειται για παθητική ασυλία επειδή το έμβρυο δεν κάνει πραγματικά κύτταρα μνήμης ή αντισώματα παρά μόνο τα δανείζεται. Αυτή η παθητική ανοσία είναι συνήθως βραχυπρόθεσμη, διαρκεί από λίγες μέρες μέχρι μερικούς μήνες. Στην ιατρική, η προστατευτική παθητική ανοσία μπορεί επίσης να μεταφερθεί τεχνητά από το ένα άτομο στο άλλο μέσω του πλούσιου σε αντισώματα ορού.
Έμφυτο ανοσοποιητικό σύστημα
Οι μικροοργανισμοί ή οι τοξίνες που εισέρχονται με επιτυχία σε έναν οργανισμό συναντούν τα κύτταρα και τους μηχανισμούς του έμφυτου ανοσοποιητικού συστήματος. Η έμφυτη απόκριση συνήθως ενεργοποιείται όταν τα μικρόβια εντοπίζονται από υποδοχείς αναγνώρισης προτύπων, οι οποίοι αναγνωρίζουν συστατικά που διατηρούνται μεταξύ ευρέων ομάδων μικροοργανισμών ή όταν τα κατεστραμμένα, τραυματισμένα ή αδυνατισμένα κύτταρα στέλνουν σήματα συναγερμού, πολλά από τα οποία (αλλά όχι όλα) αναγνωρίζονται από τους ίδιους υποδοχείς με εκείνους που αναγνωρίζουν τους παθογόνους παράγοντες. Οι εγγενείς ανοσοποιητικές άμυνες είναι μη ειδικές, πράγμα που σημαίνει ότι αυτά τα συστήματα ανταποκρίνονται σε παθογόνους παράγοντες με γενικό τρόπο. Το σύστημα αυτό δεν παρέχει μακροχρόνια ανοσία έναντι ενός παθογόνου παράγοντα. Το έμφυτο ανοσοποιητικό σύστημα είναι το κυρίαρχο σύστημα υπεράσπισης των ξενιστών στους περισσότερους οργανισμούς.
Αναγνώριση μοτίβων από κύτταρα
Τα κύτταρα στο έμφυτο ανοσοποιητικό σύστημα χρησιμοποιούν υποδοχείς αναγνώρισης προτύπων (pattern recognition receptors, PRRs) για να αναγνωρίζουν μοριακές δομές που παράγονται από μικροβιακούς παθογόνους παράγοντες. Οι PRRs είναι αισθητήρες κωδικοποίησης βλαστικών σειρών, οι οποίοι ανιχνεύουν μόρια τυπικά για τους παθογόνους παράγοντες. Είναι πρωτεΐνες που εκφράζονται κυρίως από κύτταρα του έμφυτου ανοσοποιητικού συστήματος, όπως δενδριτικά κύτταρα, μακροφάγα, μονοκύτταρα, ουδετερόφιλα και επιθηλιακά κύτταρα, για την αναγνώριση δύο κατηγοριών μορίων: τα σχετιζόμενα με τα παθογόνα μοριακά πρότυπα (pathogen-associated molecular patterns, PAMPs), τα οποία σχετίζονται με μικροβιακούς παθογόνους παράγοντες και τα μοριακά πρότυπα που σχετίζονται με βλάβες (damage-associated molecular patterns, DAMPs), τα οποία σχετίζονται με συστατικά των κυττάρων του ξενιστή που απελευθερώνονται κατά τη διάρκεια κυτταρικής βλάβης ή κυτταρικού θανάτου.
Δεσμευτικοί υποδοχείς
Η αναγνώριση των σχετιζόμενων με εξωκυτταρικό ή ενδοσωμικό παθογόνο μοριακών προτύπων προκαλείται από διαμεμβρανικές πρωτεΐνες γνωστές ως υποδοχείς τύπου Toll (Toll-like Receptors, TLRs). Οι TLRs μοιράζονται ένα τυπικό δομικό μοτίβο, τις επαναλήψεις πλούσιες σε λευκίνη (Leucine rich repeats, LRR), οι οποίες τους δίνουν την ιδιαίτερη εμφάνιση και είναι επίσης υπεύθυνες για τη λειτουργικότητα των TLRs. Οι υποδοχείς TLRs ανακαλύφθηκαν για πρώτη φορά στις Δροσόφιλα (είναι γένος δίπτερων εντόμων της οικογένειας Drosophilidae που αποκαλούνται συχνά και φρουτόμυγες ή ξιδόμυγες) και πυροδότησαν τη σύνθεση και την έκκριση κυτοκινών και την ενεργοποίηση άλλων προγραμμάτων άμυνας του ξενιστή που είναι απαραίτητα τόσο για τις έμφυτες όσο και για τις προσαρμοστικές ανοσολογικές αντιδράσεις. Μέχρι σήμερα, δέκα λειτουργικά μέλη της οικογένειας TLRs έχουν περιγραφεί στους ανθρώπους.
Υποδοχείς κυτοσόλιου
Τα κύτταρα στο έμφυτο ανοσοποιητικό σύστημα έχουν υποδοχείς αναγνώρισης προτύπων που ανιχνεύουν μόλυνση ή κυτταρική βλάβη στο κυτταρόπλασμα. Τρεις κύριες κατηγορίες αυτών των υποδοχέων κυτοσόλιων είναι υποδοχείς τύπου NOD, RIG (παρόμοιοι με το ρετινοϊκό οξύ) υποδοχείς και αισθητήρες κυτοσόλιου DNA.
Φλεγμονώματα
Τα φλεγμονώματα είναι σύμπλοκα πολυπρωτεϊνών (αποτελούνται από ένα NLR, την πρωτεΐνη προσαρμογής ASC και το μόριο τελεστή pro-caspase-1) που σχηματίζονται σε απόκριση σε κυτοσολικά PAMPs και DAMPs, η λειτουργία των οποίων είναι η δημιουργία ενεργών μορφών των φλεγμονωδών κυτοκινών IL-1 β και IL-18.
Επιφανειακά εμπόδια
Πολλά εμπόδια προστατεύουν τους οργανισμούς από τη μόλυνση, συμπεριλαμβανομένων μηχανικών, χημικών και βιολογικών φραγμών. Η κηρώδης επιδερμίδα των περισσότερων φύλλων, ο εξωσκελετός των εντόμων, τα κελύφη και οι μεμβράνες των εξωτερικής εναπόθεσης αυγών και το δέρμα αποτελούν παραδείγματα μηχανικών φραγμών που αποτελούν την πρώτη γραμμή άμυνας έναντι μιας λοίμωξης. Ωστόσο, καθώς οι οργανισμοί δεν μπορούν να σφραγιστούν πλήρως από το περιβάλλον τους, άλλα συστήματα δρουν για την προστασία των ανοιγμάτων του σώματος, όπως οι πνεύμονες, τα έντερα και η ουρογεννητική οδός. Στους πνεύμονες, ο βήχας και το φτέρνισμα εκτοξεύουν μηχανικά παθογόνους παράγοντες και άλλους ερεθιστικούς παράγοντες μακριά από την αναπνευστική οδό. Η δράση έκπλυσης των δακρύων και των ούρων εξουδετερώνει επίσης μηχανικά τους παθογόνους παράγοντες, ενώ η βλέννα που εκκρίνεται από την αναπνευστική και γαστρεντερική οδό χρησιμεύει για την παγίδευση και την εμπλοκή μικροοργανισμών.
Τα χημικά εμπόδια προστατεύουν επίσης από τη μόλυνση. Το δέρμα και η αναπνευστική οδός εκκρίνουν αντιμικροβιακά πεπτίδια όπως οι β-αμυντικές ενώσεις. Τα ένζυμα όπως η λυσοζύμη και η φωσφολιπάση Α2 στο σάλιο, στα δάκρυα και στο μητρικό γάλα είναι επίσης αντιβακτηριακά. Οι κολπικές εκκρίσεις χρησιμεύουν ως ένα χημικό φράγμα μετά την εκκίνηση της έμμηνου ρήσης, όταν γίνονται ελαφρώς όξινες, ενώ το σπέρμα περιέχει αμυντικές ενώσεις και ψευδάργυρο για να σκοτώσει τους παθογόνους παράγοντες. Στο στομάχι, το γαστρικό οξύ χρησιμεύει ως μια ισχυρή χημική άμυνα κατά των παθογόνων που έχουν εισέλθει με κατάποση.
Στο εσωτερικό των ουρογεννητικών και γαστρεντερικών οδών, η συντροφική χλωρίδα χρησιμεύει ως βιολογικά εμπόδια, ανταγωνιζόμενη παθογόνα βακτήρια για τροφή και χώρο και, σε ορισμένες περιπτώσεις, μεταβάλλοντας τις συνθήκες στο περιβάλλον τους, όπως το pΗ ή τον διαθέσιμο σίδηρο. Ως αποτέλεσμα του συμβιωτικής σχέσης μεταξύ της συντροφικής χλωρίδας και του ανοσοποιητικού συστήματος, μειώνεται η πιθανότητα οι παθογόνοι οργανισμοί να φθάσουν σε επαρκείς αριθμούς για να προκαλέσουν ασθένεια. Ωστόσο, επειδή τα περισσότερα αντιβιοτικά δεν στοχεύουν ειδικά βακτήρια και δεν επηρεάζουν τους μύκητες, τα από του στόματος αντιβιοτικά μπορούν να οδηγήσουν σε “υπερανάπτυξη” μυκήτων και να προκαλέσουν καταστάσεις όπως κολπική καντιντίαση (μόλυνση ζύμης). Υπάρχουν καλά αποδεικτικά στοιχεία ότι η επανεισαγωγή της προβιοτικής χλωρίδας, όπως οι καθαρές καλλιέργειες των γαλακτοβακίλλων που βρίσκονται κανονικά στο μη παστεριωμένο γιαούρτι, συμβάλλει στην αποκατάσταση μιας υγιούς ισορροπίας μικροβιακών πληθυσμών σε εντερικές λοιμώξεις στα παιδιά και στην ενθάρρυνση προκαταρκτικών δεδομένων σε μελέτες βακτηριακής γαστρεντερίτιδας, σε φλεγμονώδεις νόσους του εντέρου, σε λοίμωξη του ουροποιητικού συστήματος και σε μετα-χειρουργικές λοιμώξεις.
Κυτταρικά συστατικά
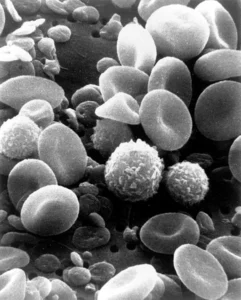
Μια εικόνα ηλεκτρονικού μικροσκοπίου με φυσιολογικό ανθρώπινο αίμα που κυκλοφορεί. Μπορούν να παρατηρηθούν ερυθρά αιμοσφαίρια, μερικά λευκά αιμοσφαίρια, συμπεριλαμβανομένων των λεμφοκυττάρων, ένα μονοκύτταρο, ένα ουδετερόφιλο και πολλά μικρά αιμοπετάλια σε σχήμα δίσκου.
Τα λευκοκύτταρα (λευκά αιμοσφαίρια) δρουν σαν ανεξάρτητοι, μονοκύτταροι οργανισμοί και είναι ο δεύτερος βραχίονας του έμφυτου ανοσοποιητικού συστήματος. Τα έμφυτα λευκοκύτταρα περιλαμβάνουν τα φαγοκύτταρα (μακροφάγα, ουδετερόφιλα και δενδριτικά κύτταρα), έμφυτα λεμφοειδή κύτταρα, μαστοκύτταρα, ηωσινόφιλα, βασεόφιλα και φυσικά κύτταρα φονιάδες. Αυτά τα κύτταρα ταυτοποιούν και εξαλείφουν τους παθογόνους οργανισμούς, είτε προσβάλλοντας μεγαλύτερα παθογόνα μέσω της επαφής είτε με κατακλυσμό και στη συνέχεια θανάτωση μικροοργανισμών. Τα ενδογενή κύτταρα είναι επίσης σημαντικοί μεσολαβητές στην ανάπτυξη λεμφοειδών οργάνων και στην ενεργοποίηση του προσαρμοστικού ανοσοποιητικού συστήματος.
Η φαγοκυττάρωση είναι ένα σημαντικό χαρακτηριστικό της κυτταρικής εγγενούς ανοσίας που εκτελείται από κύτταρα που ονομάζονται φαγοκύτταρα που κατακλύζουν ή τρώνε παθογόνα ή σωματίδια. Τα φαγοκύτταρα γενικά περιπολούν το σώμα αναζητώντας παθογόνα, αλλά μπορούν να καλούνται σε συγκεκριμένες θέσεις από κυτοκίνες. Μόλις ένα παθογόνο έχει απορροφηθεί από ένα φαγοκύτταρο, παγιδεύεται σε ένα ενδοκυτταρικό κυστίδιο που ονομάζεται φαγόσωμα, το οποίο στη συνέχεια συντήκεται με ένα άλλο κυστίδιο που ονομάζεται λυσοσόμημα για να σχηματίσει ένα φαγολυσόσωμα. Το παθογόνο θανατώνεται από τη δραστηριότητα των πεπτικών ενζύμων ή μετά από αναπνευστική έκρηξη που απελευθερώνει ελεύθερες ρίζες στο φαγολυσόσωμα. Η φαγοκυττάρωση εξελίχθηκε ως μέσο για την απόκτηση θρεπτικών συστατικών, αλλά ο ρόλος αυτός επεκτάθηκε στα φαγοκύτταρα για να συμπεριλάβει την καταπόνηση των παθογόνων ως έναν αμυντικό μηχανισμό. Η φαγοκυττάρωση πιθανόν αντιπροσωπεύει την παλαιότερη μορφή άμυνας του ξενιστή, καθώς τα φαγοκύτταρα έχουν ταυτοποιηθεί σε σπονδυλωτά και ασπόνδυλα ζώα.
Φαγοκύτταρα
Τα ουδετερόφιλα και τα μακροφάγα είναι φαγοκύτταρα που ταξιδεύουν σε ολόκληρο το σώμα σε καταδίωξη παθογόνων που τυχόν έχουν εισβάλει. Τα ουδετερόφιλα βρίσκονται κανονικά στην κυκλοφορία του αίματος και είναι ο πιο άφθονος τύπος φαγοκυττάρου, που αντιπροσωπεύει φυσιολογικά το 50% έως 60% των συνολικών κυκλοφορούντων λευκοκυττάρων και αποτελείται από υποπληθυσμούς ουδετερόφιλων–δολοφόνων και ουδετεροφίλων-εντοπιστών. Κατά τη διάρκεια της οξείας φάσης φλεγμονής, ιδιαίτερα ως αποτέλεσμα βακτηριακής μόλυνσης, τα ουδετερόφιλα μεταναστεύουν προς τη θέση της φλεγμονής σε μια διαδικασία που ονομάζεται χημειοταξία και είναι συνήθως τα πρώτα κύτταρα που φθάνουν στο σημείο της λοίμωξης. Τα μακροφάγα είναι πολυδύναμα κύτταρα που βρίσκονται μέσα στους ιστούς και παράγουν μια ευρεία σειρά χημικών, συμπεριλαμβανομένων των ενζύμων, των συμπληρωματικών πρωτεϊνών και των κυτοκινών, ενώ μπορούν επίσης να δράσουν ως σαρωτές που απαλλάσσουν το σώμα από φθαρμένα κύτταρα και άλλα συντρίμματα και ως κύτταρα που παρουσιάζουν αντιγόνο που ενεργοποιούν το προσαρμοστικό ανοσοποιητικό σύστημα.
Δενδριτικά κύτταρα
Τα δενδριτικά κύτταρα (Dendritic cells, DC) είναι φαγοκύτταρα σε ιστούς που έρχονται σε επαφή με το εξωτερικό περιβάλλον, επομένως, βρίσκονται κυρίως στο δέρμα, τη μύτη, τους πνεύμονες, το στομάχι και τα έντερα. Ονομάζονται έτσι για την ομοιότητά τους με τους νευρώνες δενδριτών, καθώς και τα δύο έχουν πολλές σπονδυλικές προβολές, αλλά τα δενδριτικά κύτταρα δεν συνδέονται καθόλου με το νευρικό σύστημα. Τα δενδριτικά κύτταρα χρησιμεύουν ως σύνδεσμος μεταξύ των σωματικών ιστών και του έμφυτου και προσαρμοστικού ανοσοποιητικού συστήματος, καθώς παρουσιάζουν αντιγόνα στα Τ κύτταρα, έναν από τους βασικούς κυτταρικούς τύπους του προσαρμοστικού ανοσοποιητικού συστήματος.
Κοκκιοκύτταρα
Τα κοκκιοκύτταρα είναι λευκοκύτταρα που έχουν κοκκία στο κυτταρόπλασμα τους. Στην κατηγορία αυτή περιλαμβάνονται τα ουδετερόφιλα, τα μαστοκύτταρα, τα βασεόφιλα και τα ηωσινόφιλα. Τα μαστοκύτταρα βρίσκονται σε συνδετικούς ιστούς και βλεννογόνους και ρυθμίζουν την φλεγμονώδη απόκριση. Συνήθως συνδέονται με την αλλεργία και την αναφυλαξία. Τα βασεόφιλα και τα ηωσινόφιλα σχετίζονται με τα ουδετερόφιλα. Εκκρίνουν χημικούς μεσολαβητές που εμπλέκονται στην υπεράσπιση έναντι των παρασίτων και παίζουν ρόλο σε αλλεργικές αντιδράσεις, όπως το άσθμα.
Ενδογενή λεμφοειδή κύτταρα
Τα ενδογενή λεμφοειδή κύτταρα (Innate lymphoid cells, ILCs) είναι μια ομάδα εγγενών ανοσοκυττάρων που προέρχονται από κοινό λεμφικό πρόγονο (lymphoid progenitor, CLP) και ανήκουν στην οικογένεια των λεμφοειδών. Αυτά τα κύτταρα ορίζονται από την απουσία αντιγόνου ειδικού υποδοχέα Β ή Τ κυττάρου εξαιτίας της έλλειψης γονιδίου ενεργοποίησης ανασυνδυασμού (recombination activating gene, RAG). Τα ILCs δεν εκφράζουν μυελοειδείς ή δενδριτικούς κυτταρικούς δείκτες.
Τα φυσικά κύτταρα δολοφόνοι (Natural killer cells), ένα από τα ILC μέλη, είναι λεμφοκύτταρα και ένα συστατικό του έμφυτου ανοσοποιητικού συστήματος το οποίο δεν προσβάλλει απευθείας τα εισβάλλοντα μικρόβια. Αντίθετα, τα NK κύτταρα καταστρέφουν τα υποβαθμισμένα κύτταρα-ξενιστές, όπως κύτταρα όγκου ή κύτταρα που έχουν μολυνθεί από τον ιό, αναγνωρίζοντας τέτοια κύτταρα με μια κατάσταση γνωστή ως “missing self” (έχουν γίνει μη οικεία). Αυτός ο όρος περιγράφει κύτταρα με χαμηλά επίπεδα δείκτη κυτταρικής επιφάνειας που ονομάζεται MHC I (major histocompatibility complex / κύριο σύμπλεγμα ιστοσυμβατότητας), μια κατάσταση που μπορεί να προκύψει σε ιογενείς λοιμώξεις των κυττάρων-ξενιστών. Ονομάστηκαν “φυσικοί δολοφόνοι” εξαιτίας της αρχικής ιδέας ότι δεν απαιτούν ενεργοποίηση για να σκοτώσουν τα κύτταρα που είναι σε κατάσταση “missing self”. Για πολλά χρόνια δεν ήταν σαφές πώς τα κύτταρα NK αναγνωρίζουν κύτταρα όγκου και μολυσμένα κύτταρα. Είναι τώρα γνωστό ότι η σύνθεση MHC στην επιφάνεια αυτών των κυττάρων μεταβάλλεται και τα κύτταρα ΝΚ ενεργοποιούνται μέσω της αναγνώρισης της κατάστασης “missing self”. Τα φυσιολογικά κύτταρα του σώματος δεν αναγνωρίζονται και δεν προσβάλλονται από τα κύτταρα ΝΚ επειδή εκφράζουν ανέπαφα τα MHC αντιγόνα. Αυτά τα MHC αντιγόνα αναγνωρίζονται από τους υποδοχείς ανοσοσφαιρίνης των κυττάρων δολοφόνων (killer cell immunoglobulin receptors, KIR) που ουσιαστικά φρενάρουν τα κύτταρα ΝΚ.
Φλεγμονή
Η φλεγμονή είναι μια από τις πρώτες απαντήσεις / αποκρίσεις του ανοσοποιητικού συστήματος σε λοίμωξη. Τα συμπτώματα της φλεγμονής είναι ερυθρότητα, οίδημα, θερμότητα και πόνος, τα οποία προκαλούνται από αυξημένη ροή αίματος σε ιστό. Η φλεγμονή παράγεται από εικοσανοειδή και κυτοκίνες, τα οποία απελευθερώνονται από τραυματισμένα ή μολυσμένα κύτταρα. Τα εικοσανοειδή περιλαμβάνουν προσταγλανδίνες που προκαλούν πυρετό και διαστολή αιμοφόρων αγγείων που σχετίζονται με φλεγμονή και λευκοτριένια που προσελκύουν ορισμένα λευκά αιμοσφαίρια (λευκοκύτταρα). Οι κοινές κυτοκίνες περιλαμβάνουν τις ιντερλευκίνες που είναι υπεύθυνες για την επικοινωνία μεταξύ των λευκών αιμοσφαιρίων, τις χημειοκίνες που προάγουν χημειοταξία και τις ιντερφερόνες που έχουν αντι-ιικές επιδράσεις, όπως διακοπή της πρωτεϊνικής σύνθεσης στο κύτταρο ξενιστή. Μπορούν επίσης να απελευθερωθούν παράγοντες ανάπτυξης και κυτταροτοξικοί παράγοντες. Αυτές οι κυτοκίνες και άλλες χημικές ουσίες προσλαμβάνουν κύτταρα ανοσίας στο σημείο της λοίμωξης και προάγουν την επούλωση οποιουδήποτε κατεστραμμένου ιστού μετά την απομάκρυνση των παθογόνων.
Συμπληρωματικό σύστημα
Το συμπληρωματικό σύστημα είναι ένας βιοχημικός καταρράκτης που προσβάλλει τις επιφάνειες ξένων κυττάρων. Περιέχει πάνω από 20 διαφορετικές πρωτεΐνες και ονομάζεται έτσι λόγω της ικανότητάς του να “συμπληρώνει” τη θανάτωση των παθογόνων με αντισώματα. Το συμπληρωματικό είναι το κύριο χυμικό συστατικό της έμφυτης ανοσοαπόκρισης. Πολλά είδη έχουν συμπληρωματικά συστήματα, συμπεριλαμβανομένων των μη θηλαστικών όπως τα φυτά, τα ψάρια και μερικά ασπόνδυλα.
Στον άνθρωπο, αυτή η απόκριση ενεργοποιείται με συμπληρωματική δέσμευση στα αντισώματα που έχουν προσδεθεί σε αυτά τα μικρόβια ή τη δέσμευση πρωτεϊνών συμπληρώματος σε υδατάνθρακες στις επιφάνειες των μικροβίων. Αυτό το σήμα αναγνώρισης ενεργοποιεί μια γρήγορη απόκριση θανάτου. Η ταχύτητα της απόκρισης είναι ένα αποτέλεσμα ενίσχυσης σήματος που συμβαίνει μετά από διαδοχική πρωτεολυτική ενεργοποίηση μορίων συμπληρώματος, που είναι επίσης πρωτεάσες. Αφού οι πρωτεΐνες του συμπληρώματος αρχικά δεσμεύονται στο μικρόβιο, ενεργοποιούν τη δραστικότητα πρωτεάσης τους, η οποία με τη σειρά της ενεργοποιεί άλλες πρωτεάσες συμπληρώματος και ούτω καθεξής. Αυτό παράγει έναν καταλυτικό καταρράκτη που ενισχύει το αρχικό σήμα με ελεγχόμενη θετική ανατροφοδότηση. Ο καταρράκτης έχει ως αποτέλεσμα την παραγωγή πεπτιδίων που προσελκύουν ανοσοκύτταρα, αυξάνουν την αγγειακή διαπερατότητα και καταδεικνύουν την επιφάνεια ενός παθογόνου, χαρακτηρίζοντάς το για καταστροφή. Αυτή η εναπόθεση συμπληρώματος μπορεί επίσης να εξοντώσει τα κύτταρα απευθείας μέσω της ρήξης της μεμβράνης πλάσματος τους.
Προσαρμοστικό ανοσοποιητικό σύστημα
Το προσαρμοστικό ανοσοποιητικό σύστημα εξελίχθηκε στα πρώιμα σπονδυλωτά και επιτρέπει μια ισχυρότερη ανοσοαπόκριση καθώς και ανοσολογική μνήμη, όπου κάθε παθογόνο “απομνημονεύεται” με ένα αντιγόνο-υπογραφή. Η προσαρμοστική ανοσοαπόκριση είναι ειδική για το αντιγόνο και απαιτεί την αναγνώριση ειδικών αντιγόνων “μη ενδογενών” κατά τη διάρκεια μιας διαδικασίας που ονομάζεται παρουσίαση αντιγόνου. Η εξειδίκευση του αντιγόνου επιτρέπει τη δημιουργία αποκρίσεων προσαρμοσμένων σε συγκεκριμένα παθογόνα ή σε κύτταρα που έχουν μολυνθεί από παθογόνα. Η ικανότητα να προσαρμόζονται αυτές οι προσαρμοσμένες απαντήσεις διατηρείται στο σώμα με τα “κύτταρα μνήμης”. Εάν ένα παθογόνο μολύνει το σώμα περισσότερο από μία φορά, αυτά τα συγκεκριμένα κύτταρα μνήμης χρησιμοποιούνται για να το εξαλείψουν γρήγορα.
Η αναγνώριση του αντιγόνου
Τα κύτταρα του προσαρμοστικού ανοσοποιητικού συστήματος είναι ειδικοί τύποι λευκοκυττάρων, που ονομάζονται λεμφοκύτταρα. Τα Β κύτταρα και τα Τ κύτταρα είναι οι κυριότεροι τύποι λεμφοκυττάρων και προέρχονται από αιματοποιητικά βλαστοκύτταρα στον μυελό των οστών. Τα Β κύτταρα εμπλέκονται στην χυμική ανοσοαπόκριση, ενώ τα Τ κύτταρα εμπλέκονται στην κυτταρική μεσολαβούμενη ανοσοαπόκριση.
Τα Τ κύτταρα δολοφόνοι, αναγνωρίζουν μόνο αντιγόνα συζευγμένα με μόρια MHC Κατηγορίας Ι (Class I MHC), ενώ τα βοηθητικά Τ κύτταρα και τα ρυθμιστικά Τ κύτταρα αναγνωρίζουν μόνο αντιγόνα συζευγμένα με μόρια MHC Κατηγορίας II (Class II MHC). Αυτοί οι δύο μηχανισμοί παρουσίασης αντιγόνου αντικατοπτρίζουν τους διαφορετικούς ρόλους των δύο τύπων Τ κυττάρων. Ένας τρίτος, δευτερεύων τύπος είναι τα Τ κύτταρα που αναγνωρίζουν άθικτα αντιγόνα που δεν δεσμεύονται με τους υποδοχείς MHC. Τα διπλά-θετικά Τ κύτταρα εκτίθενται σε μια ευρεία ποικιλία αυτοαντιγόνων στον θύμο αδένα, στον οποίο το ιώδιο είναι απαραίτητο για την ανάπτυξη του θύμου και τη δραστηριότητα του.
Αντίθετα, ο αντιγόνος-ειδικός υποδοχέας Β κυττάρων είναι ένα μόριο αντισώματος στην επιφάνεια των B κυττάρων και αναγνωρίζει ολόκληρα παθογόνα χωρίς καμία ανάγκη για επεξεργασία αντιγόνου. Κάθε σειρά B κυττάρων εκφράζει ένα διαφορετικό αντίσωμα, έτσι ώστε το πλήρες σετ υποδοχέων αντιγόνου Β κυττάρων να αντιπροσωπεύει όλα τα αντισώματα που μπορεί να παράγει το σώμα.
Παρουσία αντιγόνου σε Τ λεμφοκύτταρα
Και τα Β κύτταρα και τα Τ κύτταρα φέρουν μόρια υποδοχέα που αναγνωρίζουν συγκεκριμένους στόχους. Τα Τ-λεμφοκύτταρα αναγνωρίζουν έναν “non-self” στόχο, όπως είναι ο παθογόνος παράγοντας, μόνο αφού τα αντιγόνα (μικρά θραύσματα του παθογόνου) έχουν υποβληθεί σε επεξεργασία και παρουσιάζονται σε συνδυασμό με έναν “self” υποδοχέα που ονομάζεται κύριο μόριο συμπλέγματος ιστοσυμβατότητας (major histocompatibility complex, MHC).
Κυτταρομεσολαβούμενη ανοσία
Υπάρχουν δύο κύριοι υποτύποι Τ κυττάρων: το T κύτταρο δολοφόνος και το βοηθητικό Τ κύτταρο. Επιπλέον υπάρχουν ρυθμιστικά Τ κύτταρα τα οποία έχουν ένα ρόλο στη διαμόρφωση της ανοσοαπόκρισης.
Τα Τ κύτταρα δολοφόνοι
Τα Τ κύτταρα δολοφόνοι είναι μια υποομάδα Τ κυττάρων που θανατώνουν κύτταρα που είναι μολυσμένα με ιούς (και άλλα παθογόνα) ή είναι αλλοιωμένα ή δυσλειτουργικά. Όπως και με τα Β κύτταρα, κάθε τύπος Τ κυττάρου αναγνωρίζει ένα διαφορετικό αντιγόνο. Τα Τ κύτταρα δολοφόνοι ενεργοποιούνται όταν ο υποδοχέας Τ-κυττάρων (T-cell receptor, TCR) δεσμεύεται με αυτό το ειδικό αντιγόνο σε ένα σύμπλεγμα με τον υποδοχέα MHC Κατηγορίας Ι ενός άλλου κυττάρου. Η αναγνώριση αυτού του συμπλόκου MHC με αντιγόνο, βοηθείται από έναν συν-υποδοχέα στο Τ κύτταρο, που ονομάζεται CD8. Στη συνέχεια, το Τ κύτταρο ταξιδεύει σε ολόκληρο το σώμα σε αναζήτηση κυττάρων όπου οι υποδοχείς MHC Ι φέρουν αυτό το αντιγόνο. Όταν ένα ενεργοποιημένο Τ κύτταρο έρχεται σε επαφή με τέτοια κύτταρα, απελευθερώνει κυτοτοξίνες, όπως η περφορίνη, οι οποίες σχηματίζουν πόρους στη μεμβράνη πλάσματος του κυττάρου-στόχου, επιτρέποντας την είσοδο ιόντων, νερού και τοξινών. Η είσοδος άλλης τοξίνης που ονομάζεται κοκκιολυσίνη (μια πρωτεάση) προκαλεί στο κύτταρο στόχο την απόπτωση. Η θανάτωση των κυττάρων-ξενιστές από τα Τ κύτταρα είναι ιδιαίτερα σημαντική στην πρόληψη της αντιγραφής των ιών. Η ενεργοποίηση των T κυττάρων ελέγχεται αυστηρά και γενικά απαιτεί ένα πολύ ισχυρό σήμα ενεργοποίησης MHC / αντιγόνου ή επιπρόσθετα σήματα ενεργοποίησης που παρέχονται από “βοηθητικά” Τ κύτταρα.
Βοηθητικά T κύτταρα
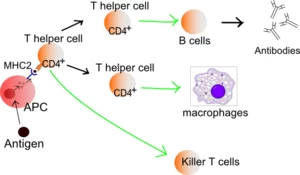
Λειτουργία βοηθητικών Τ κυττάρων: Τα κύτταρα που παρουσιάζουν αντιγόνο (Antigen-presenting cells, APCs), παρουσιάζουν αντιγόνο στα μόρια MHC Kατηγορίας II (MHC2). Τα βοηθητικά Τ κύτταρα τα αναγνωρίζουν, με τη βοήθεια της έκφρασης του CD4 συν-υποδοχέα (CD4+). Η ενεργοποίηση ενός βοηθητικού Τ-λεμφοκυττάρου βοηθά στην απελευθέρωση των κυτοκινών και άλλων σημάτων διέγερσης (πράσινα βέλη) που διεγείρουν τη δραστηριότητα των μακροφάγων, των Τ κυττάρων και των Β κυττάρων, τα οποία παράγουν αντισώματα. Η διέγερση των Β-λεμφοκυττάρων και των μακροφάγων επιτυγχάνει τον πολλαπλασιασμό των βοηθητικών T κυττάρων.
Τα βοηθητικά Τ κύτταρα ρυθμίζουν τόσο τις έμφυτες όσο και τις προσαρμοστικές ανοσολογικές αποκρίσεις και βοηθούν στον προσδιορισμό των ανοσιακών αποκρίσεων που κάνει το σώμα σε ένα συγκεκριμένο παθογόνο. Αυτά τα κύτταρα δεν έχουν κυτταροτοξική δράση και δεν θανατώνουν μολυσμένα κύτταρα ούτε και καθαρίζουν άμεσα τα παθογόνα. Αντιθέτως, ελέγχουν την ανοσολογική απόκριση κατευθύνοντας άλλα κύτταρα για να εκτελέσουν αυτές τις εργασίες.
Τα βοηθητικά Τ κύτταρα εκφράζουν υποδοχείς Τ κυττάρων (T cell receptors, TCRs) που αναγνωρίζουν το δεσμευμένο αντιγόνο σε μόρια MHC κατηγορίας II. Το σύμπλοκο MHC με αντιγόνο, αναγνωρίζεται επίσης από τον συν-υποδοχέα CD4 του βοηθητικού κυττάρου, ο οποίος προσλαμβάνει μόρια εντός του Τ κυττάρου (πχ. Lck) που είναι υπεύθυνα για την ενεργοποίηση του Τ κυττάρου. Τα βοηθητικά Τ-λεμφοκύτταρα έχουν ασθενέστερη συσχέτιση με το σύμπλεγμα MHC με αντιγόνο από ότι παρατηρήθηκε για τα T κύτταρα δολοφόνους, που σημαίνει ότι πολλοί υποδοχείς (περίπου 200-300) στο βοηθητικό Τ κύτταρο πρέπει να δεσμεύονται από ένα σύμπλεγμα MHC:αντιγόνου προκειμένου να ενεργοποιήσουν το βοηθητικό κύτταρο, ενώ τα Τ κύτταρα δολοφόνοι μπορούν να ενεργοποιηθούν με δέσμευση ενός μονού MHC:αντιγόνου. Η ενεργοποίηση του βοηθητικού Τ κυττάρου απαιτεί επίσης μεγαλύτερη διάρκεια δέσμευσης με ένα κύτταρο παρουσίασης αντιγόνου. Η ενεργοποίηση ενός βοηθητικού Τ λεμφοκυττάρου βοηθά στην απελευθέρωση των κυτοκινών που επηρεάζουν τη δραστηριότητα πολλών τύπων κυττάρων. Τα σήματα κυτοκίνης που παράγονται από βοηθητικά Τ κύτταρα ενισχύουν τη μικροβιοκτόνο λειτουργία των μακροφάγων και τη δραστηριότητα των T κυττάρων δολοφόνων. Επιπλέον, η ενεργοποίηση των βοηθητικών T κυττάρων προκαλεί μια ρύθμιση προς τα πάνω των μορίων που εκφράζονται στην επιφάνεια των T κυττάρων, όπως ο συμπλοκοποιητής CD40 (επίσης αποκαλούμενος CD154), που παρέχουν επιπλέον διεγερτικά σήματα τα οποία τυπικά απαιτούνται για την ενεργοποίηση των B κυττάρων που παράγουν αντισώματα.
Τα γάμμα δέλτα T κύτταρα
Τα γάμμα δέλτα T κύτταρα (γδ Τ κύτταρα) κατέχουν έναν εναλλακτικό υποδοχέα Τ-κυττάρων (TCR) σε αντίθεση με τα CD4+ και CD8+ (αβ) Τ κύτταρα και μοιράζονται τα χαρακτηριστικά βοηθητικών Τ κυττάρων, κυτταροτοξικών Τ κυττάρων και ΝΚ κυττάρων. Οι συνθήκες που παράγουν αποκρίσεις από γδ Τ κύτταρα δεν είναι πλήρως κατανοητές. Όπως και άλλα “αντισυμβατικά” υποσύνολα Τ κυττάρων που φέρουν αμετάβλητους TCRs, όπως τα περιορισμένα με CD1d φυσικοί δολοφόνοι Τ λεμφοκύτταρα, τα γδ Τ κύτταρα διασκελίζουν το όριο μεταξύ έμφυτης και προσαρμοστικής ανοσίας. Από τη μία πλευρά, τα γδ Τ κύτταρα είναι ένα συστατικό της προσαρμοστικής ανοσίας, καθώς αναδιατάσσουν τα γονίδια TCR για να παράγουν ποικιλία υποδοχέα και μπορούν επίσης να αναπτύξουν ένα φαινότυπο μνήμης. Από την άλλη πλευρά, τα διάφορα υποσύνολα είναι επίσης μέρος του έμφυτου ανοσοποιητικού συστήματος, όπως οι περιορισμένοι TCR ή NK υποδοχείς μπορούν να χρησιμοποιηθούν ως υποδοχείς αναγνώρισης προτύπων. Για παράδειγμα, μεγάλοι αριθμοί ανθρώπινων Vγ9/Vδ2 T κυττάρων ανταποκρίνονται μέσα σε ώρες σε κοινά μόρια που παράγονται από μικρόβια, ενώ τα εξαιρετικά περιορισμένα Vδ1+ Τ κύτταρα στο επιθήλιο αποκρίνονται σε στρετσαρισμένα επιθηλιακά κύτταρα.
Η χυμική ανοσοαπόκριση
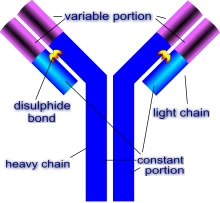
Ένα αντίσωμα αποτελείται από δύο βαριές αλυσίδες και δύο ελαφρές αλυσίδες. Η μοναδική μεταβλητή περιοχή επιτρέπει στο αντίσωμα να αναγνωρίζει το αντίστοιχο αντιγόνο του.
Ένα Β κύτταρο αναγνωρίζει παθογόνα όταν τα αντισώματα στην επιφάνειά του συνδέονται με ένα συγκεκριμένο ξένο αντιγόνο. Αυτό το σύμπλοκο αντιγόνου / αντισώματος παραλαμβάνεται από το Β κύτταρο και υποβάλλεται σε επεξεργασία με πρωτεόλυση σε πεπτίδια. Το Β κύτταρο εμφανίζει έπειτα αυτά τα αντιγονικά πεπτίδια επί των επιφανειακών μορίων MHC Κατηγορίας II. Αυτός ο συνδυασμός MHC και αντιγόνου προσελκύει ένα βοηθητικό Τ κύτταρο, το οποίο απελευθερώνει λεμφοκίνες και ενεργοποιεί το Β κύτταρο. Καθώς το ενεργοποιημένο Β κύτταρο αρχίζει τότε να διαιρείται, οι απόγονοί του (κύτταρα πλάσματος) εκκρίνουν εκατομμύρια αντίγραφα του αντισώματος που αναγνωρίζει αυτό το αντιγόνο. Αυτά τα αντισώματα κυκλοφορούν στο πλάσμα του αίματος και της λέμφου, δεσμεύονται σε παθογόνους παράγοντες που εκφράζουν το αντιγόνο και τα χαρακτηρίζουν για καταστροφή με ενεργοποίηση συμπληρώματος ή για πρόσληψη και καταστροφή από τα φαγοκύτταρα. Τα αντισώματα μπορούν επίσης να εξουδετερώνουν άμεσα τις προκλήσεις, με τη δέσμευση σε βακτηριακές τοξίνες ή με παρεμβολή στους υποδοχείς που χρησιμοποιούν οι ιοί και τα βακτηρίδια για να μολύνουν τα κύτταρα.
Ανοσολογική μνήμη
Όταν τα Β κύτταρα και τα Τ κύτταρα ενεργοποιούνται και αρχίζουν να αναπαράγονται, κάποιοι από τους απογόνους τους γίνονται κύτταρα μακράς διαρκείας. Καθ’ όλη τη διάρκεια ζωής ενός ζώου, αυτά τα κύτταρα μνήμης θυμούνται κάθε συγκεκριμένο παθογόνο που έχουν συναντήσει και μπορούν να δώσουν ισχυρή απάντηση αν ανιχνευθεί ξανά το παθογόνο. Αυτό είναι “προσαρμοστικό” επειδή εμφανίζεται (επίκτητο) κατά τη διάρκεια της ζωής ενός ατόμου ως προσαρμογή στη μόλυνση με αυτόν τον παθογόνο παράγοντα και προετοιμάζει το ανοσοποιητικό σύστημα για μελλοντικές προκλήσεις. Η ανοσολογική μνήμη μπορεί να είναι είτε παθητική βραχυπρόθεσμη μνήμη είτε ενεργή μακροχρόνια μνήμη.
Φυσιολογική ρύθμιση
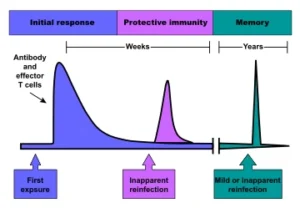
Η χρονική πορεία μιας ανοσοαπόκρισης ξεκινά με την αρχική αντιμετώπιση των παθογόνων (ή τον αρχικό εμβολιασμό) και οδηγεί στο σχηματισμό και τη διατήρηση της ενεργού ανοσολογικής μνήμης.
Το ανοσοποιητικό σύστημα εμπλέκεται σε πολλές πτυχές της φυσιολογικής ρύθμισης στο σώμα. Το ανοσοποιητικό σύστημα αλληλεπιδρά στενά με άλλα συστήματα, όπως το ενδοκρινικό και το νευρικό σύστημα. Το ανοσοποιητικό σύστημα διαδραματίζει επίσης σημαντικό ρόλο στην εμβρυογένεση (ανάπτυξη του εμβρύου), καθώς και στην αποκατάσταση και αναγέννηση των ιστών.
Ορμόνες
Οι ορμόνες μπορούν να λειτουργήσουν ως ανοσοτροποποιητές, αλλάζοντας την ευαισθησία του ανοσοποιητικού συστήματος. Για παράδειγμα, οι γυναικείες σεξουαλικές ορμόνες είναι γνωστοί ανοσοδιεγέρτες τόσο των προσαρμοστικών όσο και των έμφυτων ανοσολογικών αποκρίσεων. Ορισμένες αυτοάνοσες ασθένειες, όπως ο ερυθηματώδης λύκος, προξενούνται στις γυναίκες και η εμφάνισή τους συχνά συμπίπτει με την εφηβεία. Αντίθετα, οι ανδρικές σεξουαλικές ορμόνες όπως η τεστοστερόνη φαίνεται να είναι ανοσοκατασταλτικές. Άλλες ορμόνες φαίνεται να ρυθμίζουν και το ανοσοποιητικό σύστημα, κυρίως η προλακτίνη, η αυξητική ορμόνη και η βιταμίνη D.
Βιταμίνη D
Όταν ένα Τ κύτταρο συναντά ένα ξένο παθογόνο, επεκτείνει έναν υποδοχέα βιταμίνης D. Αυτό είναι ουσιαστικά μια συσκευή σηματοδότησης που επιτρέπει στο Τ κύτταρο να δεσμεύεται στην ενεργό μορφή της βιταμίνης D, της στεροειδούς ορμόνης καλσιτριόλη. Τα Τ κύτταρα έχουν μια συμβιωτική σχέση με τη βιταμίνη D. Όχι μόνο το Τ κύτταρο επεκτείνει έναν υποδοχέα βιταμίνης D, ζητώντας ουσιαστικά να συνδεθεί με την έκδοση στεροειδών ορμονών της βιταμίνης D, της καλσιτριόλης, αλλά το Τ κύτταρο εκφράζει το γονίδιο CYP27B1, που είναι το γονίδιο που είναι υπεύθυνο για τη μετατροπή της προ-ορμονικής έκδοσης της βιταμίνης D, της καλσιδιόλης στην έκδοση των στεροειδών ορμονών, την καλσιτριόλη. Μόνο μετά τη σύνδεση με την καλσιτριόλη μπορούν τα Τ κύτταρα να εκτελέσουν την προβλεπόμενη λειτουργία τους. Άλλα κύτταρα του ανοσοποιητικού συστήματος που είναι γνωστό ότι εκφράζουν το CYP27B1 και έτσι ενεργοποιούν την καλσιδιόλη της βιταμίνης D, είναι τα δενδριτικά κύτταρα, τα κερατινοκύτταρα και τα μακροφάγα.
Υποτίθεται ότι μια προοδευτική μείωση των ορμονικών επιπέδων με την ηλικία είναι εν μέρει υπεύθυνη για τις εξασθενημένες ανοσολογικές αντιδράσεις στα γηράσκοντα άτομα. Αντίθετα, ορισμένες ορμόνες ρυθμίζονται από το ανοσοποιητικό σύστημα, κυρίως από τη δραστηριότητα των θυρεοειδικών ορμονών. Η μείωση της ανοσολογικής λειτουργίας που σχετίζεται με την ηλικία σχετίζεται επίσης με τη μείωση των επιπέδων βιταμίνης D στους ηλικιωμένους. Καθώς οι άνθρωποι γερνούν, συμβαίνουν δύο πράγματα που επηρεάζουν αρνητικά τα επίπεδα βιταμίνης D. Πρώτον, αυτά τα άτομα παραμένουν εντός κατοικίας περισσότερο λόγω μειωμένων επιπέδων δραστηριότητας. Αυτό σημαίνει ότι παίρνουν λιγότερο ήλιο και κατά συνέπεια παράγουν λιγότερη χοληκαλσιφερόλη μέσω της UVB ακτινοβολίας. Δεύτερον, καθώς ένα άτομο μεγαλώνει, το δέρμα γίνεται λιγότερο αποδοτικό στην παραγωγή βιταμίνης D.
Ύπνος και ξεκούραση
Το ανοσοποιητικό σύστημα επηρεάζεται από τον ύπνο και την ανάπαυση και η στέρηση του ύπνου είναι επιζήμια για την ανοσολογική λειτουργία. Οι σύνθετοι κύκλοι ανάδρασης που εμπλέκουν κυτοκίνες, όπως η ιντερλευκίνη-1 και ο παράγοντας νέκρωσης όγκων-α, που παράγονται ως ανταπόκριση σε λοίμωξη, φαίνεται να παίζουν επίσης ρόλο στη ρύθμιση του ύπνου μη ταχείας κίνησης των ματιών (REM). Έτσι, η ανοσοαπόκριση στη μόλυνση μπορεί να οδηγήσει σε αλλαγές στον κύκλο του ύπνου, συμπεριλαμβανομένης της αύξησης του ύπνου με αργό κύμα σε σχέση με τον ύπνο REM.
Όταν υποφέρουμε από στέρηση ύπνου, οι ενεργές ανοσοποιήσεις μπορεί να έχουν μειωμένο αποτέλεσμα και μπορεί να οδηγήσουν σε χαμηλότερη παραγωγή αντισωμάτων και χαμηλότερη ανοσιακή απόκριση από ότι θα παρατηρηθεί σε ένα ξεκούραστο άτομο. Επιπλέον, πρωτεΐνες όπως η NFIL3, οι οποίες έχουν αποδειχθεί ότι είναι στενά συνδεδεμένες τόσο με τη διαφοροποίηση των Τ κυττάρων όσο και με τους κιρκάδιους ρυθμούς μας, μπορούν να επηρεαστούν μέσω της διαταραχής του φυσικού φωτός και των σκοτεινών κύκλων μέσω περιπτώσεων στέρησης ύπνου, εργασίας με βάρδιες κλπ. Ως συνέπεια, αυτές οι διαταραχές μπορούν να οδηγήσουν σε αύξηση των χρόνιων παθήσεων όπως είναι οι καρδιακές παθήσεις, ο χρόνιος πόνος και το άσθμα.
Εκτός από τις αρνητικές συνέπειες της στέρησης του ύπνου, ο ύπνος και το αλληλοσυνδεδεμένο κιρκαδικό σύστημα έχουν αποδειχθεί ότι έχουν ισχυρές ρυθμιστικές επιδράσεις στις ανοσολογικές λειτουργίες που επηρεάζουν τόσο την έμφυτη όσο και την προσαρμοστική ανοσία. Κατ’ αρχάς, κατά τη διάρκεια της πρώιμης φάσης αργού κύματος ύπνου, μια ξαφνική πτώση των επιπέδων κορτιζόλης, επινεφρίνης και νορεπινεφρίνης στο αίμα προκαλεί αυξημένα επίπεδα στο αίμα των ορμονών λεπτίνη, αυξητική ορμόνη της υπόφυσης και προλακτίνη. Αυτά τα σήματα προκαλούν μια προ-φλεγμονώδη κατάσταση μέσω της παραγωγής των προ-φλεγμονωδών κυτοκινών ιντερλευκίνη-1, ιντερλευκίνη-12, ΤΝΡ-άλφα και ΙΡΝ-γ. Αυτές οι κυτοκίνες στη συνέχεια διεγείρουν ανοσολογικές λειτουργίες όπως η ενεργοποίηση των ανοσοκυττάρων, τον πολλαπλασιασμό και την διαφοροποίηση. Κατά τη διάρκεια αυτού του χρονικού διαστήματος, τα αδιαφοροποίητα ή λιγότερο διαφοροποιημένα κύτταρα, όπως τα απλοϊκά και τα κεντρικής μνήμης T κύτταρα, κορυφώνονται (δηλ. κατά τη διάρκεια ενός χρόνου αργά εξελισσόμενης προσαρμοστικής ανοσοαπόκρισης). Εκτός από αυτές τις επιδράσεις, το περιβάλλον των ορμονών που παράγονται αυτή τη στιγμή (λεπτίνη, αυξητική ορμόνη της υπόφυσης και προλακτίνη) υποστηρίζει τις αλληλεπιδράσεις μεταξύ APCs και Τ κυττάρων, μετατόπιση του ισοζυγίου κυτοκίνης Th1/Th2 προς ένα που υποστηρίζει Th1, αύξηση του συνολικού πολλαπλασιασμού των κυττάρων Th και μετανάστευση των Τ κυττάρων σε λεμφαδένες. Αυτό το περιβάλλον πιστεύεται επίσης ότι υποστηρίζει το σχηματισμό μακροχρόνιας ανοσοποιητικής μνήμης μέσω της έναρξης ανοσοαποκρίσεων Th1.
Αντίθετα, κατά τη διάρκεια των περιόδων αφύπνισης, διαφοροποιημένα κύτταρα τελεστές, όπως κυτταροτοξικά φυσικά κύτταρα δολοφόνοι και τα CTLs (κυτταροτοξικά Τ λεμφοκύτταρα), κορυφώνουν για να προκαλέσουν αποτελεσματική απόκριση έναντι τυχόν παθογόνων που εισβάλλουν. Επίσης, κατά τη διάρκεια των άγρυπνων ενεργών χρόνων, τα αντιφλεγμονώδη μόρια, όπως η κορτιζόλη και οι κατεχολαμίνες, κορυφώνονται. Υπάρχουν δύο θεωρίες ως προς το γιατί η προ-φλεγμονώδης κατάσταση έχει δεσμευτεί για τον ύπνο. Πρώτον, η φλεγμονή θα προκαλούσε σοβαρές γνωστικές και σωματικές βλάβες εάν επρόκειτο να συμβεί κατά τη διάρκεια των χρόνων αφύπνισης. Δεύτερον, μπορεί να εμφανιστεί φλεγμονή κατά τη διάρκεια του ύπνου λόγω της παρουσίας μελατονίνης. Η φλεγμονή προκαλεί μεγάλο οξειδωτικό στρες και η παρουσία μελατονίνης κατά τη διάρκεια του ύπνου μπορεί να αντισταθμίσει ενεργά την παραγωγή ελεύθερων ριζών κατά τη διάρκεια αυτής της περιόδου.
Διατροφή και σίτιση
Η υπερκατανάλωση σχετίζεται με ασθένειες όπως ο διαβήτης και η παχυσαρκία, οι οποίες είναι γνωστό ότι επηρεάζουν την ανοσολογική λειτουργία. Ο πιο μέτριος υποσιτισμός, καθώς και ορισμένες συγκεκριμένες ανωμαλίες ιχνοστοιχείων και θρεπτικών συστατικών, μπορούν επίσης να θέσουν σε κίνδυνο την ανοσοαπόκριση.
Τα τρόφιμα πλούσια σε ορισμένα λιπαρά οξέα μπορούν να προωθήσουν ένα υγιές ανοσοποιητικό σύστημα. Παρομοίως, η υποσίτιση του εμβρύου μπορεί να προκαλέσει μια δια βίου εξασθένιση του ανοσοποιητικού του συστήματος.
Επισκευή και αναγέννηση
Το ανοσοποιητικό σύστημα, ιδιαίτερα το έμφυτο κομμάτι του, παίζει αποφασιστικό ρόλο στην αποκατάσταση ιστών μετά από προσβολή. Οι βασικοί παράγοντες περιλαμβάνουν μακροφάγα και ουδετερόφιλα, αλλά είναι επίσης σημαντικοί άλλοι κυτταρικοί παράγοντες, συμπεριλαμβανομένων των γδ Τ κυττάρων, των εγγενών λεμφοειδών κυττάρων (innate lymphoid cells, ILCs) και των ρυθμιστικών Τ κυττάρων (Tregs). Η πλαστικότητα των ανοσολογικών κυττάρων και η ισορροπία μεταξύ των προ-φλεγμονωδών και των αντιφλεγμονωδών σημάτων είναι ζωτικής σημασίας για την αποτελεσματική αποκατάσταση ιστών. Τα ανοσοποιητικά συστατικά και οι οδοί εμπλέκονται επίσης στην αναγέννηση, για παράδειγμα στα αμφίβια. Σύμφωνα με μία υπόθεση, οι οργανισμοί που μπορούν να αναγεννηθούν θα μπορούσαν να είναι λιγότερο ανοσοποιημένοι από τους οργανισμούς που δεν μπορούν να αναγεννηθούν.
Διαταραχές της ανθρώπινης ανοσίας
Το ανοσοποιητικό σύστημα είναι μια αξιοσημείωτα αποτελεσματική δομή που ενσωματώνει την εξειδίκευση, την επαγωγικότητα και την προσαρμογή. Παρ’ όλα αυτά, οι αποτυχίες της άμυνας του ξενιστή εμφανίζονται σε τρεις ευρείες κατηγορίες: ανοσοανεπάρκεια, αυτοανοσία και υπερευαισθησία.
Ανοσοανεπάρκεια
Οι ανοσοανεπάρκειες εμφανίζονται όταν ένα ή περισσότερα από τα συστατικά του ανοσοποιητικού συστήματος είναι ανενεργά. Η ικανότητα του ανοσοποιητικού συστήματος να ανταποκρίνεται στα παθογόνα μειώνεται τόσο στους νέους όσο και στους ηλικιωμένους, με τις ανοσολογικές αντιδράσεις να αρχίζουν να μειώνονται σε ηλικία περίπου 50 ετών λόγω της ανοσοενισχυτικότητας. Στις ανεπτυγμένες χώρες, η παχυσαρκία, ο αλκοολισμός και η χρήση ουσιών είναι κοινά αίτια της κακής ανοσολογικής λειτουργίας. Ωστόσο, ο υποσιτισμός είναι η πιο κοινή αιτία της ανοσοανεπάρκειας στις αναπτυσσόμενες χώρες. Οι δίαιτες που δεν έχουν επαρκή πρωτεΐνη σχετίζονται με την εξασθενημένη ανοσία που προκαλείται από κύτταρα, τη συμπληρωματική δραστικότητα, την λειτουργία των φαγοκυττάρων, την συγκέντρωση αντισωμάτων IgA και την παραγωγή κυτοκίνης. Επιπρόσθετα, η απώλεια του θύμου αδένα σε νεαρή ηλικία μέσω γενετικής μετάλλαξης ή χειρουργικής απομάκρυνσης έχει ως αποτέλεσμα σοβαρή ανοσοανεπάρκεια και υψηλή ευαισθησία σε λοίμωξη.
Οι ανοσοανεπάρκειες μπορούν επίσης να κληρονομηθούν ή να “αποκτηθούν”. Η χρόνια κοκκιωματώδης νόσος, όπου τα φαγοκύτταρα έχουν μειωμένη ικανότητα να καταστρέφουν τους παθογόνους παράγοντες, αποτελεί παράδειγμα κληρονομικής ή συγγενούς ανοσοανεπάρκειας. Το AIDS και μερικοί τύποι καρκίνου προκαλούν ανοσοανεπάρκεια.
Αυτοανοσία
Οι υπερδραστικές ανοσοαποκρίσεις περιλαμβάνουν το άλλο άκρο της ανοσολογικής δυσλειτουργίας, ιδιαίτερα τις αυτοάνοσες διαταραχές. Εδώ, το ανοσοποιητικό σύστημα αποτυγχάνει να διακρίνει σωστά μεταξύ του ενδογενούς (“self”) και του μη-ενδογενούς (“non-self”) και επιτίθεται σε μέρος του σώματος. Υπό κανονικές συνθήκες, πολλά Τ κύτταρα και αντισώματα αντιδρούν με πεπτίδια “self”. Μια από τις λειτουργίες εξειδικευμένων κυττάρων (που βρίσκονται στον θύμο αδένα και τον μυελό των οστών) είναι να παρουσιάσουν νεαρά λεμφοκύτταρα με αυτοαντιγόνα που παράγονται σε ολόκληρο το σώμα και να εξαλείψουν εκείνα τα κύτταρα που αναγνωρίζουν αυτοαντιγόνα, αποτρέποντας την αυτοανοσία.
Υπερευαισθησία
Η υπερευαισθησία είναι μια ανοσοαπόκριση που καταστρέφει τους ιστούς του οργανισμού. Διακρίνονται σε τέσσερις κατηγορίες (Τύποι Ι έως IV) βάσει των μηχανισμών που εμπλέκονται και της χρονικής πορείας της αντίδρασης υπερευαισθησίας. Η υπερευαισθησία Τύπου Ι είναι μια άμεση ή αναφυλακτική αντίδραση, που συχνά σχετίζεται με την αλλεργία. Τα συμπτώματα μπορεί να κυμαίνονται από ήπια δυσφορία μέχρι και θάνατο. Η υπερευαισθησία Τύπου Ι προκαλείται από την IgE, η οποία προκαλεί την αποκοκκίωση των μαστοκυττάρων και των βασεόφιλων όταν συνδέονται σταυρωτά με αντιγόνα. Η υπερευαισθησία Τύπου II συμβαίνει όταν τα αντισώματα συνδέονται με αντιγόνα στα κύτταρα του ίδιου του ασθενούς, τα οποία και τα καταστρέφουν. Αυτό ονομάζεται επίσης υπερευαισθησία εξαρτώμενη από αντίσωμα (ή κυτταροτοξική) και προκαλείται από αντισώματα IgG και IgM. Τα ανοσοσυμπλέγματα (συσσωματώματα αντιγόνων, πρωτεΐνες συμπληρώματος και αντισώματα IgG και IgM) που έχουν κατατεθεί σε διάφορους ιστούς προκαλούν αντιδράσεις υπερευαισθησίας Τύπου ΙΙΙ. Η υπερευαισθησία Τύπου IV (γνωστή επίσης ως υπερευαισθησία με μεσολάβηση κυττάρων ή καθυστερημένου τύπου) συνήθως διαρκεί μεταξύ δύο και τριών ημερών για να αναπτυχθεί. Οι αντιδράσεις Τύπου IV εμπλέκονται σε πολλές αυτοάνοσες και μολυσματικές ασθένειες, αλλά μπορεί επίσης να περιλαμβάνουν δερματίτιδα εξ επαφής (δηλητήριο κισσού). Αυτές οι αντιδράσεις προκαλούνται από Τ κύτταρα, μονοκύτταρα και μακροφάγα.
Ιδιοπαθής φλεγμονή
Η φλεγμονή είναι μία από τις πρώτες απαντήσεις του ανοσοποιητικού συστήματος στη λοίμωξη, αλλά μπορεί να εμφανιστεί χωρίς γνωστή αιτία.
Η φλεγμονή παράγεται από εικοσανοειδή και κυτοκίνες, τα οποία απελευθερώνονται από τραυματισμένα ή μολυσμένα κύτταρα. Τα εικοσανοειδή περιλαμβάνουν προσταγλανδίνες που προκαλούν πυρετό και διαστολή αιμοφόρων αγγείων που σχετίζονται με φλεγμονή και λευκοτριένια που προσελκύουν ορισμένα λευκά αιμοσφαίρια (λευκοκύτταρα). Οι κοινές κυτοκίνες περιλαμβάνουν τις ιντερλευκίνες που είναι υπεύθυνες για την επικοινωνία μεταξύ των λευκών αιμοσφαιρίων, τις χημειοκίνες που προάγουν χημειοταξία και τις ιντερφερόνες που έχουν αντι-ιικές επιδράσεις, όπως διακοπή της πρωτεϊνικής σύνθεσης στο κύτταρο ξενιστή. Μπορούν επίσης να απελευθερωθούν παράγοντες ανάπτυξης και κυτταροτοξικοί παράγοντες. Αυτές οι κυτοκίνες και άλλες χημικές ουσίες προσλαμβάνουν κύτταρα ανοσίας στο σημείο της λοίμωξης και προάγουν την επούλωση οποιουδήποτε κατεστραμμένου ιστού μετά την απομάκρυνση των παθογόνων.
Χειρισμός στην ιατρική
Το ανοσοκατασταλτικό φάρμακο δεξαμεθαζόνη
Η ανοσοαπόκριση μπορεί να χειραγωγηθεί για να καταστείλει ανεπιθύμητες αποκρίσεις που προκύπτουν από αυτοανοσία, αλλεργία και απόρριψη μοσχεύματος και να διεγείρει προστατευτικές αντιδράσεις κατά παθογόνων που αποφεύγουν σε μεγάλο βαθμό το ανοσοποιητικό σύστημα (βλέπε ανοσοποίηση) ή στον καρκίνο.
Ανοσοκαταστολή
Ανοσοκατασταλτικά φάρμακα χρησιμοποιούνται για τον έλεγχο αυτοάνοσων διαταραχών ή φλεγμονών όταν εμφανίζεται υπερβολική βλάβη ιστού και για την πρόληψη της απόρριψης μοσχεύματος μετά από μεταμόσχευση οργάνου.
Τα αντιφλεγμονώδη φάρμακα χρησιμοποιούνται συχνά για τον έλεγχο των επιδράσεων της φλεγμονής. Τα γλυκοκορτικοειδή είναι τα πιο ισχυρά από αυτά τα φάρμακα. Ωστόσο, αυτά τα φάρμακα μπορεί να έχουν πολλές ανεπιθύμητες παρενέργειες, όπως κεντρική παχυσαρκία, υπεργλυκαιμία, οστεοπόρωση και η χρήση τους πρέπει να ελέγχεται αυστηρά. Χαμηλές δόσεις αντιφλεγμονωδών φαρμάκων χρησιμοποιούνται συχνά σε συνδυασμό με κυτταροτοξικά ή ανοσοκατασταλτικά φάρμακα όπως μεθοτρεξάτη ή αζαθειοπρίνη. Τα κυτταροτοξικά φάρμακα αναστέλλουν την ανοσοαπόκριση με θανάτωση διαχωρισμένων κυττάρων όπως τα ενεργοποιημένα Τ κύτταρα. Ωστόσο, η θανάτωση είναι αδιάκριτη και επηρεάζονται άλλα συνεχώς διαιρούμενα κύτταρα και τα όργανα τους, γεγονός που προκαλεί τοξικές παρενέργειες. Τα ανοσοκατασταλτικά φάρμακα, όπως η κυκλοσπορίνη, εμποδίζουν τα Τ κύτταρα να ανταποκρίνονται σωστά στα σήματα αναστέλλοντας τις οδούς μεταγωγής σήματος.
Ανοσοδιέγερση
Η ανοσοθεραπεία του καρκίνου καλύπτει τους ιατρικούς τρόπους για την τόνωση του ανοσοποιητικού συστήματος για την αντιμετώπιση καρκινικών όγκων.
Εμβολιασμός
Η μακροχρόνια ενεργή μνήμη αποκτάται μετά από μόλυνση με ενεργοποίηση Β και Τ κυττάρων. Η ενεργή ανοσία μπορεί επίσης να δημιουργηθεί τεχνητά, μέσω του εμβολιασμού. Η αρχή πίσω από τον εμβολιασμό (επίσης ονομάζεται ανοσοποίηση) είναι η εισαγωγή αντιγόνου από παθογόνο προκειμένου να διεγερθεί το ανοσοποιητικό σύστημα και να αναπτυχθεί ειδική ανοσία έναντι αυτού του συγκεκριμένου παθογόνου παράγοντα χωρίς να προκληθεί ασθένεια που σχετίζεται με αυτόν τον οργανισμό. Αυτή η σκόπιμη επαγωγή μιας ανοσοαπόκρισης είναι επιτυχής επειδή εκμεταλλεύεται τη φυσική εξειδίκευση του ανοσοποιητικού συστήματος, καθώς και την ευκινησία του. Δεδομένου ότι η μολυσματική ασθένεια παραμένει μία από τις κύριες αιτίες θανάτου στον ανθρώπινο πληθυσμό, ο εμβολιασμός αντιπροσωπεύει τον αποτελεσματικότερο χειρισμό του ανοσοποιητικού συστήματος που έχει αναπτύξει η ανθρωπότητα.
Τα περισσότερα εμβόλια ιών βασίζονται σε ζώντες εξασθενημένους ιούς, ενώ πολλά βακτηριακά εμβόλια βασίζονται σε ακυτταρικά συστατικά μικροοργανισμών, συμπεριλαμβανομένων αβλαβών συστατικών τοξινών. Δεδομένου ότι πολλά αντιγόνα που προέρχονται από ακυτταρικά εμβόλια δεν προκαλούν έντονα την προσαρμοστική απόκριση, τα περισσότερα βακτηριακά εμβόλια παρέχονται με πρόσθετα που ενεργοποιούν τα κύτταρα που παρουσιάζουν αντιγόνο του έμφυτου ανοσοποιητικού συστήματος και μεγιστοποιούν την ανοσογονικότητα.
Ανοσολογία των όγκων
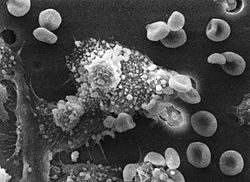
Τα μακρόφαγα έχουν εντοπίσει ένα καρκινικό κύτταρο (η μεγάλη, αγκαθωτή μάζα). Με τη σύντηξη με το καρκινικό κύτταρο, τα μακρόφαγα (μικρότερα λευκά κύτταρα) εισάγουν τοξίνες που σκοτώνουν το κύτταρο όγκου. Η ανοσοθεραπεία για τη θεραπεία του καρκίνου είναι ένας ενεργός τομέας της ιατρικής έρευνας.
Ένας άλλος σημαντικός ρόλος του ανοσοποιητικού συστήματος είναι ο εντοπισμός και η εξάλειψη των όγκων. Αυτό ονομάζεται ανοσολογική παρακολούθηση. Τα μετασχηματισμένα κύτταρα των όγκων εκφράζουν αντιγόνα που δεν βρίσκονται στα φυσιολογικά κύτταρα. Στο ανοσοποιητικό σύστημα, αυτά τα αντιγόνα εμφανίζονται ως ξένα και η παρουσία τους προκαλεί τα κύτταρα του ανοσοποιητικού συστήματος να προσβάλλουν τα μετασχηματισμένα κύτταρα όγκου. Τα αντιγόνα που εκφράζονται από τους όγκους έχουν διάφορες πηγές, μερικοί προέρχονται από ογκογονικούς ιούς όπως ο ιός του ανθρώπινου θηλώματος, ο οποίος προκαλεί καρκίνο του τραχήλου της μήτρας, ενώ άλλοι είναι οι ίδιες πρωτεΐνες του οργανισμού που εμφανίζονται σε χαμηλά επίπεδα σε φυσιολογικά κύτταρα αλλά φθάνουν σε υψηλά επίπεδα στα κύτταρα όγκου. Ένα παράδειγμα είναι ένα ένζυμο που ονομάζεται τυροσινάση, το οποίο, όταν εκφράζεται σε υψηλά επίπεδα, μετασχηματίζει ορισμένα κύτταρα του δέρματος (πχ. μελανοκύτταρα) σε όγκους που ονομάζονται μελανώματα. Μια τρίτη πιθανή πηγή αντιγόνων όγκου είναι πρωτεΐνες που είναι φυσιολογικά σημαντικές για τη ρύθμιση της κυτταρικής ανάπτυξης και της επιβίωσης, που συνήθως μεταλλάσσονται σε μόρια που προκαλούν καρκίνο που ονομάζονται ογκογονίδια.
Η κυριότερη απόκριση του ανοσοποιητικού συστήματος στους όγκους είναι η καταστροφή των ανώμαλων κυττάρων με τη χρήση T κυττάρων δολοφόνων, μερικές φορές με τη βοήθεια βοηθητικών T κυττάρων. Τα αντιγόνα όγκου παρουσιάζονται σε μόρια MHC Κατηγορίας Ι κατά παρόμοιο τρόπο με τα αντιγόνα του ιού. Αυτό επιτρέπει στα T κύτταρα δολοφόνους να αναγνωρίσουν το κύτταρο όγκου ως ανώμαλο. Τα NK κύτταρα επίσης σκοτώνουν τα καρκινικά κύτταρα με παρόμοιο τρόπο, ειδικά εάν τα καρκινικά κύτταρα έχουν λιγότερα μόρια MHC Κατηγορίας Ι στην επιφάνειά τους από το κανονικό. Αυτό είναι ένα κοινό φαινόμενο με όγκους. Μερικές φορές παράγονται αντισώματα ενάντια σε καρκινικά κύτταρα που επιτρέπουν την καταστροφή τους από το συμπληρωματικό σύστημα.
Σαφώς, ορισμένοι όγκοι αποφεύγουν το ανοσοποιητικό σύστημα και συνεχίζουν να γίνονται καρκίνοι. Τα κύτταρα όγκου έχουν συχνά μειωμένο αριθμό μορίων MHC Κατηγορίας Ι στην επιφάνειά τους, αποφεύγοντας έτσι την ανίχνευση από T κύτταρα δολοφόνους. Μερικά κύτταρα όγκου επίσης απελευθερώνουν προϊόντα που αναστέλλουν την ανοσοαπόκριση. Για παράδειγμα με την έκκριση της κυτοκίνης TGF-β, η οποία καταστέλλει τη δραστηριότητα των μακροφάγων και των λεμφοκυττάρων. Επιπλέον, η ανοσολογική ανοχή μπορεί να αναπτυχθεί έναντι των αντιγόνων του όγκου, έτσι ώστε το ανοσοποιητικό σύστημα να μην προσβάλλει πλέον τα καρκινικά κύτταρα.
Παραδόξως, τα μακρόφαγα μπορούν να προάγουν την ανάπτυξη του όγκου όταν τα καρκινικά κύτταρα στέλνουν τις κυτοκίνες που προσελκύουν μακροφάγα, τα οποία στη συνέχεια παράγουν κυτοκίνες και αυξητικούς παράγοντες όπως παράγοντα άλφα νεκρώσεως όγκων που καλλιεργούν ανάπτυξη όγκου ή προάγουν πλαστικότητα τύπου στελεχιαίων κυττάρων. Επιπρόσθετα, ένας συνδυασμός υποξίας στον όγκο και μιας κυτοκίνης που παράγεται από μακρόφαγα επάγει κύτταρα όγκου για να μειώσουν την παραγωγή μιας πρωτεΐνης που μπλοκάρει τη μετάσταση και έτσι βοηθά στην εξάπλωση των καρκινικών κυττάρων.
Προβλέποντας την ανοσογονικότητα
Τα χοντρότερα φάρμακα (> 500Da) μπορούν να προκαλέσουν μια εξουδετερωτική ανοσοαπόκριση, ιδιαίτερα εάν τα φάρμακα χορηγούνται επανειλημμένα ή σε μεγαλύτερες δόσεις. Αυτό περιορίζει την αποτελεσματικότητα φαρμάκων που βασίζονται σε μεγαλύτερα πεπτίδια και πρωτεΐνες (τα οποία τυπικά είναι μεγαλύτερα από 6.000Da). Σε ορισμένες περιπτώσεις, το ίδιο το φάρμακο δεν είναι ανοσογόνο, αλλά μπορεί να συγχορηγείται με μια ανοσογόνο ένωση, όπως συμβαίνει μερικές φορές στην περίπτωση του Taxol. Έχουν αναπτυχθεί υπολογιστικές μέθοδοι για την πρόβλεψη της ανοσογονικότητας των πεπτιδίων και των πρωτεϊνών, οι οποίες είναι ιδιαίτερα χρήσιμες στο σχεδιασμό θεραπευτικών αντισωμάτων, στην εκτίμηση της πιθανής λοιμογόνου δράσης των μεταλλάξεων στα σωματίδια του ιικού περιβλήματος και στην επικύρωση των προτεινόμενων θεραπευτικών αγωγών με πεπτίδιο. Οι πρώτες τεχνικές βασίστηκαν κυρίως στην παρατήρηση ότι τα υδρόφιλα αμινοξέα υπερεκπροσωπούνται σε περιοχές επιτόπιων παρά σε υδρόφοβα αμινοξέα. Όμως οι πιο πρόσφατες εξελίξεις βασίζονται σε τεχνικές μηχανικής μάθησης που χρησιμοποιούν βάσεις δεδομένων για υπάρχοντες γνωστούς επιτόπιους, που έχουν μελετηθεί ως πρωτεΐνες ιού, ως σύνολο εκπαίδευσης. Έχει δημιουργηθεί μια δημόσια προσβάσιμη βάση δεδομένων για την καταλογογράφηση των επιτόπιων από παθογόνα που είναι γνωστό ότι είναι αναγνωρίσιμα από Β κύτταρα. Το αναδυόμενο πεδίο των μελετών της ανοσογονικότητας που βασίζονται σε βιοπληροφορική αναφέρεται ως ανοσοπληροφορική. Η ανοσοπροστατευτική είναι η μελέτη μεγάλων συνόλων πρωτεϊνών (πρωτεϊνωμάτων) που εμπλέκονται στην ανοσοαπόκριση.
Εξέλιξη και άλλοι μηχανισμοί
Εξέλιξη του ανοσοποιητικού συστήματος
Είναι πιθανό ότι ένα πολυσωματικό, προσαρμοστικό ανοσοποιητικό σύστημα να προέκυψε από τα πρώτα σπονδυλωτά, καθώς τα ασπόνδυλα δεν παράγουν λεμφοκύτταρα ή χυμική απόκριση με βάση αντισώματα. Πολλά είδη, ωστόσο, χρησιμοποιούν μηχανισμούς που φαίνεται να είναι πρόδρομοι αυτών των πτυχών της ανοσίας των σπονδυλωτών. Τα ανοσοποιητικά συστήματα εμφανίζονται ακόμη και στις δομικά πιο απλές μορφές ζωής, με τα βακτηρίδια να χρησιμοποιούν ένα μοναδικό αμυντικό μηχανισμό, που ονομάζεται σύστημα τροποποίησης περιορισμού, για να προστατευθούν από παθογόνους ιούς, που ονομάζονται βακτηριοφάγοι. Οι προκαρυώτες διαθέτουν επίσης επίκτητη ανοσία μέσω ενός συστήματος που χρησιμοποιεί ακολουθίες CRISPR για να συγκρατούν θραύσματα των γονιδιωμάτων του φάγου που έχουν έρθει σε επαφή στο παρελθόν, γεγονός που τους επιτρέπει να εμποδίζουν την αναπαραγωγή του ιού μέσω μίας μορφής παρεμβολής του RNA. Οι προκαρυώτες διαθέτουν επίσης και άλλους αμυντικούς μηχανισμούς. Τα επιθετικά στοιχεία του ανοσοποιητικού συστήματος είναι επίσης παρόντα στους μονοκύτταρους ευκαρυώτες, αλλά οι μελέτες των ρόλων τους στην άμυνα είναι λίγες.
Οι υποδοχείς αναγνώρισης μοτίβων είναι πρωτεΐνες που χρησιμοποιούνται από σχεδόν όλους τους οργανισμούς για την αναγνώριση μορίων που σχετίζονται με παθογόνους παράγοντες. Τα αντιμικροβιακά πεπτίδια που ονομάζονται αμυντοσίνες είναι ένα εξελικτικά διατηρημένο συστατικό της έμφυτης ανοσολογικής αντίδρασης που απαντάται σε όλα τα ζώα και τα φυτά και αποτελούν την κύρια μορφή της συστηματικής ανοσίας των ασπόνδυλων. Το συμπληρωματικό σύστημα και τα φαγοκυτταρικά κύτταρα χρησιμοποιούνται επίσης από τις περισσότερες μορφές ασπόνδυλων. Οι ριβονουκλεάσες και η οδός παρεμβολής του RNA διατηρούνται σε όλους τους ευκαρυώτες και πιστεύεται ότι παίζουν κάποιο ρόλο στην ανοσολογική απόκριση σε ιούς.
Σε αντίθεση με τα ζώα, τα φυτά στερούνται φαγοκυτταρικών κυττάρων, αλλά πολλές φυτικές ανοσολογικές αντιδράσεις περιλαμβάνουν συστηματικά χημικά σήματα που αποστέλλονται μέσω ενός φυτού. Τα μεμονωμένα φυτικά κύτταρα ανταποκρίνονται σε μόρια που σχετίζονται με παθογόνα γνωστά ως σχετιζόμενα με μοριακά πρότυπα παθογόνου ή PAMPs (Pathogen-associated molecular patterns). Όταν ένα μέρος ενός φυτού μολύνεται, το φυτό παράγει μια εντοπισμένη υπερευαισθησία, όπου τα κύτταρα στο σημείο της μόλυνσης υφίστανται ταχεία απόπτωση για να εμποδίσουν την εξάπλωση της νόσου σε άλλα μέρη του φυτού. Η συστημική επίκτητη αντίσταση (Systemic acquired resistance, SAR) είναι ένας τύπος αμυντικής απόκρισης που χρησιμοποιείται από φυτά που καθιστά το σύνολο του φυτού ανθεκτικό σε συγκεκριμένο μολυσματικό παράγοντα. Οι μηχανισμοί σίγασης RNA είναι ιδιαίτερα σημαντικοί σε αυτή τη συστηματική απόκριση καθώς μπορούν να εμποδίσουν την αναπαραγωγή ιού.
Εναλλακτικό προσαρμοστικό ανοσοποιητικό σύστημα
Εξέλιξη του προσαρμοστικού ανοσοποιητικού συστήματος συνέβη σε έναν πρόγονο των σπονδυλωτών. Πολλά από τα κλασικά μόρια του προσαρμοστικού ανοσοποιητικού συστήματος (πχ. ανοσοσφαιρίνες και υποδοχείς Τ κυττάρων) υπάρχουν μόνο στα σπονδυλωτά. Ωστόσο, ένα ξεχωριστό μόριο που προέρχεται από λεμφοκύτταρα έχει ανακαλυφθεί σε πρωτόγονα σπονδυλωτά, όπως στο lamprey και στο hagfish. Αυτά τα ζώα διαθέτουν μια μεγάλη ποικιλία μορίων που ονομάζονται μεταβλητοί υποδοχείς λεμφοκυττάρων (Variable lymphocyte receptors, VLRs), που, όπως και οι υποδοχείς αντιγόνων των σπονδυλωτών, παράγονται από ένα μικρό αριθμό (ένα ή δύο) γονιδίων. Αυτά τα μόρια πιστεύεται ότι συνδέονται με παθογόνα αντιγόνα με παρόμοιο τρόπο με τα αντισώματα και με τον ίδιο βαθμό εξειδίκευσης.
Χειρισμός από παθογόνα
Η επιτυχία οποιουδήποτε παθογόνου εξαρτάται από την ικανότητά του να παραλείπει τις ανοσολογικές αποκρίσεις του ξενιστή. Επομένως, τα παθογόνα έχουν αναπτύξει διάφορες μεθόδους που τους επιτρέπουν να μολύνουν επιτυχώς έναν ξενιστή, αποφεύγοντας ανίχνευση ή καταστροφή από το ανοσοποιητικό σύστημα. Τα βακτήρια συχνά ξεπερνούν τα φυσικά εμπόδια με την έκκριση ενζύμων που χωνεύουν το φράγμα, για παράδειγμα, χρησιμοποιώντας ένα σύστημα έκκρισης τύπου ΙΙ. Εναλλακτικά, χρησιμοποιώντας ένα σύστημα έκκρισης τύπου III, μπορούν να εισάγουν έναν κοίλο σωλήνα στο κύτταρο ξενιστή, παρέχοντας μια άμεση οδό για να μετακινηθούν οι πρωτεΐνες από τον παθογόνο στον ξενιστή. Αυτές οι πρωτεΐνες χρησιμοποιούνται συχνά για να κλείσουν τις άμυνες του ξενιστή.
Μια στρατηγική διαφυγής που χρησιμοποιείται από διάφορα παθογόνα για την αποφυγή του έμφυτου ανοσοποιητικού συστήματος είναι η απόκρυψη μέσα στα κύτταρα του ξενιστή τους (επίσης αποκαλούμενη ενδοκυτταρική παθογένεση). Εδώ, ένα παθογόνο ξοδεύει το μεγαλύτερο μέρος του κύκλου της ζωής του μέσα στα κύτταρα-ξενιστές, όπου προστατεύεται από την άμεση επαφή με ανοσοκύτταρα, αντισώματα και συμπληρώματα. Μερικά παραδείγματα ενδοκυτταρικών παθογόνων περιλαμβάνουν τους ιούς, το βακτήριο τροφικής δηλητηρίασης Σαλμονέλα (Salmonella) και τα ευκαρυωτικά παράσιτα που προκαλούν ελονοσία (Plasmodium falciparum) και λεϊσμανίαση (Leishmania spp.). Άλλα βακτήρια, όπως το Mycobacterium tuberculosis, ζουν μέσα σε μια προστατευτική κάψουλα που εμποδίζει τη λύση με συμπλήρωμα. Πολλά παθογόνα εκκρίνουν ενώσεις που μειώνουν ή διαστρέφουν την ανοσολογική απόκριση του ξενιστή. Ορισμένα βακτήρια σχηματίζουν βιοφίλμ (biofilms) για να προστατευθούν από τα κύτταρα και τις πρωτεΐνες του ανοσοποιητικού συστήματος. Τέτοια βιολογικά φιλμ υπάρχουν σε πολλές επιτυχείς μολύνσεις, πχ. χρόνιες λοιμώξεις Pseudomonas aeruginosa και Burkholderia cenocepacia χαρακτηριστικές της κυστικής ίνωσης. Άλλα βακτήρια παράγουν επιφανειακές πρωτεΐνες που δεσμεύονται με αντισώματα, καθιστώντας τες αναποτελεσματικές. Παραδείγματα περιλαμβάνουν τα Streptococcus (πρωτεΐνη G), Staphylococcus aureus (πρωτεΐνη Α) και Peptostreptococcus magnus (πρωτεΐνη L).
Οι μηχανισμοί που χρησιμοποιούνται για να αποφύγουν το προσαρμοστικό ανοσοποιητικό σύστημα είναι πιο περίπλοκοι. Η απλούστερη προσέγγιση είναι η ταχεία αλλαγή μη ουσιαστικών επιτόπιων (αμινοξέων ή/και σακχάρων) στην επιφάνεια του παθογόνου, διατηρώντας παράλληλα τους ουσιαστικούς επιτόπιους που αποκρύπτονται. Αυτό ονομάζεται αντιγονική παραλλαγή. Ένα παράδειγμα είναι ο HIV, ο οποίος μεταλλάσσεται ταχέως, έτσι ώστε οι πρωτεΐνες στο ιικό περίβλημα που είναι απαραίτητες για την είσοδο στο κύτταρο-στόχο του ξενιστή αλλάζουν διαρκώς. Αυτές οι συχνές αλλαγές στα αντιγόνα μπορούν να εξηγήσουν τις αποτυχίες των εμβολίων που στρέφονται προς αυτόν τον ιό. Το παράσιτο Trypanosoma brucei χρησιμοποιεί μια παρόμοια στρατηγική, αλλάζοντας συνεχώς έναν τύπο επιφανειακής πρωτεΐνης από την μια στην άλλη, επιτρέποντάς του έτσι να παραμείνει ένα βήμα μπροστά από την αντίδραση του αντισώματος. Τα αντιγόνα κάλυψης με μόρια ξενιστών είναι μια άλλη κοινή στρατηγική για την αποφυγή ανίχνευσης από το ανοσοποιητικό σύστημα. Στον HIV, το περίβλημα που καλύπτει το ιοσωμάτιο σχηματίζεται από την εξωτερική μεμβράνη του κυττάρου ξενιστή. Αυτοί οι “αυτοκάλυπτοι” ιοί δυσκολεύουν το ανοσοποιητικό σύστημα να τους αναγνωρίσει ως δομές “non-self”.
Ιστορία της ανοσολογίας
Η ανοσολογία είναι μια επιστήμη που εξετάζει τη δομή και τη λειτουργία του ανοσοποιητικού συστήματος. Προέρχεται από την ιατρική και τις πρώτες μελέτες σχετικά με τις αιτίες της ανοσίας στις ασθένειες. Η παλαιότερη γνωστή αναφορά στην ανοσία ήταν κατά τη διάρκεια της πανώλης των Αθηνών το 430 π.Χ. Ο Θουκυδίδης σημείωνε ότι οι άνθρωποι που είχαν αναρρώσει από μια προηγούμενη περίοδο της νόσου μπορούσαν να νοσηλεύσουν τους άρρωστους χωρίς να ασθενήσουν από την ασθένεια για δεύτερη φορά. Κατά τον 18ο αιώνα, ο Pierre-Louis Moreau de Maupertuis πραγματοποίησε πειράματα με δηλητήριο σκορπιού και διαπίστωσε ότι ορισμένα σκυλιά και ποντίκια ήταν άνοσα σε αυτό το δηλητήριο. Κατά τον 10ο αιώνα, ο Πέρσης ιατρός al-Razi (γνωστός επίσης ως Rhazes) έγραψε την πρώτη καταγεγραμμένη θεωρία της επίκτητης ανοσίας, σημειώνοντας ότι μια περίοδος ευλογιάς προστατεύει τους επιζώντες από μελλοντικές λοιμώξεις. Παρόλο που εξήγησε την ασυλία από την άποψη της “υπερβολικής υγρασίας” που εξωθήθηκε από το αίμα (και επομένως απέτρεψε την εμφάνιση της νόσου για δεύτερη φορά) αυτή η θεωρία εξήγησε πολλές παρατηρήσεις σχετικά με την ευλογιά που ήταν γνωστές εκείνη την στιγμή.
Αυτές και άλλες παρατηρήσεις της επίκτητης ανοσίας χρησιμοποιήθηκαν αργότερα από τον Louis Pasteur στην εξέλιξη του εμβολιασμού και την προτεινόμενη βλαστική θεωρία της νόσου. Η θεωρία του Παστέρ ήταν σε άμεση αντίθεση με τις σύγχρονες θεωρίες για την νόσο, όπως η θεωρία του μιάσματος. Δεν ήταν παρά μόνο όταν επιβεβαιώθηκαν τα αποδεικτικά στοιχεία από τον Robert Koch το 1891, για τα οποία του απονεμήθηκε το βραβείο Νόμπελ το 1905, ότι οι μικροοργανισμοί επιβεβαιώθηκαν ως αιτία της λοιμώδους νόσου. Οι ιοί επιβεβαιώθηκαν ως ανθρώπινα παθογόνα το 1901, με την ανακάλυψη του ιού του κίτρινου πυρετού από τον Walter Reed.
Η ανοσολογία έκανε μια μεγάλη πρόοδο προς τα τέλη του 19ου αιώνα, μέσα από ταχείες εξελίξεις, στη μελέτη της χυμικής ανοσίας και της κυτταρικής ανοσίας. Ιδιαίτερα σημαντική ήταν η εργασία του Paul Ehrlich, ο οποίος πρότεινε την θεωρία πλευρικής αλυσίδας για να εξηγήσει την εξειδίκευση της αντίδρασης αντιγόνου-αντισώματος. Οι συνεισφορές του στην κατανόηση της χυμικής ανοσίας αναγνωρίστηκαν με την απονομή βραβείου Νόμπελ το 1908, το οποίο απονεμήθηκε από κοινού με τον ιδρυτή της κυτταρικής ανοσολογίας, Elie Metchnikoff.
Θεωρητικές προσεγγίσεις στο ανοσοποιητικό σύστημα
Η ανοσολογία είναι έντονα πειραματική στην καθημερινή πρακτική, αλλά χαρακτηρίζεται επίσης από μια συνεχιζόμενη θεωρητική στάση. Πολλές θεωρίες έχουν προταθεί στην ανοσολογία από το τέλος του δέκατου ένατου αιώνα μέχρι σήμερα. Στα τέλη του 19ου αιώνα και στις αρχές του 20ού αιώνα παρατηρήθηκε μια μάχη ανάμεσα στις “κυτταρικές” και τις “χυμικές” θεωρίες της ανοσίας. Σύμφωνα με την κυτταρική θεωρία της ανοσίας, που εκπροσωπείται ιδιαίτερα από τον Elie Metchnikoff, είναι τα κύτταρα (ακριβέστερα τα φαγοκύτταρα) που είναι υπεύθυνα για τις ανοσολογικές αντιδράσεις. Αντίθετα, η χυμική θεωρία της ανοσίας, η οποία καθιερώθηκε, μεταξύ άλλων, από τους Robert Koch και Emil von Behring, δηλώνει ότι οι ενεργοί ανοσοποιητικοί παράγοντες είναι διαλυτά συστατικά (μόρια) που υπάρχουν στους “χυμούς” (εξ’ ου και το χυμική) του οργανισμού και όχι στα κύτταρα του.
Στα μέσα της δεκαετίας του 1950, ο Frank Burnet, εμπνευσμένος από μια πρόταση του Niels Jerne, διατύπωσε τη θεωρία της κλωνικής επιλογής (clonal selection theory, CST) της ανοσίας. Με βάση την CST, ο Burnet ανέπτυξε μια θεωρία για το πώς ενεργοποιείται μια ανοσοαπόκριση σύμφωνα με την διάκριση “self/non-self”. Τα “self” συστατικά (τα συστατικά του σώματος) δεν προκαλούν καταστροφικές ανοσολογικές αποκρίσεις, ενώ οι “non-self” οντότητες (παθογόνα, ένα αλλομόσχευμα) προκαλούν καταστροφική ανοσοαπόκριση. Η θεωρία τροποποιήθηκε αργότερα για να αντικατοπτρίζει τις νέες ανακαλύψεις που σχετίζονται με την ιστοσυμβατότητα ή την πολύπλοκη ενεργοποίηση διπλής σηματοδότησης (“two-signal”) των Τ λεμφοκυττάρων. Η “self/non-self” θεωρία της ανοσίας και το “self/non-self” λεξιλόγιο έχουν επικριθεί, αλλά παραμένουν να έχουν πολύ επιρροή.
Πιο πρόσφατα, έχουν προταθεί αρκετά θεωρητικά πλαίσια στην ανοσολογία, συμπεριλαμβανομένων των απόψεων της “αυτοπάθειας” (“autopoietic”), της “γνωστικής ανοσίας” (“cognitive immune”), του “μοντέλου κινδύνου” (“danger model”) (ή της “θεωρίας κινδύνου”/ “danger theory”) και της “ασυνέχειας” (“discontinuity”). Το μοντέλο κινδύνου, που προτάθηκε από τον Polly Matzinger και τους συναδέλφους του, έχει μεγάλη επιρροή, προκαλώντας πολλά σχόλια και συζητήσεις.
Βιβλιογραφικές αναφορές