(Αναδημοσίευση με μετάφραση από: Marijuana Doctors, “Medical Marijuana for Myasthenia Gravis” https://www.marijuanadoctors.com/conditions/myasthenia-gravis/
Medical content reviewed by Dr. Joseph Rosado, MD, M.B.A, Chief Medical Officer, Updated on June 15, 2020)
Με την κοινή γνώμη στις ΗΠΑ να αλλάζει θετικά ως προς την ιατρική χρήση της κάνναβης, οι ερευνητές μελετούν πώς αυτή η ελεγχόμενη και ρυθμιζόμενη ουσία (κανονικά είναι όλο το φυτό με τις πολλές χημικές του ενώσεις) μπορεί να λειτουργήσει για τηn θεραπεία μιας ποικιλίας από ασθένειες. Συγκεκριμένα, μία ασθένεια που μελετάται τώρα είναι η Μυασθένεια Gravis (Myasthenia Gravis, MG), ICD-10 G-70 Myasthenia gravis and other myoneural disorders / Βαρεία μυασθένεια και άλλες νευρομυϊκές διαταραχές. Οι ερευνητές βρίσκουν ότι η κάνναβη για την μυασθένεια gravis είναι χρήσιμη για την θεραπεία ενός ευρέος φάσματος συμπτωμάτων που συνοδεύουν την ασθένεια.
Τι είναι η μυασθένεια gravis;
Η MG είναι μια αυτοάνοση ασθένεια που κάνει τους μυς μας αδύναμους. Το όνομά της προήλθε από λατινικές και ελληνικές λέξεις που σημαίνουν “σοβαρή μυϊκή αδυναμία” (grave muscle weakness). Ωστόσο, σε πολλές περιπτώσεις, η ασθένεια δεν είναι τόσο “σοβαρή” όπως υποδηλώνει το όνομα της και οι περισσότεροι ασθενείς με MG μπορούν να ζήσουν μια σχετικά φυσιολογική ζωή.
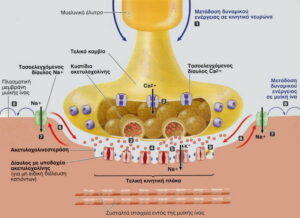
Η πάθηση της μυασθένειας gravis οφείλεται σε ανεπαρκή ποσότητα υποδοχέων ακετυλοχολίνης(*) στη μετασυναπτική μεμβράνη μας στις νευρομυϊκές συνάψεις μας, εκεί που ενώνονται / επικοινωνούν τα νεύρα με τους μύες. Αυτό οδηγεί σε μυϊκή αδυναμία. Τόσο οι επίκτητες όσο και οι συγγενείς μορφές της MG εμφανίζονται και σε γάτες και σε σκύλους και σε ανθρώπους.
(*) “Η ακετυλοχολίνη είναι ένας νευροδιαβιβαστής, μια βιολογικά ενεργή (βιογενής) αμίνη. Νευροδιαβιβαστές ονομάζονται οι χημικές ενώσεις, οι οποίες χρησιμεύουν στη μεταβίβαση πληροφοριών από έναν νευρώνα στον επόμενο. Η ηλεκτρική διέγερση που φτάνει στον νευράξονα οδηγεί στην απελευθέρωση του νευροδιαβιβαστή από τον προσυναπτικό νευρώνα στο συναπτικό κενό, όπου μπορεί να δράσει στους ανάλογους υποδοχείς που βρίσκονται στο μετασυναπτικό νευρώνα. Με αυτόν τον τρόπο η ηλεκτρική ώση μετατρέπεται σε χημική. Η αντίδραση του μετασυναπτικού κυττάρου στον νευροδιαβιβαστή εξαρτάται από τους υποδοχείς που υπάρχουν στη μεμβράνη του”.
Πηγή: “Νευροδιαβιβαστής” https://el.wikipedia.org/wiki/Νευροδιαβιβαστής
Η MG είναι μια διαταραχή στον χώρο μεταξύ των μυών και των νεύρων μας που είναι γνωστή ως νευρομυϊκή σύνδεση / σύναψη. Το νεύρο αποκρίνεται σε ένα ηλεκτρικό σήμα και απελευθερώνει νευροδιαβιβαστές που διασχίζουν αυτήν την περιοχή για να ενεργοποιήσουν τις κινήσεις των μυών μας.
Επειδή η MG είναι μια αυτοάνοση διαταραχή, ουσιαστικά το ανοσοποιητικό μας σύστημα επιτίθεται στον ίδιο μας τον εαυτό. Εξαιτίας αυτού, οι υποδοχείς μας στους νευροδιαβιβαστές ακετυλοχολίνης μειώνονται σε λειτουργία και αριθμό. Δεδομένου ότι ο μυς δεν λαμβάνει πλέον τα κατάλληλα σήματα όταν έχουμε MG, αυτό έχει ως συνέπεια ο ασθενής να αντιμετωπίζει αδυναμία στους μύες (εξασθένιση).
Ιστορικό της μυασθένειας gravis
Το περιοδικό Neuromuscular Disorder[1], που αναφέρθηκε από τα National Institutes of Health, παρέχει ένα πρώιμο χρονοδιάγραμμα της ιστορίας της MG. Η MG αναγνωρίστηκε για πρώτη φορά από έναν ιατρό της Οξφόρδης τον 17ο αιώνα, τον Thomas Willis, ο οποίος την θεωρούσε ως μια ξεχωριστή κλινική οντότητα.
[1] Trevor Hughes “The early history of myasthenia gravis” (Η πρώιμη ιστορία της μυασθένειας gravis) Neuromuscul Disord. 2005 Dec;15(12):878-86.
https://pubmed.ncbi.nlm.nih.gov/16289896/
Περίληψη
“Η μυασθένεια gravis αναγνωρίστηκε για πρώτη φορά ως ξεχωριστή κλινική οντότητα από τον Thomas Willis, ιατρό της Οξφόρδης του 17ου αιώνα, που η αναφορά το 1672 στα Λατινικά είχε περάσει σε μεγάλο βαθμό απαρατήρητη μέχρι το 1903. Η πρώτη σύγχρονη περιγραφή έγινε το 1877 από τον Samuel Wilks, γιατρό του Λονδίνου. Προς το τέλος του 19ου αιώνα, οι πρωτογενείς μυϊκές ασθένειες και οι ασθένειες που οφείλονται στην ατροφία των μυών μελετήθηκαν από Άγγλους, Γάλλους και Γερμανούς γιατρούς. Οι πρώτες πλήρεις περιγραφές της μυασθένειας gravis ήταν από τον Wilhelm Erb, της Χαϊδελβέργης και τον Samuel Goldflam της Βαρσοβίας. Οι αναφορές του Willis και η βιβλιογραφία του 19ου αιώνα για τη μυασθένεια gravis εξετάζονται, αποκαλύπτοντας την κυριαρχία των Γερμανών ιατρών και νευροπαθολόγων στην πρώιμη κατανόηση της νόσου. Περιγράφεται η εξέλιξη της παθολογίας, της αιτιολογίας και της θεραπείας στο πρώτο μισό του 20ού αιώνα”.
Το 1877, ένας γιατρός στο Λονδίνο, ο Samuel Wilks, έγραψε την πρώτη σύγχρονη περιγραφή. Γύρω στα τέλη του 19ου αιώνα, οι πρωτογενείς ασθένειες των μυών και οι ασθένειες που προκλήθηκαν από την ατροφία των μυών μελετήθηκαν από Άγγλους, Γερμανούς και Γάλλους γιατρούς.
Ο Samuel Goldflam στην Βαρσοβία και ο Wilhelm Erb στην Χαϊδελβέργη δημοσίευσαν τις πρώτες πλήρεις περιγραφές της διαταραχής. Οι αναφορές του Willis και η βιβλιογραφία για την MG του 19ου αιώνα, αποκαλύπτουν την επίδραση των Γερμανών νευροπαθολόγων και ιατρών στην πρώιμη κατανόηση της νόσου. Οι γιατροί περιέγραψαν την εξέλιξη της αιτιολογίας, της παθολογίας και της θεραπείας της κατάστασης στο πρώτο μισό του 20ου αιώνα.
Τα συμπτώματα της μυασθένειας gravis
Αν και η MG μπορεί να επηρεάσει οποιονδήποτε σκελετικό μυ, οι μύες που ελέγχουν την κίνηση των βλεφάρων και των ματιών μας, την κατάποση και την έκφραση του προσώπου επηρεάζονται περισσότερο. Η διαταραχή μπορεί να εμφανιστεί ξαφνικά και τα συμπτώματά της συχνά δεν αναγνωρίζονται αμέσως ως συμπτώματα της MG.

Συχνά, η αδυναμία των μυών των ματιών είναι το πρώτο αισθητό σύμπτωμα. Μερικές φορές, η μειωμένη ομιλία και η δυσκολία στην κατάποση μπορεί να είναι τα πρώτα συμπτώματα που προκύπτουν. Κάθε άτομο είναι μοναδικό στον βαθμό της μυϊκής αδυναμίας του στην MG και μπορεί να κυμαίνεται από οφθαλμική μυασθένεια, εντοπισμένη μορφή που περιορίζεται στους μυς του ματιού, έως μια γενικευμένη ή σοβαρή μορφή όπου επηρεάζει πολλούς από τους μύες, συμπεριλαμβανομένων των μυών που ελέγχουν την αναπνοή.
Ενώ δεν υπάρχει επί του παρόντος θεραπεία για την MG, η όποια θεραπεία μπορεί να βοηθήσει στην ανακούφιση των συμπτωμάτων της πάθησης, όπως:
* Αδυναμία των μυών του βραχίονα ή των ποδιών
* Διπλή όραση
* Βλεφαρόπτωση
* Δυσκολίες στην ομιλία
* Μάσημα
* Κατάποση
* Αναπνοή
Η επίπτωση της νόσου είναι συνήθως περίπου 3 έως 30 περιπτώσεις ανά εκατομμύριο ετησίως και συνεχίζει να αυξάνεται ως αποτέλεσμα της αυξημένης ευαισθητοποίησης.
Υπάρχουν παράγοντες που μπορούν να προκαλέσουν ή να επιδεινώσουν τις παροξύνσεις της MG, όπως:
* Μια χειρουργική επέμβαση
* Ένα συναισθηματικό στρες
* Το φωτεινό ηλιακό φως
* Μια τρέχουσα ασθένεια (πχ. ιογενής λοίμωξη)
* Μια ανοσοποίηση
* Η εμμηνόρροια
* Φάρμακα (πχ. σιπροφλοξασίνη, αμινογλυκοσίδες, προκαΐνη, χλωροκίνη, λίθιο, προκαϊναμίδη, βήτα-αποκλειστές και στατίνες)
Ο γιατρός θα φτάσει σε μια διάγνωση MG ρωτώντας τον ασθενή για τα συμπτώματά του και πραγματοποιώντας μια φυσική και νευρολογική εξέταση. Οι ειδικές εξετάσεις που μπορεί να κάνει ο γιατρός περιλαμβάνουν:
* Έλεγχος για μυϊκή αδυναμία
* Δοκιμή των αντανακλαστικών
* Παρατήρηση του μυϊκού τόνου
* Μελέτη του συντονισμό των μυών
* Εξέταση της κίνησης των ματιών
* Δοκιμή των αισθήσεων του σώματος
* Παρακολούθηση των λειτουργιών της κίνησης, όπως το άγγιγμα της μύτης με το δάχτυλο
* Διεξαγωγή εξετάσεων απεικόνισης του θώρακα, όπως αξονική τομογραφία ή μαγνητική τομογραφία, για έλεγχο ύπαρξης όγκου
* Εκτέλεση επαναληπτικής δοκιμής διέγερσης νεύρων
* Δοκιμή του αίματος σας για αντισώματα που σχετίζονται με MG
* Διεξαγωγή δοκιμής εφελκυσμού
* Δοκιμή της λειτουργίας των πνευμόνων
Ο γιατρός μπορεί να εκτελέσει ηλεκτρομυογραφία μίας ίνας ή EMG, εάν άλλες εξετάσεις δεν καταλήξουν σε διάγνωση της μυασθένειας gravis. Το EMG θεωρείται ένα από τα πιο ευαίσθητα τεστ για την MG και μπορεί να είναι επωφελές για την διάγνωση ακόμη και των ήπιων περιπτώσεων της MG.
Επιδράσεις της μυασθένειας gravis
Παρόλο που οι επιπλοκές της MG είναι σχετικά αντιμετωπίσιμες, μερικές μπορεί να είναι απειλητικές για την ζωή.
Οι επιπλοκές που σχετίζονται με την MG μπορεί να περιλαμβάνουν:
* Μια απειλητική για τη ζωή κατάσταση, γνωστή ως μυασθενική κρίση (myasthenic crisis), που μπορεί να επηρεάσει την αναπνοή του πάσχοντα. Αυτό απαιτεί άμεση θεραπεία ώστε να μπορεί να αναπνέει από μόνος του.
* Όγκοι του θύμου αδένα, αν και δεν είναι συνήθως καρκινικοί, εμφανίζονται σε περίπου στο 15% των ατόμων με MG.
* Υπερδραστήριος ή ανενεργός θυρεοειδής και Λύκος (ΣΕΛ), ρευματοειδής αρθρίτιδα και άλλες αυτοάνοσες διαταραχές.
Στατιστικές γα την μυασθένεια gravis
Περίπου 20 άτομα στα 100.000[2], στις ΗΠΑ ζουν με MG, σύμφωνα με το Myasthenia Gravis Foundation of America.
[2] “WHAT IS MG?” (Τι είναι η MG;) https://myasthenia.org/What-is-MG/FAQs

Άλλες στατιστικές για την MG που αναφέρθηκαν από το National Institute of Neurological Disorders and Stroke (NINDS)[3] αποκαλύπτουν ότι:
* Η MG συνήθως επηρεάζει τις ενήλικες γυναίκες κάτω των 40 ετών και τους άνδρες άνω των 60 ετών. Ωστόσο, μπορεί να επηρεάσει οποιονδήποτε σε οποιαδήποτε ηλικία, συμπεριλαμβανομένων και παιδιών.
* Περίπου το 20% των ατόμων με MG αντιμετωπίζουν μυασθενική κρίση τουλάχιστον μία φορά.
[3] “Myasthenia Gravis Fact Sheet” (Ενημερωτικό δελτίο στοιχείων για την μυασθένεια gravis) https://www.ninds.nih.gov/Disorders/Patient-Caregiver-Education/Fact-Sheets/Myasthenia-Gravis-Fact-Sheet
Τρέχουσες διαθέσιμες θεραπείες για την μυασθένεια gravis
Μπορούν να ελεγχθούν τα συμπτώματα της MG μέσω θεραπειών που βοηθούν στην μείωση και την βελτίωση της μυϊκής αδυναμίας. Αυτές περιλαμβάνουν:
Θυμεκτομή
Αυτή είναι μια χειρουργική επέμβαση που περιλαμβάνει την αφαίρεση του θύμου αδένα. Η θυμεκτομή μπορεί να μειώσει τα συμπτώματα της MG. Μπορεί ακόμη και να θεραπεύσει από τα συμπτώματα της ασθένειας εξισορροπώντας εκ νέου το ανοσοποιητικό σύστημα.
Σύμφωνα με μια πρόσφατη μελέτη που χρηματοδοτήθηκε από το NINDS, η θυμεκτομή είναι ευεργετική για άτομα με θύμωμα (thymoma, το πλέον κοινό νεόπλασμα του θύμου αδένα αλλά και ολόκληρου του μεσοθωρακίου) και άτομα που δεν έχουν ενδείξεις όγκων. Αυτή η κλινική δοκιμή εξέτασε 126 ασθενείς με MG χωρίς ορατό θύμωμα. Τα αποτελέσματα της μελέτης έδειξαν ότι η χειρουργική επέμβαση μείωσε την ανάγκη για ανοσοκατασταλτικά φάρμακα και μείωσε την μυϊκή αδυναμία.
Δεδομένου ότι πρόκειται για μια σημαντική χειρουργική επέμβαση, υπάρχουν ορισμένοι κίνδυνοι που πρέπει να γνωρίζει ο ασθενής, όπως:
* Αιμορραγία
* Μετεγχειρητικές λοιμώξεις
* Κατάρρευση πνεύμονα
Μπορεί επίσης να υπάρχει η αίσθηση πόνου στο σημείο της τομής και στην πλάτη. Λόγω του άγχους της χειρουργικής επέμβασης και της αναισθησίας, μπορεί επίσης να να υπάρξει αδυναμία μετά την επέμβαση. Επιπλέον, εάν υπάρχουν και άλλα ιατρικά προβλήματα, ενδέχεται να υπάρξουν και περισσότερες επιπλοκές.
Πλασμαφαίρεση και ενδοφλέβια ανοσοσφαιρίνη
Εάν πρόκειται για σοβαρή περίπτωση MG, αυτές οι δύο θεραπείες θα μπορούσαν να είναι μια επιλογή. Ο ασθενής μπορεί να έχει αντισώματα στο πλάσμα του που προσβάλλουν τις νευρομυϊκές συνάψεις. Αυτές οι δύο θεραπείες βοηθούν στην εξάλειψη των καταστρεπτικών αντισωμάτων. Ωστόσο, τα αποτελέσματά τους συχνά διαρκούν μόνο για αρκετές εβδομάδες έως μήνες.
Η πλασμαφαίρεση είναι μια διαδικασία που χρησιμοποιεί μια μηχανή για να απαλλάξει το πλάσμα στο αίμα από τα επιβλαβή αντισώματα και να τα αντικαταστήσει με ένα υποκατάστατο πλάσματος ή με ένα υγιές πλάσμα.
Οι συχνές ανεπιθύμητες παρενέργειες της πλασμαφαίρεσης και της ενδοφλέβιας ανοσοσφαιρίνης μπορεί να περιλαμβάνουν:
* Κόπωση
* Ναυτία
* Ζάλη
* Μείωση της αρτηριακής πίεσης
Η ενδοφλέβια ανοσοσφαιρίνη είναι μια ένεση υψηλής συγκέντρωσης αντισωμάτων από υγιείς δότες που αλλάζουν τον τρόπο λειτουργίας του ανοσοποιητικού συστήματος του ασθενή προσωρινά. Συνδέεται με τα αντισώματα που προκαλούν την MG και τα εξαλείφει από την κυκλοφορία.
Οι συχνές ανεπιθύμητες παρενέργειες της ενδοφλέβιας ανοσοσφαιρίνης μπορεί να είναι:
* Πονοκέφαλος
* Κοκκίνισμα
* Μυϊκές κράμπες
* Ζάλη
* Πυρετός
* Πόνος στις αρθρώσεις / στην πλάτη
* Ρίγη
* Ναυτία
* Έμετος
Εάν αντιμετωπίσεις κάποιο από αυτά τα συμπτώματα για μεγάλο χρονικό διάστημα ή εάν υπάρξει επιδείνωση τους, θα πρέπει να συμβουλευτείς τον γιατρό σου. Μπορεί επίσης να αντιμετωπίσεις κάποια ερυθρότητα, πρήξιμο και πόνο στο σημείο της ένεσης.
Ανοσοκατασταλτικά φάρμακα
Τα ανοσοκατασταλτικά φάρμακα καταστέλλουν την ανώμαλη παραγωγή αντισωμάτων και βελτιώνουν την μυϊκή δύναμη. Αυτά τα φάρμακα μπορεί να είναι αζαθειοπρίνη, πρεδνιζόνη, ριτουξιμάμπη, τακρόλιμους και μυκοφαινολάτη (azathioprine, prednisone, rituximab, tacrolimus and mycophenolate, αντίστοιχα).
Οι παρενέργειες των ανοσοκατασταλτικών φαρμάκων ποικίλλουν σημαντικά για κάθε διαφορετικό ανοσοκατασταλτικό φάρμακο από τα πολλά που διατίθενται. Οι συχνές ανεπιθύμητες παρενέργειες μπορεί να περιλαμβάνουν:
* Πρόβλημα ούρησης
* Ρίγη ή πυρετός
* Πόνος χαμηλά στην πλάτη
* Συχνή ούρηση
* Επώδυνη ούρηση
* Ασυνήθιστη αδυναμία ή κόπωση
Φάρμακα αντιχολινεστεράσης
Αυτά τα φάρμακα περιλαμβάνουν παράγοντες αντιχολινεστεράσης, όπως ρεγκονόλη ή mestinon και αργή διάσπαση της ακετυλοχολίνης στις νευρομυϊκές συνάψεις, βοηθώντας στην αύξηση της μυϊκής δύναμης και στην βελτίωση της νευρομυϊκής μετάδοσης.
Οι παρενέργειες των φαρμάκων κατά της αντιχολινεστεράσης μπορεί να είναι:
* Πονοκέφαλος
* Διάρροια
* Ναυτία
* Έμετος
* Αϋπνία
* Έλλειψη όρεξης
* Κοιλιακό άλγος
* Αργός καρδιακός παλμός
* Κιτρινισμένο δέρμα
* Αδυναμία
* Ξαφνική ή σημαντική απώλεια βάρους
Αλλαγές στον τρόπο ζωής
Κάποιος μπορεί να βοηθηθεί στην ανακούφιση των συμπτωμάτων από την MG με μερικές αλλαγές στον τρόπο ζωής, όπως:
* Ξεκούραση για να μειωθεί η αδυναμία των μυών
* Καλύπτρα στο ένα μάτι εάν ενοχλεί η διπλή όραση
* Αποφυγή στην έκθεση σε θερμότητα και σε άγχος καθώς και τα δύο μπορεί να επιδεινώσουν τα συμπτώματα
Με οποιαδήποτε από τις παραπάνω θεραπείες, τα συμπτώματα θα βελτιωθούν. Μπορεί ακόμη και να υποχωρήσουν τόσο ώστε δεν θα χρειάζεσαι πλέον θεραπεία.
Η ιατρική χρήση της κάνναβης για την μυασθένεια gravis
Ως εναλλακτική λύση, η ιατρική χρήση της κάνναβης είναι μια εξαιρετική μορφή φαρμάκου για τους πάσχοντες από MG. Τα ενεργά συστατικά της κάνναβης μπορούν να οδηγήσουν σε μείωση των συναισθημάτων άγχους και στρες και ακόμη και στην μείωση του χρόνιου πόνου. Η ιατρική χρήση της κάνναβης επιτρέπει επίσης στους μυς του ασθενούς να χαλαρώσουν και να λειτουργήσουν με τον κατάλληλο και λειτουργικό τρόπο.

Οι παρενέργειες της ιατρικής χρήσης της κάνναβης για τη μυασθένεια gravis είναι ήπιες και μπορεί να περιλαμβάνουν:
* Ξηρά ή κόκκινα μάτια[4]
* Ξηροστομία[5]
* Ζάλη[6]
* Ναυτία
* Έμετος
* Μούδιασμα
* Πονοκέφαλο
[4] “Red Eyes” (Κόκκινα μάτια (παρενέργειες κάνναβης)) https://cannalib.eu/red_eyes_side_effects/
[5] “Dry Mouth and Thirst” (Ξηροστομία και Δίψα (παρενέργειες κάνναβης)) https://cannalib.eu/dry_mouth_and_thirst_side_effects/
[6] “Dizziness” (Ζάλη) https://www.marijuanadoctors.com/side-effects/dizziness/
Πώς και γιατί η κάνναβη είναι μια αποτελεσματική θεραπεία για την μυασθένεια gravis
Η φαρμακευτική κάνναβη, όπως οι παράγοντες ακετυλοχολινεστεράσης, μπορεί να αναστείλει την ακετυλοχολινεστεράση, το ένζυμο που είναι υπεύθυνο για την αποικοδόμηση της ακετυλοχολίνης. Εμποδίζοντας την ακετυλοχολινεστεράση, υπάρχει περισσότερος χρόνος για την αλληλεπίδραση της ακετυλοχολίνης με τον υποδοχέα της πριν από την ολοκλήρωση του κύκλου λειτουργίας και την αποκομιδή της. Αυτό μπορεί να βοηθήσει στην υπερνίκηση του αποκλεισμένου υποδοχέα που προκαλεί τις συστολές των μυών.
Πολλαπλά κανναβινοειδή έχουν αποδειχθεί αποτελεσματικά στην αύξηση των επιπέδων της ακετυλοχολίνης και στην επιβράδυνση της ολοκλήρωσης του κύκλου εργασίας της ακετυλοχολίνης. Μία μελέτη[7] που δημοσιεύτηκε στο Molecular Pharmaceutics διαπίστωσε ότι η THC, το κύριο κανναβινοειδές στην κάνναβη, εμπόδισε πλήρως την ακετυλοχολινεστεράση και αύξησε τα επίπεδα του νευροδιαβιβαστή. Άλλες μελέτες[8][9] έδειξαν την αποτελεσματικότητα των CBD και THC στη μείωση του ποσοστού αποκομιδής της ακετυλοχολίνης.
[7] Lisa M Eubanks, Claude J Rogers, Albert E Beuscher IV, George F Koob, Arthur J Olson, Tobin J Dickerson, Kim D Janda “A Molecular Link Between the Active Component of Marijuana and Alzheimer’s Disease Pathology” (Ένας μοριακός δεσμός μεταξύ του ενεργού συστατικού της κάνναβης και της παθολογίας στην Νόσο του Alzheimer) Mol Pharm. 2006;3(6):773–777.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2562334/
Περίληψη
“Η Νόσος του Alzheimer είναι η κύρια αιτία άνοιας μεταξύ των ηλικιωμένων και με το συνεχώς αυξανόμενο μέγεθος αυτού του πληθυσμού, οι περιπτώσεις της Νόσου του Alzheimer αναμένεται να τριπλασιαστούν τα επόμενα 50 χρόνια. Κατά συνέπεια, η ανάπτυξη θεραπειών που επιβραδύνουν ή σταματούν την εξέλιξη της νόσου έχουν καταστεί επιτακτική ανάγκη τόσο για τη βελτίωση της ποιότητας ζωής των ασθενών όσο και για τη μείωση του κόστους υγειονομικής περίθαλψης που οφείλεται στη Νόσο του Alzheimer. Εδώ, αποδεικνύουμε ότι το δραστικό συστατικό της κάνναβης, η Δ9-τετραϋδροκανναβινόλη (THC), αναστέλλει ανταγωνιστικά το ένζυμο ακετυλοχολινεστεράση (AChE), καθώς επίσης και αποτρέπει τη συσσώρευση αμυλοειδούς β-πεπτιδίου (Αβ) που προκαλείται από το AChE, τον βασικό παθολογικό δείκτη της Νόσου του Alzheimer. Η υπολογιστική μοντελοποίηση της αλληλεπίδρασης THC-AChE αποκάλυψε ότι η THC συνδέεται στην περιφερειακή ανιονική θέση του AChE, την κρίσιμη περιοχή που εμπλέκεται στην αμυλοειδογένεση. Σε σύγκριση με τα επί του παρόντος εγκεκριμένα φάρμακα που συνταγογραφούνται για τη θεραπεία της Νόσου του Alzheimer, η THC είναι ένας πολύ ανώτερος αναστολέας της συσσώρευσης Αβ και αυτή η μελέτη παρέχει έναν προηγουμένως μη αναγνωρισμένο μοριακό μηχανισμό μέσω του οποίου τα μόρια κανναβινοειδών μπορούν να επηρεάσουν άμεσα την εξέλιξη αυτής της εξουθενωτικής ασθένειας”.
[8] AV Revuelta, F Moroni, DL Cheney, E Costa “Effect of cannabinoids on the turnover rate of acetylcholine in rat hippocampus, striatum and cortex” (Επίδραση των κανναβινοειδών στο ποσοστό του κύκλου εργασίας της ακετυλοχολίνης στον ιππόκαμπο αρουραίου, στο ραβδωτό σώμα και στον φλοιό) Naunyn Schmiedebergs Arch Pharmacol. 1978 Sep;304(2):107-10.
https://pubmed.ncbi.nlm.nih.gov/703853/
Περίληψη
“Μελετήθηκαν οι επιδράσεις της δέλτα9-τετραϋδροκανναβινόλης (δέλτα9-THC), της κύριας ψυχοδραστικής ένωσης της κάνναβης και της κανναβιδιόλης (CBD), ενός μη ψυχοδραστικού συστατικού, στη συγκέντρωση της ακετυλοχολίνης (ACh) και του ποσοστού του κύκλου εργασίας της ACh (TRACh), σε διάφορες περιοχές του εγκεφάλου αρουραίου. Ούτε οι δόσεις δέλτα9-THC από 0,2 έως 10mg/kg ούτε η CBD (10 ή 20mg/kg) μεταβάλλουν τη συγκέντρωση ACh στις περιοχές του εγκεφάλου που εξετάστηκαν 30 λεπτά, μετά την ενδοφλέβια ένεση. Ωστόσο, η δέλτα 9-THC (δόσεις από 0,2 έως 10mg/kg) προκαλεί σημαντική μείωση του TRACh στον ιππόκαμπο ενώ η CBD δεν έχει αποτέλεσμα σε αυτήν την περιοχή του εγκεφάλου ακόμη και όταν χορηγούνται 20mg/kg. Επιπλέον, υψηλές δόσεις δέλτα9-THC (5mg/kg) και CBD (20mg/kg) που προκαλούν σημαντική μείωση του TRACh στο ραβδωτό σώμα αποτυγχάνουν να αλλάξουν το TRACh στον βρεγματικό φλοιό. Οι χαμηλές δόσεις της δέλτα9-THC που απαιτούνται για τη μείωση του TRACh στον ιππόκαμπο, υποδηλώνουν ότι μια δράση σε αυτούς τους χολινεργικούς μηχανισμούς μπορεί να παίζει ρόλο στην ψυχομιμητική δραστηριότητα της δέλτα9-THC”.
[9] HL Tripathi, FJ Vocci, DA Brase, WL Dewey “Effects of cannabinoids on levels of acetylcholine and choline and on turnover rate of acetylcholine in various regions of the mouse brain” (Επιδράσεις των κανναβινοειδών στα επίπεδα της ακετυλοχολίνης και της χολίνης και στο ποσοστό του κύκλου εργασίας της ακετυλοχολίνης σε διάφορες περιοχές του εγκεφάλου του ποντικού) Alcohol Drug Res. 1987;7(5-6):525-32.
https://pubmed.ncbi.nlm.nih.gov/3620017/
Περίληψη
“Τα ψυχοδραστικά κανναβινοειδή, δέλτα9-τετραϋδροκανναβινόλη (δέλτα9-THC), δέλτα8-τετραϋδροκανναβινόλη (δέλτα8-THC), 11-υδροξυ-δέλτα 9-τετραϋδροκανναβινόλη (11-ΟΗ-δέλτα9-THC) και 9-nor-9 beta-hydroxyhexahydrocannabinol (beta-HHC), καθώς και τα μη ψυχοδραστικά κανναβινοειδή, κανναβινόλη (CBN), κανναβιδιόλη (CBD), ανώμαλη CBD, δέλτα 8-THC μεθυλαιθέρας (1-OCH3-δέλτα 8-THC) και 9-nor-9 alpha-hydroxyhexahydrocannabinol (alpha-HHC), χρησιμοποιήθηκαν για την αξιολόγηση του ρόλου των χολινεργικών μηχανισμών στις διάφορες συμπεριφορικές δράσεις αυτών των κανναβινοειδών. Τα αποτελέσματά τους στα επίπεδα χολίνης και ακετυλοχολίνης στον εγκέφαλο του ποντικού και στην εναλλαγή ACh προσδιορίστηκαν στον φλοιό, στον ιππόκαμπο, στο ραβδωτό σώμα, στον εγκέφαλο και στον μυελό. Η δέλτα9-THC (30mg/kg) προκάλεσε σημαντική αύξηση της ACh και στις πέντε περιοχές του εγκεφάλου. Η 11-OH-δέλτα9-THC (30mg/kg) αύξησε την ACh στον ιππόκαμπο, στο ραβδωτό σώμα και στον μεσαίο εγκέφαλο. Η δέλτα8-THC (30mg/kg) αύξησε την ACh στον φλοιό και στον ιππόκαμπο. Οι δέλτα9-THC και 11-ΟΗ-δέλτα 9-THC αύξησαν τη χολίνη στον μεσαίο εγκέφαλο και στον φλοιό, ενώ η beta-ΗΗC αύξησε την χολίνη σε όλες τις περιοχές, εκτός από τον ιππόκαμπο, σε δόση 30mg/kg. Επίσης σε αυτήν τη δόση, οι δέλτα9-THC, 11-OH-δέλτα 9-THC, δέλτα8-THC και beta-ΗΗC μείωσαν τον κύκλο εργασίας της ACh στον ιππόκαμπο, όπως και η CBN (10-30mg/kg), η 1-OCH3-δέλτα8-THC (100mg/kg) και η alpha-HHC (100mg/kg). Ο κύκλος εργασίας της ACh μειώθηκε επίσης στον μεσαίο εγκέφαλο με 1-OCH3-δέλτα8-THC και στο ραβδωτό σώμα από alpha-HHC. Έτσι, οι πιο συνεπείς επιδράσεις των κανναβινοειδών, τόσο των ψυχομιμητικών σωματικών όσο και των μη ψυχομιμητικών, ήταν η αύξηση της ACh και η μείωση του κύκλου εργασίας της ACh στον ιππόκαμπο”.
Οι φαρμακολογικές επιδράσεις της CBD οφείλονται στην έμμεση ενεργοποίηση των υποδοχέων από την CBD. Οι επιδράσεις της CBD στους μεταφορείς και τα ένζυμα των νευροδιαβιβαστών φαίνεται να προκαλούνται από έναν μηχανισμό διαφορετικό από την ενεργοποίηση των υποδοχέων, ωστόσο, οι ερευνητές δεν έχουν ακόμη κατανοήσει πλήρως την ακριβή μέθοδο.
Η κάνναβη και τα συμπτώματα της μυασθένειας gravis
Η MG προκαλεί σοβαρή αδυναμία σε διάφορα μέρη του σώματος. Μπορεί να είναι μια πιο γενικευμένη ή εντοπισμένη ασθένεια που προκαλεί γρήγορη κόπωση και αδυναμία.
Με την αποτροπή της κρίσης μυασθένειας, η κάνναβη μπορεί να βοηθήσει με την σοβαρή μορφή της MG, γνωστή ως κρίση μυασθένειας (myasthenia crisis). Χαλαρώνει τους μύες, οπότε έτσι ο ασθενής μπορεί να αποφύγει την υπερπροσπάθεια μιας κρίσης μυασθένειας.
Η κάνναβη αντιμετωπίζει τον πόνο και το άγχος, ανακουφίζοντας το άγχος και τον πόνο που προκαλεί η πάθηση και το πώς επιδεινώνουν την MG. Τα ειδικά καταστήματα διάθεσης της κάνναβης (dispensaries) πωλούν βρώσιμα και συμπυκνώματα που είναι πολύ καλύτερα για κατανάλωση από ότι το κάπνισμα που επιβαρύνει το αναπνευστικό σύστημα. Δεν χρειάζεται ο ασθενής να κάνει χορήγηση με εισπνοή για την θεραπεία της MG. Έτσι μπορεί να κάνει την θεραπεία του πιο εύκολα και πιο διακριτικά.
Η κάνναβης βοηθά με τα συμπτώματα κατάθλιψης. Πολλοί άνθρωποι που πάσχουν από χρόνια νόσο αναπτύσσουν κατάθλιψη, η οποία μπορεί να είναι εξαιρετικά εξουθενωτική και εμποδίζει τον ασθενή να αποτανθεί στα άτομα χρειάζεται για να λάβει την απαραίτητη βοήθεια.
Τα συμπτώματα της κατάθλιψης μπορεί να περιλαμβάνουν:
* Μεγεθυνόμενη θλίψη
* Έλλειψη χαράς
* Απώλεια ενδιαφέροντος για την καθημερινή ζωή
* Συναισθήματα απομόνωσης και κενού
* Απώλεια όρεξης
* Δυσκολία στη λήψη αποφάσεων
* Διαταραχές ύπνου, αϋπνία ή υπερβολικός ύπνος
* Αυτοκτονικές σκέψεις
* Κατήφεια
Δεδομένου ότι το σώμα και το μυαλό μας είναι στενά συνδεδεμένα, η κατάθλιψη μπορεί να επιδεινώσει την MG. Είναι σημαντικό για κάποιον να εργαστεί έτσι ώστε να ξεπεράσει την κατάθλιψή του για να βελτιώσει την συνολική ποιότητα ζωής και υγείας του.
Η κάνναβη βοηθά στην βελτίωση της ομιλίας. Μια δόση κάνναβης με THC-A μπορεί να οδηγήσει σε ταχεία βελτίωση της ομιλίας για τους πάσχοντες από MG.
Η κάνναβη βοηθά στον απογαλακτισμό της χρήσης άλλων φαρμάκων. Το έλαιο κάνναβης βοηθά να αντιμετωπιστούν τα συμπτώματα των αυτοάνοσων ασθενειών. Αφού δοκιμάσει το έλαιο κάνναβης, ένας ασθενής έχει την δυνατότητα να απογαλακτίσει πχ. από ένα φάρμακο πρεδνιζόνης με την μείωση σε 5mg από τα 10mg μέσα σε μερικές εβδομάδες. Δεν θα παρουσιάσει συμπτώματα στέρησης και θα καταφέρει να σταματήσει εντελώς την χρήση πρεδνιζόνης μετά από δύο μήνες περίπου.
Η κάνναβη βοηθά στην βελτίωση της ποιότητας ζωής. Ο ασθενής (όπως αναφέρθηκε παραπάνω) μπορεί επίσης να είναι σε θέση να ζήσει μια καλή ποιότητα ζωής χωρίς τα επιβλαβή στεροειδή φάρμακα και τις παρενέργειες τους. Το έλαιο κάνναβης μπορεί να βοηθήσει επίσης και σε άλλα μέρη του σώματος ενός ασθενούς, όπως στα οστά, στο δέρμα, στα μάτια, στις ορμόνες και στον πόνο.
Η MG είναι μια χρόνια ασθένεια, αλλά μπορεί να αντιμετωπιστεί. Η ιατρική χρήση της κάνναβης είναι μια λύση χωρίς παρενέργειες για την αντιμετώπιση του πόνου και της μυϊκού τόνου που σχετίζεται με αυτήν την κατάσταση.
Οι καλύτερες ποικιλίες κάνναβης για χρήση στην θεραπεία της μυασθένειας gravis
Διάφορες ποικιλίες κάνναβης βοηθούν στο συμπτώματα της MG όπως στον πόνο, στην κόπωση, στο στρες, στον μυϊκό τόνο και στην κατάθλιψη. Παρακάτω αναφέρονται είναι μόνο μερικές από τις πάρα πολλές ποικιλίες που θα μπορούσαν να βοηθήσουν στην ανακούφιση από τα συμπτώματα της MG. Θα πρέπει να μιλήσεις με τον γιατρό σου ή τον ειδικό της κάνναβης σχετικά με το ποια ποικιλία ή ποικιλίες θα σου προσφέρουν τα περισσότερα οφέλη.
* Blue Dream (υβρίδιο): Η Blue Dream βοηθά στην θεραπεία του πόνου, του στρες και της κατάθλιψης που συχνά σχετίζονται με την MG.
* Green Crack (Sativa): Το Green Crack είναι μια καλή ποικιλία για την ανακούφιση όχι μόνο του πόνου και της κατάθλιψης, αλλά λειτουργεί επίσης καλά και για την κόπωση.
* Sour Diesel (Sativa): Μια άλλη χρήσιμη ποικιλία για την ανακούφιση από το άγχος. Λειτουργεί καλά για την κατάθλιψη και την κόπωση.
* Mr. Nice (Indica): Αυτή η ποικιλία λειτουργεί καλά για τον τόνο των μυών. Είναι μια πολύ χαλαρωτική ποικιλία.
* Tessa (Indica): Μια πολύ καλή ποικιλία για οτιδήποτε σχετίζεται με τους μύες.
* Granddaddy Purple (Indica): Ευεργετική για τον πόνο, το άγχος και την έλλειψη όρεξης.
* Cheese (υβρίδιο): Άλλη μια πολύ καλή ποικιλία εάν η κατάθλιψη επηρεάζει την όρεξή σου.
Βρες αυτές και πολλές άλλες χρήσιμες ποικιλίες κάνναβης για να αντιμετωπίσεις τα συμπτώματα της MG και για να βελτιώσεις την ποιότητα της ζωής σου. Αναζήτησε τες σε κάποιο ειδικό κατάστημα ή πάρε μια συνταγή από τον γιατρό σου.
Πληροφορίες σχετικά με την κάνναβη και την μυασθένεια gravis
* “How Medical Marijuana Manages Myasthenia Gravis-Related Muscle Weakness” (Πώς η ιατρική χρήση της κάνναβης διαχειρίζεται την μυϊκή αδυναμία που σχετίζεται με την μυασθένεια gravis) https://www.marijuanadoctors.com/resources/ailment-resources/medical-marijuana-manages-myasthenia-gravis-related-muscle-weakness/
* “Best Cannabis Strains to Manage Myasthenia Gravis Symptoms” (Οι καλύτερες ποικιλίες κάνναβης για την διαχείριση των συμπτωμάτων της μυασθένειας gravis) https://www.marijuanadoctors.com/resources/ailment-resources/best-strains-cannabis-manage-myasthenia-gravis-symptoms/
* “How Cannabis Improves Myasthenia Gravis Patients’ Immune Systems” (Πώς η κάνναβη βελτιώνει το ανοσοποιητικό σύστημα σε ασθενείς με μυασθένεια gravis) https://www.marijuanadoctors.com/resources/ailment-resources/using-medicinal-cannabis-improve-myasthenia-gravis-patients-immune-systems/
* “Myasthenia Gravis Research Studies” (Ερευνητικές μελέτες για την μυασθένεια gravis) https://www.marijuanadoctors.com/resources/medical-marijuana-research-studies/myasthenia-gravis-medical-marijuana-research/



